Электронная конфигурация представляет собой особую формулу, которая указывает, как электроны располагаются по различным оболочкам атома химического элемента или молекулы.
Обычно электронная конфигурация записывается для атомов в их основном состоянии.
Для определения электронной конфигурации элемента существуют следующие правила.
- Принцип заполнения говорит, что электроны в основном состоянии атома заполняют орбитали в определенной последовательности, которая определяется их энергетическими уровнями. При этом, орбитали с низшей энергией всегда заполняются первыми.
- Принцип запрета Паули устанавливает, что на одной орбитали может находиться не более двух электронов, причем они должны иметь противоположные спины, то есть разные спиновые числа.
- Правило Хунда говорит, что заполнение орбиталей одной подоболочки начинается с одиночных электронов с параллельными спинами (одинаковыми по знаку). И только после того, как все орбитали станут заняты одиночными электронами, может происходить окончательное заполнение орбиталей парами электронов с противоположными спинами.
Таким образом, электронная конфигурация является основополагающим понятием в химии, которое описывает распределение электронов в атомах и молекулах. Она основана на определенных правилах и принципах заполнения орбиталей с учетом их энергетических уровней и спиновых чисел электронов.
Содержание страницы
Электронные структуры элементов малых и больших периодов
Чтобы понять причины периодической повторяемости свойств элементов, необходимо рассмотреть последовательность изменения электронных структур.
Так как всякое свойство элемента есть лишь следствие, обусловленное внутриатомной структурой, в частности строением электронных слоев.
В таблице 1 показано размещение электронов в электронных слоях атомов каждого элемента.
Атом водорода имеет наиболее простую электронную структуру. Вокруг его ядра движется один электрон по сферической s-орбитали (находится на s-оболочке).
Гелий, следующий за водородом, имеет уже два электрона с антипараллельными спинами на s-орбитали.
Поскольку электроны находятся на первом ближайшем к ядру слое, т. е. главное квантовое число равно 1, то по формуле х = 2n2 максимальное число электронов на первом слое равно 2.
Следовательно, атом гелия имеет завершенную структуру.
Если изобразить условно квадратиками электронные орбитали, а стрелками — электроны, то электронная структура атома водорода будет выглядеть следующим образом:
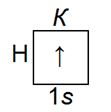
Такое условное изображение электронного слоя атома называется изображением электронной конфигурации атомов.
Выражение 1s1 обозначает следующее: цифра 1 перед буквенным обозначением указывает номер слоя, буква s — оболочку, а индекс 1 — сколько электронов имеется на данной оболочке.
Электронная структура гелия:
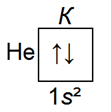
В связи с тем, что внешние электроны водорода и гелия находятся на s-орбитали, говорят, что эти элементы относятся к семейству.
• При изучении электронных конфигураций атомов зарисовывайте их в тетрадь и рядом пишите буквенные обозначения, например:

Или

Это поможет затем сопоставить и сделать выводы. Периоды отделяйте чертой.
Второй период
Второй период начинается литием. Атом лития имеет два электронных слоя: первый (К) слой завершенный, как у гелия, а на втором имеется один электрон, который находится на s-орбитали второго слоя.
Электронная структурa атома лития изображается так:

Поскольку завершению подлежит s-оболочка второго слоя, литии также следует отнести к семейству s-элементов.
Первый электронный слой (К) следующего за литием бериллия, как и у всех элементов второго периода, имеет структуру гелия, т. е. содержит 2 s-электрона.
Два электрона второго слоя атома бериллия располагаются на s-оболочке, которая теперь полностью застроена электронами с антипараллельными спинами.
Строение электронных слоев атома бериллия можно изобразить так:
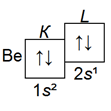
Как видно из схемы, бериллий также относится к семейству s- элементов.
Таким образом, у бериллия во втором слое имеется 2 электрона. Однако в соответствии с формулой x=2n2 во втором слое может быть размещено 8 электронов.
По-этому в атомах следующих за бериллием элементов начинает застраиваться p-оболочка второго слоя.
На каждой из трех р-орбиталей может размещаться также по 2 электрона с антипараллельными спинами. Рассмотрим структуру электронных слоев атома бора.
Первый слой такой же, как у гелия, во втором слое имеется три электрона: два из них занимают s-оболочку и один расположен на р-оболочке.
Электронная структурa атома бора:
Бор относится уже к семейству р-элементов, так как у него начинается застройка р-оболочки.
Следующий за бором углерод имеет на р-оболочке еще один электрон. Как уже говорилось, энергетически выгоднее, когда электроны занимают как можно более орбиталей.
Поэтому очередной р-электрон углерода попадает на другую р-орбиталь.
Электронная структурa атома углерода:
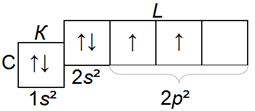
Структура электронных слоев атома азота N следующая:
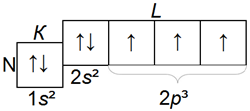
Таким образом, теперь на втором слое L имеется пять электронов. Три р-орбитали имеют по одному неспаренному электрону.
При дальнейшей достройке р-оболочки (у кислорода, фтора и неона) заполняются свободные места на р-орбиталях второго слоя.
Электронная структурa атома кислорода, фтора, неона:
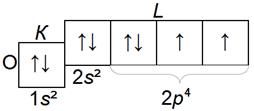
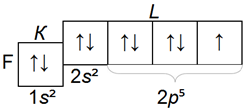
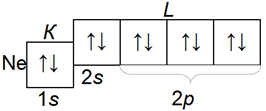
кислород, фтор и неон, так же как бор, углерод и азот, принадлежат к семейству p-элементов.
Электронные слои атома неона имеют полностью застроенные электронные оболочки и у элементов III периода должен возникнуть третий электронный слой.
Застройка этого слоя начинается, как обычно, с заполнения s-оболочки, поэтому в начале III периода, так же как и в начале II периода, находятся s-элементы.
Электронная структурa атома натрия и магния:
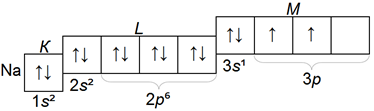

Порядок заполнения р-оболочки атомов элементов III периода такой же, как и во II периоде.
Алюминий, являясь аналогом бора, имеет структуру:
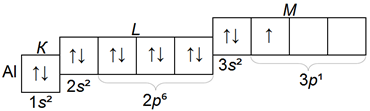
Кремний — аналог углерода:
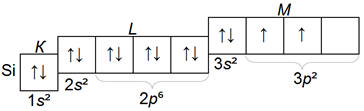
➡️ 20. Фосфор — аналог азота. Изобразите электронную конфигурацию его атома. (См. Ответ)
21. Изобразите электронную конфигурацию его атома натрия и скажите, к какому семейству — s— , p— или d— элементов он относится.
22. Изобразите электронную конфигурацию атома кремния и скажите, к какому семейству он относится. Объясните, почему 3р— электроны кремния располагаются на двух орбиталях, а не на одной?
Сера — аналог кислорода — имеет в р— оболочке слоя М два неспаренных электрона:
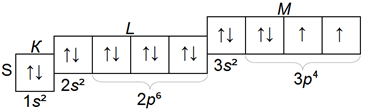
У хлора — лишь один:
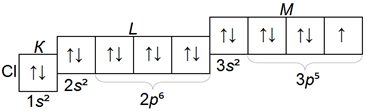
У аргона р— оболочка М— слоя полностью завершена:
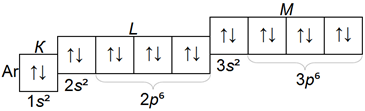
Однако емкость третьего электронного слоя М этим не исчерпывается. В соответствии с формулой х = 2n2 поскольку n = 3, на нем может располагаться до 18 электронов, а имеется лишь 8.
Другими словами, в слое М полностью застроены s— и р-оболочки, а d-оболочка, которая может вмещать 10 электронов, еще не застраивалась.
Вместе с тем слой М, являясь внешним слоем, не может далее застраиваться, так как в любом внешнем слое может размещаться не более 8 электронов.
Кроме того, застройка s-оболочки N-слоя энергетически выгоднее, чем застройка d-оболочки М— слоя, поэтому в начале IV периода мы видим снова s— элементы калий, и кальций, имеющие следующую структуру электронных слоев.
Электронная структурa атома калия и кальция:
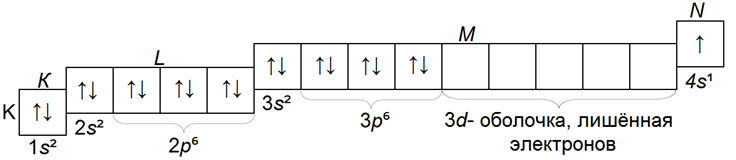

Застройка р-оболочки N-слоя при отсутствии электронов на d-оболочке М-слоя энергетически невыгодна, поэтому у скандия начинается застройка 3d-оболочки.
Электронная структурa атома скандия:

Застройка d-оболочки предвнешнего слоя продолжается у элементов четвертого периода, начиная от скандия и кончая цинком.
Эти элементы принадлежат к d-семейству.
➡️ 23. Перечислите элементы d-семейства IV периода.
24. Пользуясь табл. 1 , изобразите электронную конфигурацию третьего и четвертого электронных слоев атомов титана, ванадия, марганца, железа и цинка. (См. Ответ)
От галлия до криптона происходит застройка р-оболочки N-слоя. В результате внешний N-слой приобретает восьмиэлектронную структуру (октет).
➡️ 25. Изобразите электронную конфигурацию четвертого и пятого слоев элементов стронция, иттрия, технеция, кадмия, сурьмы, ксенона. (См. Ответ)
Электронные структуры элементов VI периода в данном курсе не рассматриваются.
Зависимость изменения свойств элементов в периодах и группах от изменения электронных структур
Рассмотрение электронных структур элементов позволяет заметить постепенность застройки каждой очередной электронной оболочки при переходе от одного элемента к другому внутри периода по мере возрастания порядковых номеров.
С этим связан переход от элементов с металлическими к элементам с неметаллическими свойствами.
С возрастанием зарядов ядер атомов элементов внутри периода притяжение ядром электронных оболочек усиливается — происходит своего рода «сжатие» их, т. е. уменьшение радиуса атома.
Этим объясняется то, что в начале периода располагаются элементы, имеющие больший радиус атома и малое число электронов на внешнем электронном слое.
Такая структура характерна для металла, поэтому в начале каждого периода находятся металлы.
Например, радиус атома лития превосходит радиусы атомов кислорода и фтора, а число электронов на внешнем слое меньше.
Понятно, что электрон, находящийся дальше от ядра, легче отрывается от своего атома. Относительная легкость отдачи электрона является главной особенностью элемента с металлическими свойствами.
Металлы сравнительно легко отдают электроны, но не могут принимать их дополнительно для застройки электронных оболочек внешнего слоя.
В этом случае говорят, что атомы металлов обладают слабой электроотрицательностью.
Электроотрицательностью элемента называют способность его атома притягивать и удерживать около себя электроны, необходимые для завершения внешнего электронного слоя.
Чем выше электроотрицательность, тем ярче выражены неметаллические свойства элементов.
Рассмотрите приведенную на стр. шкалу электроотрицательности элементов.
По мере возрастания зарядов ядер атомов в периоде число электронов во внешнем слое увеличивается, радиус атома уменьшается, а вместе с тем постепенно уменьшается легкость отдачи электронов с этого слоя, т. е. возрастают электроотрицательность и неметалличность свойств.
Наконец каждый период заканчивается инертным элементом, свойства которого не позволяют причислить его к металлам или неметаллам.
Это объясняется структурой его внешнего слоя, представляющей собой полный октет. Устойчивостью такого октета объясняется пассивное поведение инертных элементов в химических реакциях.
➡️ 26. Почему в каждом периоде с возрастанием порядкового номера свойства элементов меняются от металлов к неметаллам и инертным элементам? (См. Ответ)
27. Как влияет изменение величины радиуса атома в периоде на изменение свойств элементов? 28. Чем объясняется химическая пассивность инертных элементов?
Поскольку свойства элементов определяются в основном структурой электронных оболочек внешнего электронного слоя, сходство свойств отдельных элементов, находящихся в разных периодах, объясняется сходством структур их внешнего электронного слоя.
Например, близкими по свойствам оказываются этакие элементы, г как литий, натрий, калий — щелочные металлы, имеющие один электрон на s-оболочке внешнего слоя.
Элементы сера, селен, теллур, также проявляющие близкие химические свойства, имеют шести электронный внешний слой: два электрона на s-оболочке и четыре на р-оболочке.
Другими словами, периодическая повторяемость свойств обусловливается периодической повторяемостью структур электронных оболочек внешнего электронного слоя.
Этим же объясняется сходство свойств элементов по подгруппам в периодической системе.
Как известно, внутри подгруппы свойства элементов по мере возрастания порядковых номеров меняются, усиливается металлическая активность.
Например, у бария по сравнению с магнием, которая выражается в большей легкости отдачи электронов, т. е. в уменьшения электроотрицательности.
С другой стороны, падает неметаллическая активность, т.е. снижается способности притягивать к себе электроны.
Объясняется это увеличением числа электронных слоев, т. е. увеличением атомного радиуса. Чем дальше от ядра электроны внешнего слоя, тем слабее они удерживаются ядром.
По тем же причинам уменьшается неметаллическая активность йода по сравнению с фтором и хлором.
Этим объясняется снижение неметаллических свойств у мышьяка по сравнению с азотом и фосфором и т.д.
➡️ 29. Как объяснить периодическую повторяемость свойств с точки зрения электронных конфигураций? (См. Ответ)
30. Почему в подгруппах с возрастанием зарядов ядер усиливаются металлические свойства и ослабевают неметаллические?
31. Какой из элементов проявляет более ярко выраженные металлические свойства — титан или хром? Обоснуйте ваше мнение с точки зрения внутриатомной структуры.
32. У какого из элементов более ярко выражены неметаллические свойства — у фосфора или висмута? Объясните это с точки зрения строения их атомов.
Рассмотрение порядка застройки электронных оболочек атомов элементов малых и больших периодов позволяет заметить, что число электронов, расположенных на внешнем электронном слое атомов элементов главных подгрупп, всегда совпадает с номером группы.
Для элементов побочных подгрупп это наблюдается только в 1-й и 2-й группах. Поскольку строением внешнего электронного слоя определяются свойства элементов и их соединений.
В частности валентность элементов, возможность определять величину валентности, пользуясь номером группы в периодической системе, приобретает немаловажное значение.
Обращает на себя внимание также то, что элементы, принадлежащие к разным подгруппам, обладают различными свойствами.
Например, бром является типичным неметаллом, а марганец обладает хорошо выраженными металлическими свойствами.
Причина также заключается в различии структуры внешнего электронного слоя: марганец принадлежит к семейству d-элементов.
То есть в атоме марганца d-оболочка предвнешнего слоя находится в процессе застройки, в результате чего внешний электронный слой марганца имеет два s-электрона.
Бром принадлежит к семейству р-элементов, так как у него застраивается р-оболочка внешнего слоя, на котором располагается 7 электронов.
➡️ 33. Основываясь на электронных конфигурациях атомов, объясните, почему хром и селен обладают различными свойствами. (См. Ответ)
34. В чем причина различия химических свойств кальция и цинка?
Таблица электронные слои элементов и расположение на них электронов
| Электронные слои элементов и расположение на них электронов | |||||||||
| № Периода | № Элемента | Название элемента | Химический знак | Число электронов в слое | |||||
| K | L | M | N | O | P | ||||
| I | 1 | Водород | H | 1 | |||||
| 2 | Гелий | He | 2 | ||||||
| II | 3 | Литий | Li | 2 | 1 | ||||
| 4 | Бериллий | Be | 2 | 2 | |||||
| 5 | Бор | B | 2 | 3 | |||||
| 6 | Углерод | C | 2 | 4 | |||||
| 7 | Азот | N | 2 | 5 | |||||
| 8 | Кислород | O | 2 | 6 | |||||
| 9 | Фтор | F | 2 | 7 | |||||
| 10 | Неон | Ne | 2 | 8 | |||||
| III | 11 | Натрий | Na | 2 | 8 | 1 | |||
| 12 | Магний | Mg | 2 | 8 | 2 | ||||
| 13 | Алюминий | Al | 2 | 8 | 3 | ||||
| 14 | Кремний | Si | 2 | 8 | 4 | ||||
| 15 | Фосфор | P | 2 | 8 | 5 | ||||
| 16 | Сера | S | 2 | 8 | 6 | ||||
| 17 | Хлор | Cl | 2 | 8 | 7 | ||||
| 18 | Аргон | Ar | 2 | 8 | 8 | ||||
| IV | 19 | Калий | K | 2 | 8 | 8 | 1 | ||
| 20 | Кальций | Ca | 2 | 8 | 8 | 2 | |||
| 21 | Скандий | Sc | 2 | 8 | 9 | 2 | |||
| 22 | Титан | Ti | 2 | 8 | 10 | 2 | |||
| 23 | Ванадий | V | 2 | 8 | 11 | 2 | |||
| 24 | Хром | Cr | 2 | 8 | 13 | 1 | |||
| 25 | Марганец | Mn | 2 | 8 | 13 | 2 | |||
| 26 | Железо | Fe | 2 | 8 | 14 | 2 | |||
| 27 | Кобальт | Co | 2 | 8 | 15 | 2 | |||
| 28 | Никель | Ni | 2 | 8 | 16 | 2 | |||
| 29 | Медь | Cu | 2 | 8 | 18 | 1 | |||
| 30 | Цинк | Zn | 2 | 8 | 18 | 2 | |||
| 31 | Галлий | Ga | 2 | 8 | 18 | 3 | |||
| 32 | Германий | Ge | 2 | 8 | 18 | 4 | |||
| 33 | Мышьяк | As | 2 | 8 | 18 | 5 | |||
| 34 | Селен | Se | 2 | 8 | 18 | 6 | |||
| 35 | Бром | Br | 2 | 8 | 18 | 7 | |||
| 36 | Криптон | Kr | 2 | 8 | 18 | 8 | |||
| V | 37 | Рубидий | Rb | 2 | 8 | 18 | 8 | 1 | |
| 38 | Стронций | Sr | 2 | 8 | 18 | 8 | 2 | ||
| 39 | Иттрий | Y | 2 | 8 | 18 | 9 | 2 | ||
| 40 | Цирконий | Zr | 2 | 8 | 18 | 10 | 2 | ||
| 41 | Ниобий | Nb | 2 | 8 | 18 | 12 | 1 | ||
| 42 | Молибден | Mo | 2 | 8 | 18 | 13 | 1 | ||
| 43 | Технеций | Tc | 2 | 8 | 18 | 13 | 2 | ||
| 44 | Рутений | Ru | 2 | 8 | 18 | 15 | 1 | ||
| 45 | Родий | Rh | 2 | 8 | 18 | 16 | 1 | ||
| 46 | Палладий | Pd | 2 | 8 | 18 | 18 | 0 | ||
| 47 | Серебро | Ag | 2 | 8 | 18 | 18 | 1 | ||
| 48 | Кадмий | Cd | 2 | 8 | 18 | 18 | 2 | ||
| 49 | Индий | In | 2 | 8 | 18 | 18 | 3 | ||
| 50 | Олово | Sn | 2 | 8 | 18 | 18 | 4 | ||
| 51 | Сурьма | Sb | 2 | 8 | 18 | 18 | 5 | ||
| 52 | Теллур | Te | 2 | 8 | 18 | 18 | 6 | ||
| VI | 53 | Йод | I | 2 | 8 | 18 | 18 | 7 | |
| 54 | Ксенон | Xe | 2 | 8 | 18 | 18 | 8 | ||
| 55 | Цезий | Cs | 2 | 8 | 18 | 18 | 8 | 1 | |
| 56 | Барий | Ba | 2 | 8 | 18 | 18 | 8 | 2 | |
| 57 | Лантан | La | 2 | 8 | 18 | 18 | 9 | 2 | |
| 58 | Церий | Ce | 2 | 8 | 18 | 20 | 8 | 2 | |
| 59 | Празеодим | Pr | 2 | 8 | 18 | 21 | 8 | 2 | |
| 60 | Неодим | Nd | 2 | 8 | 18 | 22 | 8 | 2 | |
| 61 | Прометий | Pm | 2 | 8 | 18 | 23 | 8 | 2 | |
| 62 | Самарий | Sm | 2 | 8 | 18 | 24 | 8 | 2 | |
| 63 | Европий | Eu | 2 | 8 | 18 | 25 | 8 | 2 | |
| 64 | Гадолиний | Gd | 2 | 8 | 18 | 25 | 9 | 2 | |
| 65 | Тербий | Tb | 2 | 8 | 18 | 27 | 8 | 2 | |
| 66 | Диспрозий | Dy | 2 | 8 | 18 | 28 | 8 | 2 | |
| 67 | Гольмий | Ho | 2 | 8 | 18 | 29 | 8 | 2 | |
| 68 | Эрбий | Er | 2 | 8 | 18 | 30 | 8 | 2 | |
| 69 | Тулий | Tm | 2 | 8 | 18 | 31 | 8 | 2 | |
| 70 | Иттербий | Yb | 2 | 8 | 18 | 32 | 8 | 2 | |
| 71 | Лютеций | Lu | 2 | 8 | 18 | 32 | 9 | 2 | |
| 72 | Гафний | Hf | 2 | 8 | 18 | 32 | 10 | 2 | |
| 73 | Тантал | Ta | 2 | 8 | 18 | 32 | 11 | 2 | |
| 74 | Вольфрам | W | 2 | 8 | 18 | 32 | 12 | 2 | |
| 75 | Рений | Re | 2 | 8 | 18 | 32 | 13 | 2 | |
| 76 | Осмий | Os | 2 | 8 | 18 | 32 | 14 | 2 | |
| 77 | Иридий | Ir | 2 | 8 | 18 | 32 | 15 | 2 | |
| 78 | Платина | Pt | 2 | 8 | 18 | 32 | 17 | 1 | |
| 79 | Золото | Au | 2 | 8 | 18 | 32 | 18 | 1 | |
| 80 | Ртуть | Hg | 2 | 8 | 18 | 32 | 18 | 2 | |
| 81 | Таллий | Tl | 2 | 8 | 18 | 32 | 18 | 3 | |
| 82 | Свинец | Pb | 2 | 8 | 18 | 32 | 18 | 4 | |
| 83 | Висмут | Bi | 2 | 8 | 18 | 32 | 18 | 5 | |
| 84 | Полоний | Po | 2 | 8 | 18 | 32 | 18 | 6 | |
| 85 | Астат | At | 2 | 8 | 18 | 32 | 18 | 7 | |
| 86 | Радон | Rn | 2 | 8 | 18 | 32 | 18 | 8 | |
Быстрые ответы?
Электронная оболочка атома состоит из движущихся вокруг ядра электронов (е-). Число электронов N(e -) в электронной оболочке нейтрального атома равно числу протонов Z в его ядре.
Масса протона примерно равна массе нейтрона и в 1840 раз больше массы электрона, поэтому масса атома практически равна массе ядра.
Электронная структура атома серы S I содержит 16 электронов на 5 оболочках, из которых 12 полностью заполнили 4 оболочки и 4 заполняют 3p 4 — оболочку.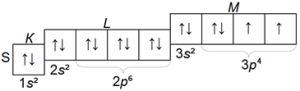
В химии и атомной физике электронную оболочку можно рассматривать как орбиту, по которой электроны движутся вокруг ядра атома.
Ближайшая к ядру оболочка называется «1 оболочка» (также называемая «K оболочка»), за ней следует «2 оболочка» (или «L оболочка»), затем «3 оболочка» (или «M оболочка») и так далее все дальше и дальше от ядра.



Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.