Полоний это радиоактивный химический элемент, имеет формулу Po, образуется при превращении радия и урана.
Это редкий природный элемент и высокорадиоактивный металл без стабильных изотопов, он был открыт в 1898 году Марией Склодовской Кюри и Пьером Кюри.
Он чрезвычайно токсичен даже в небольших количествах и называется идеальным ядом.

Содержание страницы
Что такое полоний
(Polonium; от лат. Polonia— Польша), Ро — радиоактивный химический элемент относится к группе 16 и периоду 6 в периодической таблице элементов (устаревшая VI группы периодической системы элементов).
Атомный номер 84, атомная масса дописать наиболее долгоживущего изотопа 209.
Мягкий металл серого цвета. Наиболее характерная степень окисления + 4; известны также степени окисления — 2, + 2 и + 6. Стабильные изотопы неизвестны.
Полоний существует в двух модификациях: низкотемпературной альфа-форме с простой кубической решеткой и бета-форме с простой ромбоэдрической решеткой.
Фазовое превращение происходит при т-ре около 36° С.
Плотность металлического альфа-полония (т-ра 20° С) 9,196 г/см3 tпл 254° С; tкип 962° С.
Температурный коэфф. линейного расширения (от —196 до + 30° С) 2,3 х 10-5 град-1; удельное электрическое сопротивление (т-ра 0° С) альфа-полония 42± 10мком х см.
Соединения полония с установленным составом: трех-, дву- и моноокись, тетра- и дигалогениды, моносульфид, основные нитрат и сульфат, карбонат, хромат, йодат, фосфат и др.
Полоний сильно токсичен. Предельно допустимое содержание его в воздухе 4 х 10—11 мг/м3. Работы с ним проводят в герметических боксах со спец. фильтрационной системой.
Физические свойства
Полоний — металл серебристо-белого цвета, существующий в двух аллотропных модификациях, переход из одной в другую совершается при 36° С.
Однако из-за собственной радиоактивности полоний уже при комнатной температуре находится в высокотемпературном режиме.
Температура металлического полония всегда выше окружающей среды из-за теплоты, выделяемой при торможении α-излучения, в самой массе полония.
Слой воздуха на металле светится голубоватым светом, под действием его излучения светится и ампула и сам металл.
Выделяющееся количество теплоты так велико, что образец полония способен даже расплавиться.
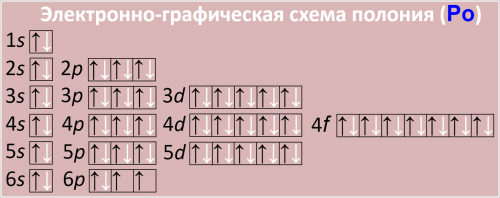
Полная электронная формула атома полония в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p4
Сокращенная электронная конфигурация Po:
[Xe] 4f14 5d10 6s2 6p4
Химические свойства полония
Легкоплавкость он похож на свинец и висмут, по электрохимическому поведению — на благородные металлы .
Достаточно хорошо изучены многочисленные соединения полония от простого оксида РоО2 до сложных комплексных соединений.
При нагревании полоний образует твердый, легко возгоняющийся оксид РоО2.
Он может быть окислителем, восстанавливаясь до Ро, а при растворении в воде дает основание:
РоО3 + 2Н2О = Ро(ОН)4
С галогенводородными кислотами дает соль:
PoO2 + 4HCI = PоCI4 + Н2О
С кислотами, особенно окисляющими, полоний реагирует как типичный металл:
Ро + 8HNO3 = Рo(NO3)4 + 4NO2 + 4H2O
Соединение полония с водородом Н2Ро неустойчиво. В отличие от теллура полоний способен входить в состав значительного числа комплексных анионов типа [PoI6]² ˉ
Изотопы
Из 27 радиоактивных изотопов наиболее долгоживущие — изотопы 209Ро, 208Ро и 210Ро с периодами полураспада соответственно 42 года, 2,9 года и 138,4 дней.
Изотопы 209Ро и 208Ро практически не используются, поскольку образуются в ничтожных количествах при бомбардировке висмута протонами или дейтронами.
Наиболее доступный изотоп 210Ро, образующийся при распаде радия, открыт польским химиком и физиком М. Склодовской-Кюри при изучении радиоактивности урановых минералов.
Равновесное содержание изотопа 210Ро в радии 0,02%. Содержание полония в земной коре 3-10 14%.
Характеристика элемента
Полоний обладает особыми качествами, обусловленными его радиоактивностью. Он образуется в результате превращений урана, радия и является их дочерним элементом.
Наибольший интерес представляет изотоп 210Ро, который легко может быть получен в чистом виде и имеет значительный период полураспада (Т½ = 138 дня).
У полония отсутствуют продукты распада, а радиоактивность его, хотя и интенсивная, состоит только из α -излучения.
Полоний — более благородный металл, чем серебро, поэтому он может быть вытеснен серебром из раствора. По химическому поведению Ро напоминает Bi и Те.
Аналогия между полонием, теллуром и висмутом была установлена еще в 1903 г.
История
В. Марквальд погрузил в солянокислый раствор, где находились остатки от переработки урановой руды, чистую пластинку из висмута.
На пластинке оказалось какое-то вещество. Оно было радиоактивным. Реакция этого вещества были похожи на теллур и Марквальд решил назвать его «радиотеллур».
Однако, когда определили период полураспада (основную характеристику любого радиоактивного элемента), то оказалось, что на пластинке вместе с висмутом находился полоний.
Первооткрыватели полония Пьер и Мария Кюри, естественно, не знали о коварстве этого обнаруженного ими элемента.
До сих пор страницы записной книжки Марин Кюри настолько радиоактивны, что засвечивают фотопленку, завернутую в светонепроницаемую бумагу.
Получение полония
Промышленными «месторождениями» полония являются заводы по переработке урановой руды и атомные реакторы. В последних путем облучения висмута можно получить значительные количества ²¹ºРо.
В лаборатории металлический полонии получают, пропуская ток через водный раствор, содержащий ионы полония.
Он осаждается на катоде, в качестве которого лучше взять золотую фольгу, чтобы легче было отделить полоний.
Дело в том, что он сильно адсорбируется, например, чтобы удалить его с платиновой фольги, надо ее долго нагревать при 1000° С.
Так же трудно удалить этот металл с химической посуды и приборов. Все это требует специальных мер предосторожности и защиты, так как α-излучение полонии ионизирует воздух, вещества к растворы.
Получение полония облучением висмута
Миллиграммовые количества полоний получают, облучая висмут нейтронами.
Основные методы отделения вещества от висмута заключаются в растворении облученного висмута в к-те и восстановлении полония до элементарного состояния.
Очищают вакуумной сублимацией.
Применение полония
Полоний применяют как источник тепла в термоэлектрических генераторах тока.
Сплавы с бериллием используют для изготовления нейтронных источников с низкой гамма-активностью.
Обращение с полонием требует особой осторожности, так как полоний способен довольно легко проникать сквозь кожные покровы.
Работают с полонием лишь в, герметических боксах, так как, кроме всего, он способен переходить в аэрозольное состояние и воздух становится опасным .
Тепловыделение полония нашло применение для создания атомных обогревателей в системах космических аппаратов.
Полониевая атомная печка советского «Лунохода-2» поддерживала необходимую температуру в приборном отсеке в течение нескольких месяцев, в то время как за бортом было —130° С.
Включение полония в сплавы для изготовления свечей внутреннего сгорания облегчает зажигание сгорания облегчает зажигание топлива при запуске двигателей в холодном состоянии.
С помощью полония создаются источники нейтронного излучения.
Для этого его сплавляют с элементом, способным поглощать о-излучение, испускаемое полонием, а взамен создавать поток нейтронов. Таким элементом является, например, бериллий.
Сам полоний используется как α-излучатель при изучении действия этих лучей на жидкости и организмы.
Интересные факты о полонии?
- Его химические свойства аналогичны свойствам висмута и теллура. (Полоний-самый тяжелый металл из халькогенов, также известный как «кислородное семейство».)
- В нем нет стабильных изотопов. (Период полураспада Po-210 составляет всего 138 дней).
- Это радиоактивный полуметалл, содержащийся в урановых рудах. Он используется в некоторых устройствах для устранения статического электричества в таких процессах, как производство листового пластика, прокатной бумаги и т.д.
- Производство листовых пластмасс и прядение синтетических волокон.
- Он испускает альфа-частицы после распада.
- Он классифицируется как металл, потому что электропроводность полония уменьшается с повышением его температуры.
- Если полоний 210 попадает внутрь организма через вдыхание или проглатывание, результаты могут быть смертельными.
- У курильщиков табака содержание полония-210 больше, чем у некурящих, потому что курение вызывает его накопление в легких.
Интересный факт
Уран и торий были единственными известными радиоактивными элементами до того, как польско-французский физик Мария Кюри открыла полоний в 1898 году.
Кюри назвала полоний в честь своей родины, Польши. Польша в то время не была независимой страной и управлялась разделом Германии, России и Австро-Венгрии.
В надежде назвать элемент в честь своей родной земли, мадам Кюри сделала это, чтобы подчеркнуть его несамостоятельность.
Полоний был первым элементом, который был назван в связи с политическими разногласиями.
Часто задаваемые вопросы ответы о полонии?
Напишите об использовании полония?
Полоний используется в:
Атомная бомба: Комбинация полония и бериллия действует как инициатор бомбы.
Благодаря своей высокой радиоактивности полоний имеет коммерческое применение, он используется в качестве легкого источника тепла для термоэлектрической энергии на спутниках и других космических аппаратах.
Благодаря альфа-излучению 1 грамм полония может приобрести температуру до 500°C. Благодаря этому свойству полония он является полезным источником тепла для космической техники.
(Концентрация Po-210 в воде измеряется pCi/л, пикокурий — это единица измерения радиоактивности в воздухе и воде, а пикокурий составляет одну миллионную или триллионную часть кюри).
Как производится полоний?
Полоний-210 присутствует в очень небольших количествах в почве и в атмосфере, но в естественных условиях он не встречается в смертельных концентрациях.
Он может быть изготовлен в ядерном реакторе путем бомбардировки изотопа висмут-209 нейтроном.
Что опаснее Цианистый водород или Полоний?
Оба они одинаково токсичны, HCN является острым токсином и приведет к мгновенной смерти.
В то время как радиоактивные изотопы полония убьют в течение нескольких дней или недель после радиационного отравления.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.