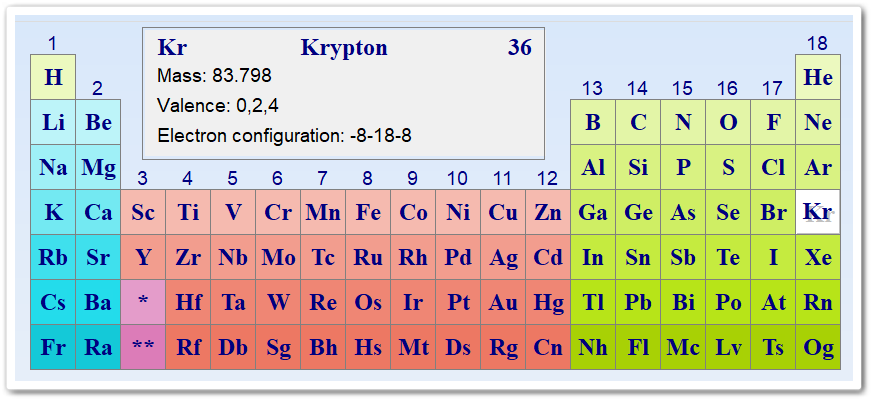
(Kryptonum; от греч. — скрытый), Кr — химический элемент 18-й группы, четвёртого периода периодической системы химических элементов (устаревшая классификация: VIII группы) периодической системы элементов.
Атомный номер 36, атомная масса 83,80. Инертный газ.
Атмосферный криптон состоит из смеси шести стабильных изотопов, среди к-рых преобладает изотоп 84Кr (56,90%). Получены 15 радиоактивных изотопов.
Криптон открыли (1898) англ. ученые У. Рам-эай и М. Траверс при спектроскопическом изучении труднолетучих фракций жидкого воздуха.
Криптон — редкий, рассеянный газ, встречается гл. обр. в атмосфере (3 • 10-4%).
Содержание страницы
- 1. Физические свойства
- 2. Получение
- 3. История
- 4. В природе
Физические свойства
Осн. термодинамические параметры — критическая точка: Т =209,35 К; ρкр = 54,3 ат; ρkр = 0,908 г/см3; тройная точка: Т, = 115,78 К;ρTP = 548,7мм рm . ст ., ρTP = 2,826 г/см3.
Нормальная т-ра кипения 119,80 К (при атм. давлении); т-ра плавления 116,55 К; теплота плавления 390,7 кал/моль) теплота испарения (в точке кипения) 2258 кал/моль; теплота сублимации (т-ра 0 К) 2666 кал/моль.
Газообразный криптон — без цвета и запаха, состоит из одноатомных молекул.
При т-ре 0° С и давлении 760 мм р. ст. его плотность 3,7493 кг/м3; коэфф. теплопроводности 2,08 х 10-5 кал/см — сек • град, растворимость в воде: 99,1 см3/л (т-ра 0° С) и 28,5 см3/л (т-ра 80° С).
В жидком состоянии плотность 2,413 г/см3; коэфф. теплопроводности 21,3 X 10-5 кал/см • сек • град.
Количество газа, образующегося при испарении 1 л жидкости, — 643,6 л.
Решетка твердого криптона — гранецентрированная кубическая с периодом (т-ра 4,2 К) а = 5,646 А.
Криптон исследовался гл. обр. по кривой равновесия кристалл — пар.
В интервале т-р 114 — 12 К плотность его изменяется от 2,799 до 3,092 г/см3; теплоемкость Cv уменьшается с 5,14 до только при пониженной т-ре.
Подобно другим инертным газам криптон образует соединения, связь в к-рых осуществляется межмолекулярными силами (напр., Кr • 6Н2О).
Электронная формула атома криптона в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6
Сокращенная электронная конфигурация Kr:
[Ar] 3d10 4s2 4p6
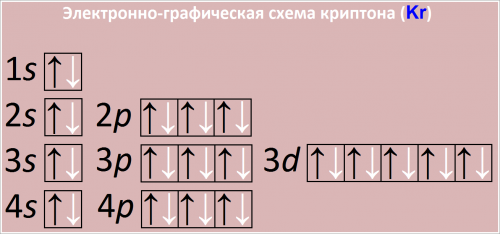
Рис. Схема распределения электронов по атомным орбиталям в атоме криптона.
Получение
Обычно получают как побочный продукт при разделении воздуха методом глубокого охлаждения.
Применяют гл. обр. в электровакуумной технике.
Криптоновые лампы накаливания служат дольше обычных, поскольку тяжелые атомы затрудняют испарение вольфрамовой нити.
История
Впервые криптоном был назван газ, выделенный Уильямом Рамзаем из минерала клевеита. Но очень скоро пришлось это имя снять и элемент «закрыть».
Английский спектроскопист Уильям Крукс установил, что газ не что иное, как уже известный по солнечному спектру гелий.
Спустя три года, в 1898 г., название «криптон» вновь появилось, его присвоили новому элементу, новому благородному газу.
Открыл его опять же Рамзай, и почти случайно — «шел в дверь, попал в другую».
Намереваясь выделить гелий из жидкого воздуха, ученый вначале пошел было по ложному следу: он пытался обнаружить гелий в высококипящих фракциях воздуха.
Разумеется, гелия, самого низко-кипящего из всех газов, там не могло быть, и Рамзай его не нашел.
Зато он увидел в спектре тяжелых фракций желтую и зеленую линии в тех местах, где подобных следов не оставлял ни один из известных элементов.
Так был открыт криптон, элемент, имя которого в переводе с греческого значит «скрытный».
Название несколько неожиданное для элемента, который сам шел в руки исследователя.
В природе
Известно, что гелий, радон, почти весь аргон и вероятно, неон нашей планеты имеют радиогенное происхождение, т. е. они — продукты радиоактивного распада. А как обстоит дело с криптоном?
Среди известных природных ядерных процессов, порождающих криптон, наибольший интерес представляет самопроизвольное деление ядер урана и тория.
В 1939 г. Г. Н. Флеров и К. А. Петржак установили» что в природе (очень редко) происходит самопроизвольное расщепление ядер урана-238 на два осколка примерно равной массы.
Еще реже таким же образом делятся ядра 232Th и 235U. Осколки —это атомы изотопов средней части периодической системы элементов.
Будучи неустойчивыми («перегруженными» нейтронами), эти осколки проходят по цепи последовательных бета-распадов.
Среди конечных продуктов распада есть и стабильные тяжелые изотопы криптона.
Подсчеты, однако, показывают, что радиоактивный распад (включая деление урана-235 медленными нейтронами) — не главный «изготовитель» криптона.
За время существования Земли (если считать его равным 4,5 млрд. лет) эти процессы смогли выработать не более двух-трех десятых процента существующего на нашей планете элемента № 36.
Сегодня на этот вопрос даются два обоснованных, но разных по смыслу ответа.
Часть ученых считает, что земной криптон возник в недрах планеты.
Прародителями криптона были трансурановые элементы, некогда существовавшие на Земле, но теперь уже «вымершие».
Следы их существования усматривают в том, что в земной коре есть элементы-долгожители нептуниевого радиоактивного ряда (ныне целиком искусственно воссозданного).
Другой подобный след — микроколичества плутония и нептуния в земных минералах, хотя они могут быть и продуктами облучения урана космическими нейтронами.
В пользу этой гипотезы говорит тот факт, что искусственно полученные актиноиды (не все, но многие) — активные «генераторы» криптона.
Их ядра самопроизвольно делятся намного чаще, чем ядра атомов урана.
Сравните периоды полураспада по спонтанному делению: 8,04 · 1015 лет —для урана-238 и всего 2000 лет —для калифорния-246.
А для фермия и менделевия соответствующие периоды полураспада измеряются всего лишь часами.
Иного мнения придерживается другая группа ученых. На их взгляд, земной криптон (как и ксенон) пришел на Землю из Вселенной, в процессе зарождения Земли.
Он присутствовал еще в протопланетном облаке, его сорбировала первичная земная материя, откуда он потом, при разогреве планеты, выделился в атмосферу.
Это мнение тоже опирается на факты. В его пользу говорит, в частности, то, что криптон — газ тяжелый, малолетучий и относительно легко конденсирующийся.
В отличие от иных компонентов первичной атмосферы вряд ли смог бы оставить Землю да первых фазах ее формирования.
Кто же прав? Скорее всего, правы обе стороны: криптон нашем планеты, вероятно, представляет собою смесь газов как космического, так и земного происхождения.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.