Прометий (Pm) — это неорганический химический элемент, простое вещество, которое относится к лантаноидам.
Он является единственным радиоактивным элементом среди лантаноидов и считается редкоземельным металлом.
Из-за своей радиоактивности и относительно короткого периода полураспада, прометий практически не встречается в земной коре в значимых количествах.
Благодаря своей радиоактивности, прометий используется в ядерных батарейках для устройств, которым требуется длительный срок службы и низкое энергопотребление (например, в космических аппаратах), а также в других нишевых применениях.
Содержание страницы
Что такое прометий
[Promethium; по имени древнегреческого мифологического титана Прометея], Рm — радиоактивный доделать хим. элемент.
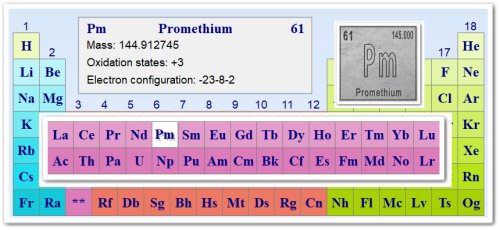
Атомный номер 61; массовое число наиболее изученного изотопа — 147 (период полураспада 2,7 года); относится к редкоземельным элементам.
Металл светло-желтого цвета. В соединениях проявляет степень окисления + 3.
Прометий выделили (1947) амер. физики Дж. Маринский, Л. Гленденин и Ч. Кориэлл из смеси радиоактивных изотопов элементов.
Которые образовались в ядерном реакторе при делении ядер урана.
Физические свойства
Кристаллическая решетка прометия двойная гексагональная плотноупакованная типа лантана, c периодами а = 3,65 ± 0,01 . А и с = 11,65 ± 0,09 А. Плотность 7,26 г/см3.
Агрегатное состояние: Твёрдое (при нормальных условиях).
Цвет: Серебристо-белый металл с металлическим блеском. На воздухе довольно быстро тускнеет, покрываясь оксидной пленкой.
Температура плавления: Приблизительно 1167,85 °C (1441 К).
Температура кипения: Около 2999,85 °C (3273 К).
Теплопроводность: Около 17.9 Вт/(м·К) (при 300 K).
Электропроводность: Является проводником электричества, как и большинство металлов. Удельная электропроводность оценивается около 1.33 × 106 См/м.
Радиоактивность: Все изотопы прометия радиоактивны. Этот фактор влияет на его свойства: он постоянно выделяет энергию в виде излучения (в основном бета-частиц), что приводит к саморазогреву образцов прометия и его соединений.
Это также означает, что с течением времени его количество уменьшается из-за распада.
Магнетизм: Является парамагнетиком.
Интересный факт: единственный из всех 15 лантаноидов (редкоземельных элементов), который не имеет ни одного стабильного изотопа.
Это означает, что весь прометий на Земле радиоактивен и постепенно распадается.
Химические свойства
По химическим свойствам прометий — типичный редкоземельный элемент.
Взаимодействуя с кислородом, образует окисел Pm2О3.
➡️ Основная степень окисления (валентность):
Прометий почти исключительно проявляет степень окисления +3 в своих соединениях. Ионы прометия в растворе имеют форму Pm3+.
➡️ Взаимодействие с неметаллами:
С кислородом (O2): Прометий, подобно другим лантаноидам, тускнеет на воздухе и медленно реагирует с кислородом при комнатной температуре, образуя оксид прометия(III).
При нагревании реакция идет энергичнее.
4Pm (s) + 3O2 (g) нагревание → 2Pm2O3 (s) (Оксид прометия(III))
➡️ С галогенами (например, хлором Cl2): Реагирует с галогенами при нагревании, образуя соответствующие тригалогениды.
2Pm (s) + 3Cl2 (g) нагревание → 2PmCl3 (s) (Хлорид прометия(III))
➡️ С водородом (H2): При нагревании образует гидрид.
2Pm (s) + 3H2 (g) нагревание → 2PmH3 (s) (Гидрид прометия(III))
➡️ Взаимодействие с водой (H2O):
Прометий медленно реагирует с холодной водой и гораздо быстрее с горячей водой или паром, образуя гидроксид прометия(III) и выделяя водород.
2Pm(s) + 6H2O (l) → 2Pm(OH)3 (aq) + 3H2 (g) (Гидроксид прометия(III))
➡️ Взаимодействие с кислотами:
Легко растворяется в разбавленных сильных неорганических кислотах, вытесняя водород и образуя соли прометия(III).
2Pm(s) + 6HCl(aq) → 2PmCl3(aq) + 3H2 (g) (Хлорид прометия(III))
2Pm(s) + 3H2SO4 (aq) → Pm2(SO4)3(aq) + 3H2 (g) (Сульфат прометия(III))
Находится в одной группе с другими элементами, но валентность прометия является ключевым свойством, отличающим его от многих других металлов.
Причина таких валентностей кроется в его атомарном строении. Чтобы увидеть это наглядно, обратите внимание на электронную формулу атома прометия.
Изотопы
Стабильные изотопы прометия в природе не обнаружены. Получены 14 радиоактивных изотопов прометий с массовыми числами от 141Рm до 154Рm.
Наиболее долгоживущий — изотоп 145Рm (период полураспада 18 лет).
Получение
Выделяют прометий из осколочного металла, получаемого при работе ядерных реакторов.
Выход изотопов 147Рm и 149Рm при делении составляет соответственно 2,6 и 1,3%.
Основной способ получения прометия — это выделение его из продуктов деления урана (или других тяжелых ядер) в ядерных реакторах.
Процесс получения включает следующие этапы:
Ядерное деление: Внутри ядерного реактора, при делении атомов урана-235 (или плутония-239) под действием нейтронов.
Образуется широкий спектр более легких атомных ядер, которые называются продуктами деления.
Среди этих продуктов и находится прометий.
Накопление: В отработанном ядерном топливе после длительной работы реактора накапливаются различные изотопы прометия.
Химическое выделение и очистка: Это наиболее сложный этап.
Отработанное топливо подвергается химической переработке.
Прометий отделяется от других продуктов деления, а также от урана и плутония.
Это очень трудоемкий процесс, так как прометий химически очень похож на другие лантаноиды (например, самарий и неодим), которые также присутствуют в продуктах деления.
Для их разделения обычно используются методы ионного обмена или экстракции растворителями.
Эти методы позволяют эффективно разделить элементы с очень близкими химическими свойствами, используя небольшие различия в их размерах и склонности к образованию комплексов.
Выделение чистого прометия: После многократных циклов разделения получают чистые соединения прометия, которые затем могут быть восстановлены до металлического прометия.
Применение
На основе изотопа 147Рm созданы миниатюрные атомные батареи с мягким излучением, к-рые используются без спец. защиты.
Батареи не чувствительны к изменению т-ры, давления и др. внешних условий.
Перспективно их применение в часах, радиоэлектронных и авиационных приборах, слуховых аппаратах, космических кораблях и др.
Ядерные батарейки (радиоизотопные термоэлектрические генераторы, РИТЭГи):
Принцип: Прометий-147 испускает бета-частицы (электроны) при радиоактивном распаде.
Энергия этих частиц может быть преобразована в электрическую с помощью полупроводниковых преобразователей (термоэлектрические элементы).
Преимущества: Отсутствие жесткого гамма-излучения у
147Pm делает его относительно безопасным для использования в небольших устройствах по сравнению с другими радиоизотопами.
Период полураспада (около 2.6 лет для 147Pm) достаточно долог для длительной работы, но достаточно короток, чтобы генерировать заметную мощность.
Применение: Использовались в компактных источниках питания для космических аппаратов, некоторых видов кардиостимуляторов (исторически, сейчас реже).
Удаленных метеостанций, океанских буев и других устройств, требующих надежного и долгосрочного источника энергии без обслуживания.
Светящиеся краски и люминесцентные источники света:
Принцип: Бета-частицы, испускаемые прометием-147, возбуждают люминофор (например, сульфид цинка), заставляя его светиться.
Применение: Ранее использовался в светящихся циферблатах часов, шкалах приборов, различных индикаторах и знаках, не требующих внешнего источника энергии.
Современное состояние: Использование прометия в люминесцентных красках значительно сократилось из-за соображений безопасности (потенциального контакта с радиоактивным материалом).
И появления более безопасных альтернатив (например, тритий или фотолюминесцентные материалы).
Измерительные приборы (источники бета-излучения):
Принцип: Стабильное бета-излучение прометия может использоваться для измерения толщины материалов.
Чем толще материал, тем меньше бета-частиц проходит через него.
Применение: В промышленных толщиномерах для контроля толщины тонких листов бумаги, пластика, металлической фольги и покрытий.
Также применяется в некоторых научных приборах как калибровочный источник бета-излучения.
Научные исследования:
Используется в химических и физических исследованиях как меченый атом (радиоактивный индикатор) для изучения механизмов реакций и процессов.
Применяется для исследования свойств редких земель и актинидов.
Литература
Филянд М. А., Семенова Е. И. Свойства редких элементов (Справочник).
Часто задаваемые вопросы
Опасен для человека из-за своей радиоактивности.
Излучение: Он является источником бета-излучения.
Вред: Бета-частицы могут вызывать ожоги кожи при внешнем облучении.
Основная опасность: При попадании внутрь организма (через дыхание, пищу, раны) прометий становится чрезвычайно опасным.
Так как вызывает внутреннее облучение тканей и органов, что может привести к поражению клеток, развитию онкологических заболеваний и другим серьезным проблемам со здоровьем.
Будучи радиоактивным элементом и продуктом деления урана, представляет опасность для окружающей среды главным образом из-за своего ионизирующего излучения (бета-частиц).
Основные угрозы:
1. Радиоактивное загрязнение.
2. Биологическое воздействие.
3. Долгосрочное воздействие.
Практически не встречается в природе в значимых количествах.
Но его можно найти в отработанном ядерном топливе.
А также в очень старых урановых рудах, где он образуется в результате самопроизвольного деления урана

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.