Селен это химический элемент, простое вещество, микроэлемент, открыт в 1817 году шведским минералогом Йенсом Якобом Берцелиусом.
Легко соединяется почти со всеми металлами. Концентрированная селеновая кислота H2SeО4 растворяем золото.
Содержание страницы
- 1. Что такое селен
- 2. Физические свойства селена
- 3. Изотопы
- 4. Химические свойства селена
- 5. Минералы селена
- 6. Аллотропные модификации
- 7. Электропроводность
- 8. Соединения селена с веществами
- 9. Получение селена
- 10. Селен высокой чистоты
- 11. Применение
- 12. Токсичность
- 13. Характеристика элемента
- 14. Свойства простых веществ и соединений
- 15. Часто задаваемые вопросы ответы о селене?
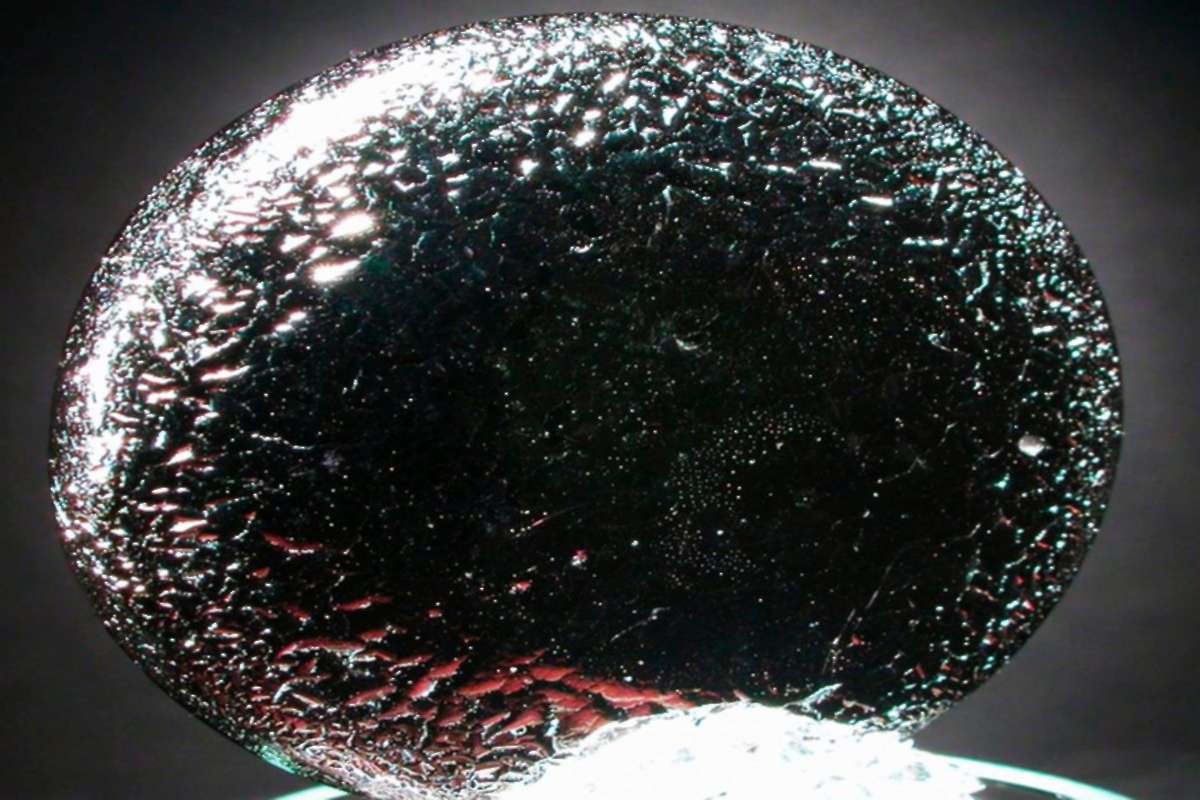
Что такое селен
(Selenium; от греческого — луна), Se — химический элемент 16 группы (устаревший VI группы) периодической системы элементов.
Атомный номер 34, атомная масса 78,96. В соединениях проявляет степени окисления -2, +4 и +6.
В природе распространен меньше серы и сопутствует ей в сернистых рудах, из которых его добывают, как побочный продукты при производстве серной кислоты.
Физические свойства селена
Теплота плавления селена 16,5 кал/г; теплота испарения 221,5 кал/г. Термический коэффициент линейного расширения 4,927 х 10-5 град-1.
Коэффициент теплопроводности (т-ра 28° С) 5,66 х 10-4 кал/см х сек х град] удельная теплоемкость (т-ра 25° С) 0,0767 кал/г х град.
Отличается диамагнитными свойствами, типичный дырочный полупроводник.
Ширина запрещенной зоны (оптическая) — 1,8 эв, подвижность носителей тока менее 1 см2/в х сек (т-ра 20° С).
Чистый селен по величине удельного электрического сопротивления (до 10 12 ом х см) при т-ре 20° С в темноте близок к изоляторам свету электропроводность возрастает в 1000 раз.
Аналогично действие рентгеновского излучения и радиации.
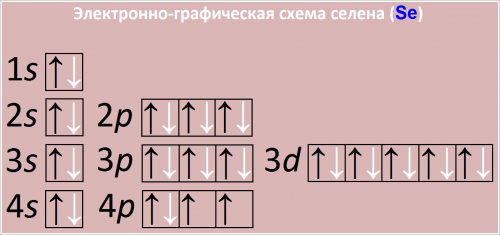
Полная электронная формула атома селена в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p4
Сокращенная электронная конфигурация Se:
[Ar] 3d10 4s2 4p4
Изотопы
Природный селен состоит из стабильных изотопов 74Se (0,98%), 76Se (9,02%), 77Sе (7,58%), 78Se (23,52%), 80Se (49,82%) u 82Se (9,19%).
Известно 11 радиоактивных изотопов. Впервые селен обнаружил (1817) швед, химик П. Я. Берцелнус в отходах сернокислотного произ-ва.
Промышленное производство началось в начале 20 в.
Селен относится к рассеянным элементам,его содержание в земной коре 8 х 10-5%.
Будучи аналогом и пост, спутником серы, содержится в небольших количествах в сульфидных минералах меди, цинка и свинца.
Химические свойства селена
При горении селен на воздухе образуется двуокись SeО2 — белое кристаллическое вещество, летучее (т-ра возгонки 317° С).
Легко растворяется в воде с образованием селенистой кислоты H2SeО3.
Высший окисел — трехокись SeО3 — получают только косвенно. Легко соединяется с металлами, образуя селениды.
При нагревании с водородом (оптимальная т-ра 500° С) или действием разбавленных к-т на селениды (например Al2Se3) получают селеноводород.
Селеноводород H2Se — бесцветный газ с очень неприятным запахом, еще более ядовитый, чем сероводород H2S.
Селено-водород растворяется в воде, образуя селеноводородную к-ту, более сильную, чем сероводородная.
Селеноводород — сильный восстановитель.
Его растворы очень нестойки и при наличии кислорода легко разлагаются с выделением красной модификации селена.
Растворением в азотной к-те получают слабую селенистую к-ту, соли которой (селениты) нерастворимы в воде (исключая соли щелочных металлов).
При действии окислителей (например перекиси водорода) селенистая к-та H2SeО3 превращается в селеновую к-ту H2SeО4.
Селеновая к-та и ее соли (селенаты) по св-вам напоминают серную к-ту и ее соли (сульфаты).
Минералы селена
Редкие собственные минералы представляют собой гл. обр. селениды — науманнит Ag2Se, тиеманит HgSe и берцелианит Cu2Se.
Практического значения селеновые минералы не имеют.
Аллотропные модификации
Подобно сере селен образует несколько аллотропных модификаций, включая стекловидную и аморфные:
- Красную.
- Коричневую.
- Черную.
- Коллоидную.
Кристаллический селен встречается в трех модификациях:
- Альфа-моноклинный.
- Бета-моноклинный.
- Гамма-гексагональный.
Термодинамически стабильной при нормальных условиях модификацией является гексагональный — темно-серое с коричневым оттенком вещество с периодами решетки а = 4,3544 А, с = 4,9496 А и плотностью 4,80 г/см3.
Все другие модификации превращаются в гексагональный при нагревании (т-ра 180 — 220° С),
Стекловидный — высокополимерное вещество темного цвета, представляющее собой смесь кольцеобразных молекул Se8 и многозвенных цепочек, содержащих до 1000 атомов селена.
Плотность стекловидного селена 4,28 г/см3, его получают при быстром охлаждении расплавленного С.; tпл 219° С; tкил 685° С.
Пары желтоватого цвета; при т-ре ниже 900° С состоят из молекул, содержащих от восьми до двух атомов.
Выше т-ры 900— 10009 С пары состоят из молекул Se2, и только при т-ре более 1500° идет диссоциация на атомы.
Электропроводность
Электропроводность зависит от температуры, структуры и чистоты образцов. В жидком состоянии сохраняет полупроводниковые свойства.
Небольшие добавки некоторых элементов (например йода) увеличивают проводимость.
Добавка ртути ведет себя как донор и увеличивает электрическое сопротивление и термоэдс без превращения его в полупроводник n-типа.
Обладает высокой термоэдс (600 мкв/град при комнатной т-ре).
Твердость Селен по Моосу — 2,0; НВ = 75; модуль норм, упругости 5500 кгс/мм2; модуль сдвига 660 кгс/мм2.
По химическому поведению — типичный неметалл. При обычной т-ре не окисляется на воздухе, кислород и вода на него также не действуют.
Устойчив к действию соляной и разбавленной серной к-т. В щелочах медленно растворяется с образованием селенитов и селенидов.
Соединения селена с веществами
Некоторые соединения, образованные селеном , следует рассматривать как стремление дополнить свою оболочку до электронной конфигурации благородного газа.
Так образуются халькогениды Se²—, хотя существование таких ионов (кроме соединений с наиболее электро положительными элементами маловероятно.
Кроме этого состояния — 2 он может находиться в степенях окисления +4 и +6.
Подобно серной, селеновая кислота очень гигроскопична, обугливает органические вещества, концентрированная селеновая к-та растворяет золото.
При обычной т-ре реагирует только с фтором, при небольшом нагревании — с хлором и бромом, образуя галогениды SeFe (только фторид), SeF4 и Se2F2 (хлорид и бромид), к-рые по общему характеру похожи на соответствующие производные серы.
Устойчивые йодиды селена не получены. Известны соединения с азотом — азотистый (Se4N4), с фосфором — селенистый фосфор (P4Se3) и др.
Получение селена
Из медных электролитных шламов селен извлекают либо окислительным обжигом с отгонкой SeО2, либо нагреванием с концентрированной серной к-той с последующей отгонкой двуокиси селена.
Применяют также метод окислительного спекания шлама с содой, в результате к-рого образуются селениты и селена-ты.
Спек выщелачивают водой, отделяют двуокись теллура, а затем выделяют элементарный С. восстановлением сернистым газом.
Технический содержит 97,5—99% Se.
Для использования в полупроводниковой технике его подвергают очистке дистилляцией в вакууме или сульфитно-циклическим методом.
Добывают при комплексной переработке рудного сырья (сульфидных медных и медноникелевых руд). В значительных количествах его извлекают из шламов сернокислотных произ-в.
При обжиге селен-содержащих пиритов возгоняется двуокись SeО2, которую восстанавливают сернистым газом до элементарного состояния.
Селен высокой чистоты
С высокой чистоты содержит не более 1 х 10-5% примесей. Окислительно-восстановительный метод дает возможность получить металл чистотой 99%.
Зонной плавкой можно повысить содержание до 99,9999%.
Наиболее чистый селен получают термической диссоциацией селеноводорода.
Технический выпускают в виде порошка, плавленный — в виде слитков массой 5 — 10 кг. Se и его соединения — токсичные вещества.
Элементарный менее ядовит, чем его соединения, среди которых наиболее токсична двуокись селена; предельно допустимая ее концентрация 0,0003 мг/л.
Применение
Производство и применение связаны с герметизацией аппаратуры, сильной вытяжкой и наличием очистных фильтров для выбросов воздуха в атмосферу.
Наибольшее применение селена находит в полупроводниковой технике — для изготовления выпрямителей и фотоэлементов.
Применяют также для синтеза селенидов, как краситель в стекольной пром-сти. для вулканизации резины, как модификатор для создания мелкозернистой структуры стали.
Se и некоторые селениды служат катализаторами в процессах гидрогенизации и дегидрогенизации органических соединений.
В качестве добавок к свинцовым сплавам, повышающих механические свойства и твердость.
Токсичность
Его соединения ядовиты. Отравления напоминают отравление мышьяком, но сопровождаются более тяжелыми последствиями.
Возможно, что это связано со способностью Se замещать серу в органических соединениях.
Характеристика элемента
Селен в главных подгруппах VIA и VIIА (устаревшая классификация) сосредоточены элементы, электронная структура внешнего электронного слоя которых весьма близка к конфигурациям завершающих периоды благородных элементов (инертных газов).
Члены этих подгрупп ярко проявляют свой неметаллический характер, за исключением полония и астата.
В соединениях с типичными металлами он образует ионные связи, а с неметаллами —ковалентные полярные.
Понятие степень окисления в большинстве случаев имеет для членов подгруппы VIA формальное значение.
Свойства простых веществ и соединений
Селен существует во многих аллотропических видоизменениях. Стекловидный селен, образующийся при быстром охлаждении его расплава, не проводит тока, а кристаллический серый селен, получающийся при медленном охлаждении, полупроводник.
При комнатной температуре Se устойчив к воздуху и кислороду. С галогенами взаимодействуют на холоду, а с йодом — в присутствии влаги.
Селен с водой и разбавленными кислотами не реагирует, но медленно растворяется в щелочи и хорошо в концентрированной азотной кислоте и «царской водке»:
Se + 2HNO3 = H2SeO4 + 2NO
При нагревании на воздухе селен образует соответственно SeО2 — твердое, возгоняющиеся при нагревании вещество.
В отличие от SО2 они служат окислителями, легко восстанавливается до свободного Se.
В воде SeО2 легко растворим и образует селенистую кислоту H2SeО3, проявляющую окислительные свойства, однако при действии сильных окислителей селенистая кислота переходит в селеновую.
Она напоминает по свойствам серную кислоту, но является более сильным окислителем.
Селен образуют H2Se, легко разлагающиеся эндотермические соединения, растворение которых в воде приводит к образованию более сильных кислот, чем сероводородная.
H2Se — сильные восстановители.
Часто задаваемые вопросы ответы о селене?
Что такое силен?
Селен — химический элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), 4-го периода в периодической системе.
Какие степени окисления у селена?
Селен — аналог серы и проявляет степени окисления −2 (H2Se), +4 (SeO2) и +6 (H2SeO4).
Однако, в отличие от серы, соединения селена в степени окисления +6 — сильнейшие окислители, а соединения селена (−2) — гораздо более сильные восстановители, чем соответствующие соединения серы.
Где селен в таблице Менделеева?
Селен — химический элемент с атомным номером 34. Принадлежит к 16-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VI группы, или к группе VIA), находится в четвёртом периоде таблицы.
Зачем нужен селен?
Селен может быть полезен в борьбе с инфекционными заболеваниями и вирусными инфекциями.
Селен участвует в поддержании правильной функции щитовидной железы.
Щитовидная железа содержит больше селена на грамм ткани, чем любой другой орган в организме, и может экспрессировать специфические селенопротеины.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.