Теория
Углерод (C) — ключевой химический элемент 14‑й группы, располагающийся во 2‑м периоде. Он является основой всей органической жизни и обладает уникальной способностью образовывать длинные цепи и циклы.
В отличие от бора, углерод проявляет гораздо более широкий спектр состояний.
Его степени окисления варьируются от −4 до +4, что позволяет ему выступать как в роли мощного восстановителя, так и окислителя.
Атомы углерода образуют прочные ковалентные связи. Благодаря средней электроотрицательности, углерод может как притягивать электронную плотность от металлов и водорода, так и отдавать её более активным неметаллам (кислороду, фтору).
Его электронная конфигурация 1s2 2s2 2p2 определяет его химическое поведение:
- Наличие четырех валентных электронов позволяет образовывать четыре химические связи (состояние +4);
- Способность к гибридизации (sp, sp2, sp3) объясняет разнообразие геометрии его молекул и соединений.
Отсутствие d-подуровня во втором периоде ограничивает максимальную валентность углерода числом 4, однако этого достаточно для создания миллионов уникальных веществ.
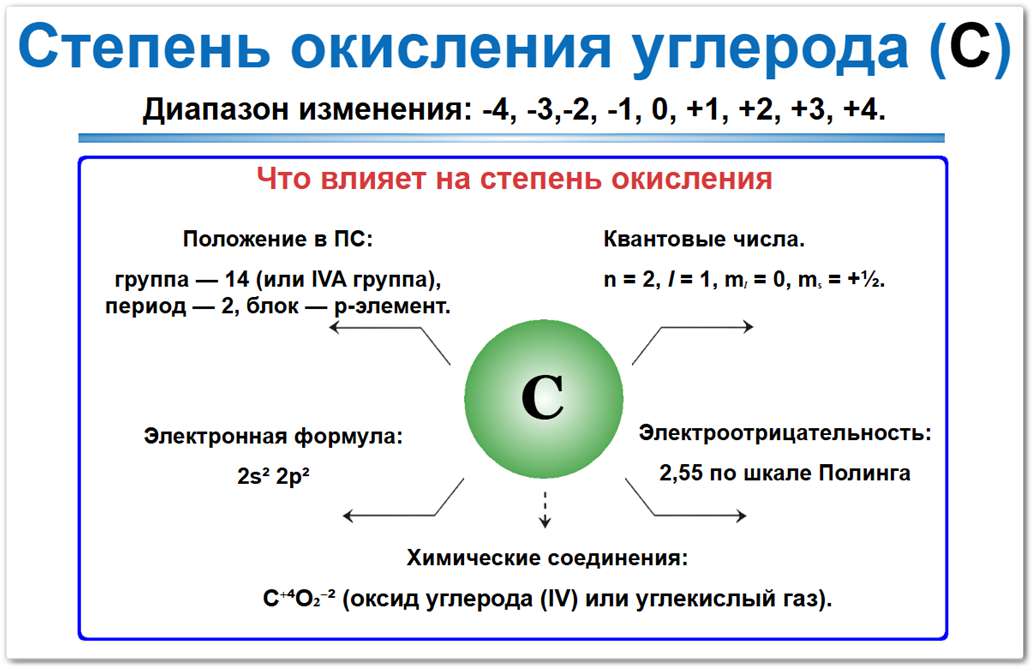
Рис. Диапазон степени окисления углерода от −4 до +4. На распределение электронов влияют положение элемента в 14-й группе ПС, значение электроотрицательности (2,55) и тип химической связи в соединениях.
Содержание страницы
Как определить степень окисления углерода
Определение степени окисления углерода (C) может быть сложнее, чем у бора, из-за обилия органических соединений, где атомы углерода могут иметь разные заряды в одной молекуле.
Чтобы правильно определить заряд, необходимо опираться на пять факторов:
- По таблице Менделеева (границы группы).
- По валентности (число связей).
- По химическому соединению (алгебраический расчет).
- По электронной конфигурации (возбужденное состояние).
- По электроотрицательности (сравнение с партнерами).
По таблице Менделеева (границы)
- Высшая степень окисления: равна номеру группы (4) — +4. Характерна для углекислого газа и карбонатов.
- Низшая степень окисления: (4 − 8) = −4. Проявляется в метане и карбидах металлов.
По валентности (число связей)
Валентность углерода почти во всех стабильных соединениях равна IV. Однако степень окисления при этом может быть разной:
- В метане (CH4) валентность IV, а степень окисления −4.
- В углекислом газе (CO2) валентность IV, а степень окисления +4.
По химическому соединению (расчёт через X)
Метод суммы зарядов (сумма всегда равна 0).
- Возьмем глюкозу C6H12O6. Водород (+1), кислород (−2).
- Уравнение: 6x + (12 · 1) + (6 · −2) = 0 → 6x + 12 − 12 = 0 → x = 0.
- Средняя степень окисления углерода в глюкозе равна 0.
По конфигурации (валентные электроны)
Внешний слой углерода — 2s2 2p2.
По электроотрицательности
Значение ЭО углерода — 2.55.
— В паре с водородом (ЭО 2.2) углерод — отрицателен.
— В паре с кислородом (ЭО 3.44) углерод — положителен.
| Степень | Химическая роль | Примеры соединений |
|---|---|---|
| −4 | Окислитель (в метанидах) | CH4, Al4C3 |
| +2 | Восстановитель | CO (угарный газ), CHCl2 |
| +4 | Высшая степень окисления | CO2, H2CO3, CCl4 |
Пример решения, задача:
▶️ Дано:
Химическое соединение: CaCO3 (Мрамор / Кальцит).
⌕ Найти:
Определите степень окисления углерода.
✨ Решение:
Кальций (Ca) — металл II группы, СО = +2. Кислород (O) = −2.
Уравнение: (+2) + x + (3 · −2) = 0 → 2 + x − 6 = 0 → x = +4.
✅ Ответ:
Степень окисления углерода в CaCO3 равна +4.
Часто задаваемые вопросы
Основные значения: −4, 0, +2 и +4. В органической химии встречаются и промежуточные значения (например, −1, −2, −3) в зависимости от окружения атома.
Нужно из суммы зарядов известных элементов (O = −2, H = +1) вычислить остаток, необходимый для обнуления молекулы.
Номер группы обычно указывает на максимально возможный положительный заряд.
Да, в сложных органических молекулах расчетная (средняя) степень окисления может быть дробной, хотя каждый отдельный атом всегда имеет целое число электронов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.