Теория
Азот (N) — химический элемент 15‑й группы, располагающийся во 2‑м периоде, один из самых распространенных неметаллов на Земле.
В отличие от бора, азот обладает высокой электроотрицательностью и способен проявлять чрезвычайно широкий диапазон степеней окисления — от −3 до +5.
Атомам азота свойственна способность образовывать кратные связи (как в молекуле N2), а также выступать в роли донора электронной пары за счет наличия неподеленной пары электронов на внешнем слое.
Нахождение азота во 2‑м периоде, как и у бора, исключает наличие d-подуровня, что ограничивает его максимальную валентность числом 4, хотя степень окисления может достигать +5.
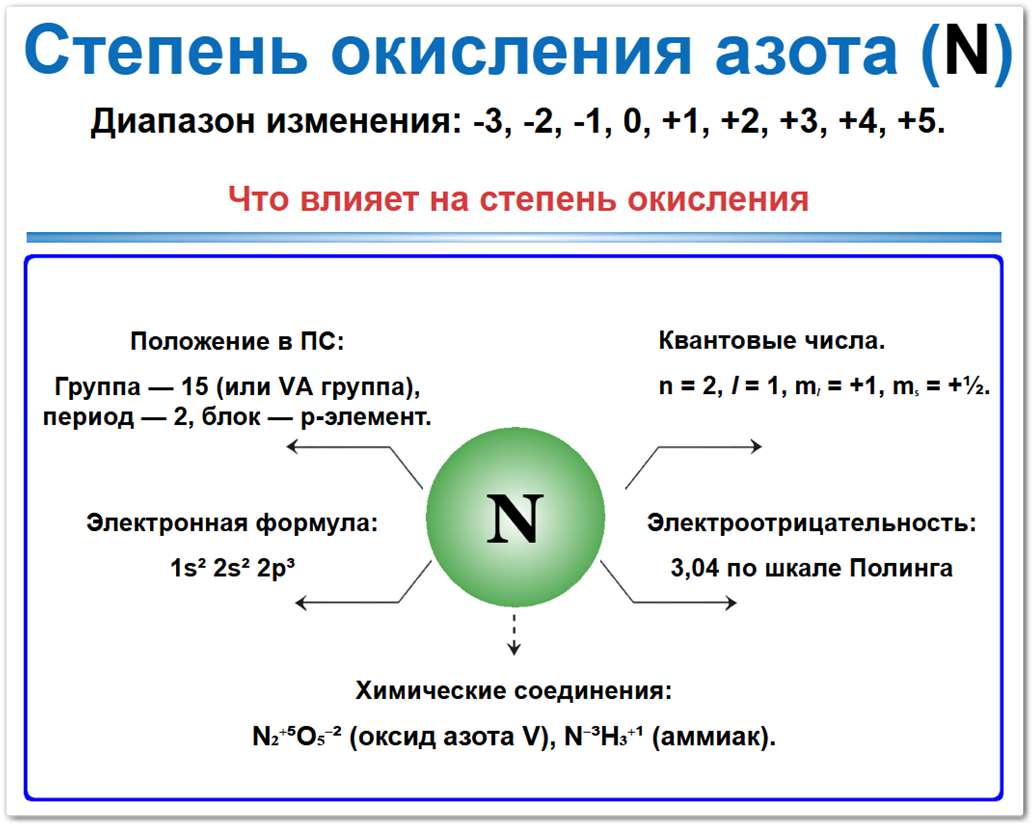
Рис. Спектр степеней окисления азота. Благодаря наличию трех неспаренных электронов на p-подуровне, азот легко образует соединения в самых разных окислительных состояниях.
Содержание страницы
- 1. Как определить степень окисления азота
- 1.1. По таблице Менделеева (границы)
- 1.2. По химическому соединению (расчёт через X)
- 1.3. По электроотрицательности
- 1.4. По электронной формуле
- 1.5. По валентности
- 1.6. Квантовые числа
- 1.7. Сводная таблица степеней окисления азота
- 2. Пример решения, задача:
- 3. Проверка знаний: Как определить Азот по таблице Менделеева
- 4. Часто задаваемые вопросы
Как определить степень окисления азота
Азот — «чемпион» по количеству степеней окисления. Его заряд в соединении зависит от того, насколько сильно партнер по связи притягивает или отдает электроны.
Чтобы правильно определить степень окисления азота, учитывайте пять факторов:
- По таблице Менделеева (границы группы).
- По валентности (структурные формулы).
- По химическому соединению (алгебраический расчет).
- По конфигурации (заполнение внешнего слоя).
- По электроотрицательности (сравнение с партнером).
По таблице Менделеева (границы)
- Высшая степень окисления: равна номеру группы (5) — +5.
- Низшая степень окисления: номер группы минус 8 — −3.
Азот возглавляет главную подгруппу V группы (подгруппу азота).
Как типичный p-элемент этой подгруппы, он имеет 5 валентных электронов, что определяет диапазон его степеней окисления от −3 до +5.
По химическому соединению (расчёт через X)
- Возьмем азотную кислоту HNO3. У H всегда +1, у O всегда −2.
- Уравнение: (+1) + x + (3 · −2) = 0 → 1 + x − 6 = 0 → x = +5.
По электроотрицательности
ЭО азота (3,04) выше, чем у большинства элементов, но ниже, чем у кислорода (3,44) и фтора (3,98).
- Отрицательная СО: в соединениях с водородом и металлами (NH3, Li3N).
- Положительная СО: в соединениях с кислородом и фтором (NO2, NF3).
По электронной формуле
Чтобы определить степень окисления азота по электронной формуле, нужно проанализировать распределение электронов на его внешнем энергетическом уровне.
Электронная конфигурация азота (N): 1s2 2s2 2p3.
Внешний уровень (второй) содержит 5 электронов. Именно они определяют возможные значения степени окисления:
Минимальная (отрицательная) СО: −3.
- На p-подуровне у азота есть 3 неспаренных электрона. Чтобы полностью заполнить внешний уровень до устойчивого состояния (октета), атому необходимо принять 3 электрона. Это происходит при взаимодействии с металлами (нитриды) или водородом (аммиак).
Пример: В NH3 азот забирает электронную плотность у трех атомов водорода.
Промежуточные и высшая (положительные) СО: от +1 до +5.
- При взаимодействии с более электроотрицательными элементами (кислород, фтор) азот начинает отдавать (смещать) свои электроны:
- Сначала смещаются 3 неспаренных p-электрона (СО +1, +2, +3).
- Затем в процесс вступают 2 спаренных s-электрона (СО +4, +5).
Пример: В азотной кислоте (HNO3) азот задействует все 5 валентных электронов, достигая высшей степени окисления +5.
Важный нюанс: Несмотря на то, что азот может отдать 5 электронов (СО +5), его валентность во втором периоде ограничена числом 4, так как у него всего 4 орбитали (одна s и три p) и нет свободных d-орбиталей для «распаривания» электронов.
По валентности
Валентность азота часто не совпадает с его степенью окисления.
Это связано с тем, что валентность определяется числом общих электронных пар (связей), а степень окисления — условным зарядом.
- Валентность III: Проявляется в аммиаке (NH₃). Здесь азот образует 3 связи с водородом и имеет одну неподеленную пару электронов. СО при этом равна −3.
- Валентность IV: Максимальная валентность азота. Она достигается в ионе аммония (NH4+) или азотной кислоте (HNO3). Четвертая связь образуется по донорно-акцепторному механизму.
Важно: Валентность азота никогда не равна V, так как у него всего 4 орбитали на внешнем уровне, на которых можно разместить электроны. При этом степень окисления +5 в нитратах — обычное явление.
Квантовые числа
Электронное строение азота объясняет его «химическую гибкость».
Последний электрон азота описывается набором квантовых чисел: n=2, l=1, mₗ=+1, mₛ=+½.
Как это влияет на заряд атома:
- Главное квантовое число (n=2): Показывает, что у азота всего два энергетических уровня. Отсутствие d-подуровня (который появляется только с n=3) не дает азоту «распаривать» электроны, что ограничивает количество связей, но не мешает отдавать электронную плотность до СО +5.
- Орбитальное число (l=1): Указывает на p-подуровень. У азота там находятся три неспаренных электрона (2p3).
- Принцип Хунда (распределение): Три электрона сидят в отдельных ячейках (px1, py1, pz1). Это позволяет азоту легко принимать 3 электрона до полного заполнения (СО −3) или поочередно отдавать их в реакциях с кислородом, создавая цепочку положительных СО: +1, +2, +3.
- Магнитное и спиновое числа: Подтверждают наличие стабильной полузаполненной оболочки, что делает молекулу N2 крайне прочной, а сам азот в свободном состоянии — инертным (СО 0).
|
СО |
Класс соединений |
Примеры |
|---|---|---|
|
−3 |
Аммиак, нитриды |
NH3, Mg3N2 |
|
0 |
Простое вещество |
N2 |
|
+1 |
Веселящий газ |
N2O |
|
+2 |
Оксид азота (II) |
NO |
|
+3 |
Азотистая кислота |
HNO2 |
|
+4 |
«Лисий хвост» |
NO2 |
|
+5 |
Азотная кислота |
HNO3, N2O5 |
Пример решения, задача:
▶️ Дано:
Соединение: NH4NO3 (Аммиачная селитра).
⌕ Найти:
Определите степени окисления двух атомов азота в этой соли.
✨ Решение:
Это ионное соединение, состоящее из ионов NH₄⁺ и NO₃⁻.
1) В NH4+: x + (4 · 1) = +1 → x = −3.
2) В NO3—: x + (3 · −2) = −1 → x = +5.
✅ Ответ:
Азот в одной молекуле имеет две разные СО: −3 и +5.
Проверка знаний: Как определить Азот по таблице Менделеева
Отметьте три правильных утверждения, которые однозначно определяют Азот (N) в Периодической системе.
По каким признакам можно безошибочно установить, что речь идёт именно об Азоте?
Показать верные ответы и пояснения
Правильные ответы: 1, 3, 4
- 1) В атомном ядре содержится ровно 7 протонов.
Это фундаментальный признак: порядковый номер (Z=7) уникален для азота и определяет все его свойства. - 3) Находится во 2-м периоде и 15-й группе (V A).
Это точное положение в таблице Менделеева характерно только для азота и указывает на:- Два электронных слоя (период 2);
- Пять валентных электронов (группа 15);
- Принадлежность к p-блоку.
- 4) Полный набор электронов описывается формулой: 1s2 2s2 2p3.
— Общее число электронов (7) равно числу протонов (Z=7).
— Распределение по уровням соответствует положению во 2-м периоде и 15-й группе (2 + 5 = 7 электронов). - 2) Является бесцветным газом атмосферы.
Это физическое свойство вещества, а не признак химического элемента в таблице. Кроме того, газы в атмосфере могут быть разными (аргон, неон), хотя азота больше всего. - 5) Находится во 2-м периоде и имеет две электронные оболочки.
Верно, но не уникально. Эту характеристику разделяют все элементы от лития (Li) до неона (Ne). - 6) Проявляет высшую степень окисления +5.
Хотя это верное свойство, оно не является «паспортом» элемента. Степень окисления +5 также проявляют фосфор (P), мышьяк (As) и другие элементы 15-й группы.
Часто задаваемые вопросы
Да, это его высшая степень окисления, она проявляется в азотной кислоте (HNO3) и ее солях — нитратах.
Наиболее химически инертна степень 0 (молекулярный азот N2), а наиболее распространенные в химии — −3 и +5.
Валентность азота никогда не превышает 4 из-за отсутствия d-орбиталей, в то время как степень окисления может быть +5.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.