Теория:
Степень окисления резерфордия (Rf) в химических соединениях проявляет единственно стабильную степень окисления +4.
Это обусловлено положением элемента в 4-й группе Периодической системы, где высшая степень окисления соответствует номеру группы и конфигурации валентных электронов.
Кроме того, выделяют показатель 0, который относится к резерфордию в виде простого вещества (тяжелый радиоактивный металл).
Например для наиболее стабильной СО +4: в соединении RfCl4 (хлорид резерфордия IV) или RfO2 (оксид резерфордия IV) заряд иона равен +4. В этом состоянии резерфордий является аналогом гафния (Hf) и циркония (Zr).
Для сравнения, другие СО: попытки обнаружить другие степени окисления на текущем уровне развития экспериментальной техники пока не привели к однозначным результатам, так как +4 является наиболее энергетически выгодной.
- Почему +4? Электронная формула резерфордия [Rn] 5f14 6d2 7s2 предполагает легкую отдачу четырех внешних электронов, что приводит к формированию устойчивой электронной конфигурации иона.
- Почему другие СО менее вероятны? Резерфордий — это тяжелый трансактиноид, для которого 4-валентное состояние наиболее полно соответствует химическому поведению группы титана, к которой он формально относится.
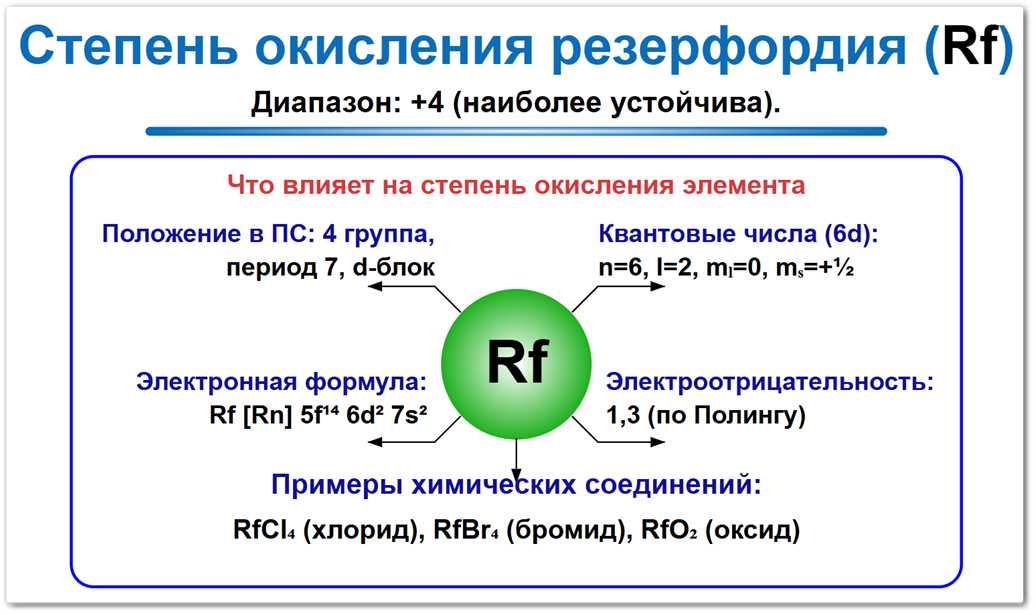
Рис. 1. Основная степень окисления резерфордия: 0 и +4.
Состояние +4 является наиболее устойчивым и единственным надежно зафиксированным в экспериментах по газофазной химии хлоридов.
Важно заметить, что резерфордий — крайне радиоактивный элемент, синтезируемый в ядерных реакторах или на ускорителях.
Его химия изучается методами «химии одного атома», что накладывает огромные ограничения на точность.
На свойства этого элемента сильно влияют релятивистские эффекты, которые делают его поведение несколько отличным от поведения более легких аналогов — гафния и циркония.
Содержание страницы
- 1. Почему +4 — самая устойчивая степень окисления у резерфордия
- 2. Степень окисления резерфордия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему резерфордий предпочитает заряд +4?
- 4. 4 способа определить степень окисления резерфордия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления резерфордия
- 6. Шпаргалка
- 7. Резерфордий вне учебника: что скрывает наука?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +4 — самая устойчивая степень окисления у резерфордия
Стабильность определяется заполнением внешних оболочек и соответствием электронной структуре 4-й группы.
- В простом веществе (Rf0): Заряд равен 0. Конфигурация:
[Rn] 5f14 6d2 7s2. - В четырехвалентном ионе (Rf+4): Резерфордий теряет 4 валентных электрона. Конфигурация:
[Rn] 5f14(стабильный инертный остов).

Рис. 2. Схема образования степени окисления +4: удаление 6d и 7s электронов.
Степень окисления резерфордия в соединениях
- Хлорид резерфордия(IV) (RfCl4): Rf +4.
- Бромид резерфордия(IV) (RfBr4): Rf +4.
Высшая степень окисления
Высшая степень окисления Rf равна +4.
Низшая степень окисления
Характерна степень окисления 0 в металлическом состоянии.
Промежуточные степени окисления
На данный момент нет достоверных данных о существовании других стабильных СО.
Важно: Резерфордий — первый из «трансактиноидов», и его изучение является ключевым для понимания периодичности химических свойств в сверхтяжелой области.
Почему резерфордий предпочитает заряд +4?
- Групповая принадлежность: Подобно титану, цирконию и гафнию, он стремится к 4-валентному состоянию.
- Электронная конфигурация: Потеря 4 электронов доводит его до конфигурации [Rn]5f14.
4 способа определить степень окисления резерфордия
По таблице Менделеева
- Семейство: Трансактиноиды (d-элементы).
- Валентные электроны: 4.
- Атомная масса: ~267 а.е.м.
По валентности (Число связей)
Валентность резерфордия (Rf) в большинстве химических соединений стабильно равна IV.
Будучи аналогом гафния и циркония, он проявляет ярко выраженную способность образовывать четыре связи с атомами других элементов.
Детальные примеры:
- В RfCl4 (тетрахлорид резерфордия): Атом Rf окружен четырьмя атомами хлора, образуя тетраэдрическую структуру. Это классический пример высшей валентности элемента.
- В RfF4 (тетрафторид резерфордия): Резерфордий образует четыре прочные связи с наиболее электроотрицательным фтором. Эти соединения крайне важны для изучения летучести трансактиноидов.
- В комплексных ионах [RfCl6]2-: Здесь резерфордий проявляет координационное число 6, что косвенно подтверждает его валентное состояние +4 и способность расширять координационную сферу.
По электронной конфигурации
Электронная формула резерфордия: [Rn] 5f14 6d2 7s2.
Как происходит ионизация:
- Валентные электроны: Резерфордий имеет 4 электрона на внешних и предвнешних уровнях (два 6d-электрона и два 7s-электрона).
- Механизм потери: Для достижения состояния +4 атом резерфордия отдает все 4 валентных электрона.
- Энергетический итог: При потере этих электронов резерфордий переходит в стабильное состояние с «пустыми» внешними оболочками над остовом 5f14. Это энергетически наиболее предпочтительный сценарий для элементов 4-й группы ПСХЭ.
- Результат: Конфигурация
[Rn] 5f14делает ион Rf4+ классическим «изоэлектронным» аналогом ионов циркония (Zr4+) и гафния (Hf4+).
По химическому соединению (Алгебраический расчет)
Для определения степени окисления используется правило электронейтральности молекулы: сумма всех степеней окисления в соединении всегда равна 0.
Пример для RfCl4:
- 1. Хлор (Cl) в большинстве бинарных соединений имеет степень окисления -1.
- 2. В молекуле RfCl4 содержится 4 атома хлора, следовательно, их суммарный заряд: 4 · (-1) = -4.
- 3. Обозначим степень окисления резерфордия за x. Составляем уравнение: x + (-4) = 0.
- 4. Решаем уравнение: x = +4.
✅ Вывод: Степень окисления резерфордия в данном соединении равна +4.
Примеры степеней окисления резерфордия
| СО | Характеристика | Примеры |
|---|---|---|
| +4 | Наиболее стабильная. | RfCl4 |
Шпаргалка
- +4 — доминирующая СО.
- Аналог гафния — химическое поведение очень близко к элементам 4-й группы.
Резерфордий вне учебника: что скрывает наука?
Аномальное поведение в растворах:
Резерфордий — это первый трансактиноид, химия которого начала серьезно изучаться в растворах.
Ученые обнаружили, что в растворах соляной кислоты он ведет себя не совсем как классический «тяжелый аналог» циркония или гафния.
Из-за мощных релятивистских эффектов орбитали резерфордия деформируются, что меняет прочность его связей с лигандами.
Сверхтяжелые комплексные соединения:
В отличие от гафния, резерфордий способен образовывать комплексные анионы с хлорид-ионами гораздо легче.
Например, существование иона [RfCl6]2- подтверждает, что при движении по таблице Менделеева в область сверхтяжелых элементов привычная «групповая» химия начинает корректироваться теорией относительности.
Проблема «одного атома»:
Резерфордий не существует в виде куска металла, который можно подержать в руках.
Его синтезируют в ускорителях по одному атому в минуту, и эти атомы живут лишь считанные секунды.
Вся «химия» резерфордия — это невероятно сложная автоматизированная работа роботов и детекторов, которые ловят распад каждого конкретного атома, чтобы доказать: «да, это соединение действительно RfCl4».
Интересный факт: Резерфордий стал предметом долгих споров о названии элемента между американскими и советскими физиками. СССР предлагал название «Курчатовий» (в честь Игоря Курчатова), а США — «Резерфордий».
В итоге международное сообщество IUPAC остановилось на втором варианте, но этот эпизод стал символом «холодной войны» в физике высоких энергий.
Пример решения задачи:
▶️ Дано:
Соединение: RfO2 (оксид резерфордия IV).
⌕ Найти:
Определите степень окисления (СО) резерфордия.
✨ Решение:
В оксидах кислород практически всегда имеет постоянную степень окисления -2.
В молекуле RfO2 содержится два атома кислорода, что дает суммарный отрицательный заряд: 2 · (-2) = -4.
Так как молекула электрически нейтральна, сумма степеней окисления всех атомов должна быть равна 0. Обозначим СО резерфордия за x:
x + 2 · (-2) = 0
x — 4 = 0
x = +4
✅ Ответ:
СО резерфордия (Rf) в данном оксиде равна +4.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 3, 5.
Разбор ошибок:
4 — неверно: элемент искусственно синтезирован.
Часто задаваемые вопросы
Теоретические расчёты указывают на потенциальную возможность существования и других состояний:
+3 — некоторые модели допускают такую возможность, но её реализация крайне маловероятна и не подтверждена экспериментально.
+2 — маловероятна, так как требует существенного отклонения от типичного поведения элементов IV группы.
Степени окисления +5 и +6 для резерфордия не рассматриваются современными теоретическими моделями как реалистичные.
Не проявляет отрицательных степеней окисления по трем фундаментальным причинам, связанным с его природой как тяжелого металла:
1. Природа элемента (Металл).
2. Энергетический барьер.
3. Релятивистские эффекты.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.