Теория:
Степень окисления ванадия в наиболее устойчивых соединениях равна +5, а также 0, +1, +2, +3, +4.
Это определяется его положением в периодической системе: ванадий — элемент 5‑й группы (побочная подгруппа), 4‑го периода.
Как переходный металл, он имеет пять валентных электронов на внешнем и предвнешнем уровнях (3d34s2), которые он способен отдавать ступенчато, образуя широкий спектр соединений разного цвета.
В отличие от ванадия, для многих других элементов положение в таблице даёт лишь базовую информацию о степенях окисления.
Чтобы определить все возможные значения, используют электронную формулу.
Например:
- Для фосфора (1s22s22p63s23p3) формула объясняет наличие трех неспаренных электронов и вакантных d-орбиталей, что позволяет ему проявлять степени окисления от -3 до +5;
- Для хрома (1s22s22p63s23p63d54s1) — возможность достижения высшей степени окисления +6 за счёт участия всех шести валентных электронов, включая «провалившийся» электрон с s-уровня.
Ванадий наиболее стабилен в своей высшей степени окисления +5, где он приобретает электронную конфигурацию инертного газа аргона ([Ar]).
![Степень окисления ванадия на примерах Схема: степени окисления ванадия (V) = +2, +3, +4, +5, +1 неустойчивая. Свойства (V), которые определяют СО: положение в ПС (5-я группа), электронная формула V [Ar] 3d³ 4s², электроотрицательность 1,63.](https://znaesh-kak.com/wp-content/uploads/2026/02/stepen-okisleniya-vanadiya.jpg)
Рис. Степень окисления ванадия 0, +2, +3, +4, +5. Факторы, влияющие на СО — наличие трех d-электронов и двух s-электронов, возможность их последовательной отдачи.
Содержание страницы
- 1. Почему у ванадия переменные степени окисления?
- 2. Степень окисления ванадия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Как определить степень окисления ванадия
- 3.1. По таблице Менделеева
- 3.2. По электронной конфигурации
- 3.3. По валентности (Число связей)
- 3.4. По химическому соединению (Алгебраический расчет)
- 4. Примеры степеней окисления ванадия
- 5. Шпаргалка для определения степени окисления ванадия
- 6. Пример решения задачи:
- 7. Проверка знаний: Как определить Ванадий по таблице Менделеева
- 8. Часто задаваемые вопросы
Почему у ванадия переменные степени окисления?
Причина многообразия ванадия — наличие пяти валентных электронов на 3d и 4s подуровнях.
- В простом веществе (V⁰): Пять валентных электронов принадлежат атому. Заряд равен 0.
3d [↑][↑][↑][ ][ ] 4s [↑↓]. - В соединениях (V+5): Ванадий отдаёт все 5 электронов, достигая конфигурации аргона. Подуровни 4s и 3d пустеют.
3d [ ][ ][ ][ ][ ] 4s [ ].
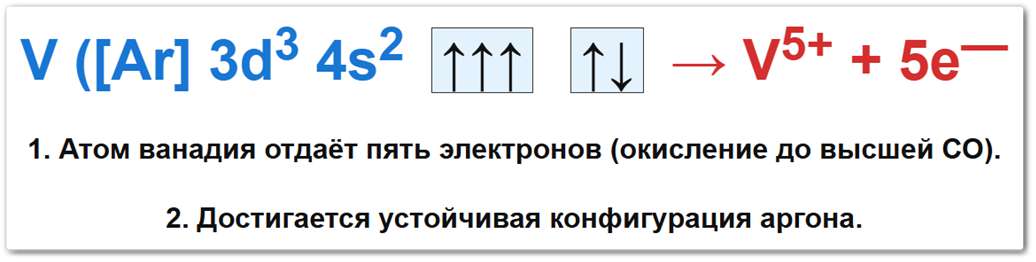
Рис. 2 Схема окисления атома ванадия: атом V ([Ar] 3d3 4s2) последовательно теряет электроны, достигая высшего состояния +5.
Степень окисления ванадия в соединениях
Ванадий — настоящий «хамелеон» в химии. Его растворы меняют цвет в зависимости от степени окисления: +2 (фиолетовый), +3 (зеленый), +4 (синий), +5 (желтый).
- Оксид ванадия(V) (V2O5): V +5, O -2.
- Оксид ванадия(IV) (VO2): V +4, O -2.
- Сульфат ванадила (VOSO4): V +4, O -2, S +6.
- Хлорид ванадия(III) (VCl3): V +3, Cl -1.
Высшая степень окисления
Высшая степень окисления ванадия равна +5 (соответствует номеру группы). Это состояние наиболее характерно для кислородных соединений, таких как ванадаты.
Низшая степень окисления
Низшая равна 0 (металл в чистом виде).
Промежуточные степени окисления
- +2, +3 — проявляют выраженные восстановительные свойства (легко отдают электроны дальше).
- +4 — довольно устойчивая степень окисления, встречается в виде иона ванадила (VO2+).
Примечание: степень окисления +1, крайне не стабильная и очень редкая.
Как определить степень окисления ванадия
По таблице Менделеева
По электронной конфигурации
- Электронная формула ванадия: [Ar] 3d3 4s2, подробнее о квантовых числах → [таблица].
- Сначала уходят 2 электрона с 4s-уровня (СО +2), затем последовательно три электрона с 3d-уровня (+3, +4, +5).
По валентности (Число связей)
Валентность ванадия в наиболее устойчивых соединениях (в степени окисления +5) равна V.
Это означает, что атом ванадия образует пять химических связей с более электроотрицательными элементами.
- В оксиде ванадия (V) V2O5 каждый атом ванадия образует по пять связей с атомами кислорода, проявляя валентность V.
- В соединениях ванадила (например, VOCl3) ванадий также пятичленен: он связан двойной связью с кислородом и тремя одинарными связями с хлором, валентность — V.
Примечание: Ванадий — один из немногих металлов, способных проявлять валентность, равную пяти, благодаря наличию пяти валентных электронов на 3d и 4s орбиталях.
По химическому соединению (Алгебраический расчет)
Пример для NH4VO3 (метанавадат аммония): Сумма СО равна 0. Группа NH4 имеет общий заряд +1, кислород -2. Обозначим ванадий за x.
(+1) + x + 3 · (-2) = 0 → 1 + x — 6 = 0 ⇒ x = +5.
Примеры степеней окисления ванадия
| СО | Цвет в растворе | Примеры соединений |
|---|---|---|
| +5 | Желтый | V2O5, KVO3 |
| +4 | Синий | VO2, VOSO4 |
| +3 | Зеленый | V2O3, VCl3 |
| +2 | Фиолетовый | VO, VCl2 |
Шпаргалка для определения степени окисления ванадия
Представьте, что атом ванадия — это кошелёк, в котором 5 монет (4s23d3).
- 0 — «кошелёк полный» (чистый металл V).
- +2 — «отдали 2 s-монеты» (состояние +2).
- +3 — «отдали 2 s-монеты и 1 d-монету» (состояние +3).
- +4 — «в кошельке осталась всего 1 d-монета» (состояние +4).
- +5 — «отдали всё до копейки» — достигли стабильного «нулевого баланса» аргона (состояние +5).
Пример решения задачи:
▶️ Дано:
Соединение: V2O5.
⌕ Найти:
Определите СО ванадия.
✨ Решение:
Кислород (O) имеет СО = −2. Сумма зарядов: 2 · x + 5 · (−2) = 0 → 2x − 10 = 0 → 2x = 10 → x = +5.
✅ Ответ:
V(+5).
Проверка знаний: Как определить Ванадий по таблице Менделеева
Отметьте три правильных утверждения для Ванадия (V):
Показать верные ответы и пояснения
Правильные ответы: 1, 3, 4
- 1) Порядковый номер 23 — это паспорт ванадия.
- 3) Формула 3d3 4s2 объясняет наличие 5 валентных электронов.
- 4) Номер группы (5) определяет его высшую степень окисления +5.
- 2 — ошибка (период 4-й), 5 — ошибка (это d-элемент).
Часто задаваемые вопросы
Из-за его способности легко переходить между степенями окисления +2, +3, +4 и +5, каждая из которых имеет свой неповторимый цвет в водном растворе.
Наиболее устойчивой является степень окисления +5, особенно в форме оксида V2O5 или ванадатов.
Это типичный металл. У него низкая электроотрицательность (1,63), поэтому ему гораздо выгоднее отдавать свои 5 валентных электронов, чем принимать чужие.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.