Содержание страницы
Резерфордий или Курчатовий
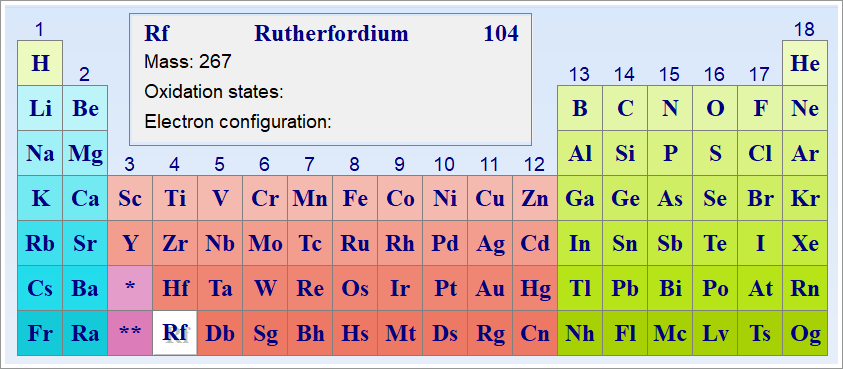
Rf (лат. Rutherfordium или Kurchatovium; по имени сов. физика И. В. Курчатова Кu), — 4-й группы искусственно полученный радиоактивный 104-й элемент в периодической системе (устаревшая классификация: IV группы периодической системы элементов.
Атомный номер 104, первый «трансактиноидный» элемент, для к-рого характерна степень окисления +4.
При облучении мишеней из калифорния, берклия и кюрия ускоренными ионами углерода, азота и кислорода, предложив назвать этот элемент резерфордием (Rf).
Химические свойства аналогичны химическим свойствам гафния. Безводный хлорид Резерфордий (Курчатовий) возгоняется при т-ре 313° С.
Физические свойства
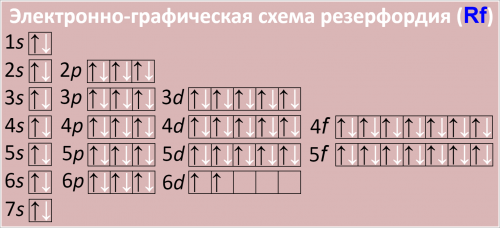
Полная электронная формула атома резерфордия в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d2
Подгруппа (IVB устаревшая классификация) лишь относительно недавно, в 1964 г., пополнилась еще одним элементом.
Получен он трудами коллектива ученых Объединенного института ядерных исследований в г. Дубне бомбардировкой изотопов плутония ускоренными ионами неона:
24294Pu + 2210Ne = 260104Ku + 4 10n
Реакция происходит в одном случае из нескольких миллиардов столкновений.
Время жизни этого элемента очень невелико — не более 4,5 с (изотоп ²⁶ºКu имеет период полураспада 0,1±0,05 с).
Теоретически предполагалось, что он первый из элементов, не входящих в число актиноидов. Подтверждением должно являться поведение его химических соединений.
Свойства вещества и соединений
Тщательными опытами было установлено, что его хлорид является аналогом циркония и гафния.
За основу метода идентификации была взята разница в летучести тетрахлоридов III и IV групп.
При 260° С хлориды гафния и его аналогов переходят в газообразное состояние, тогда как хлориды элементов III группы (в том числе лантаноидов) остаются твердыми.
Поток газа-носителя из ZrCI, и NbCl нагревался до 350° С и с огромной скоростью за десятые доли секунды переносил атомы резерфордий (курчатовия).
Образовавшиеся в результате облучения плутониевой мишени, к пластинам детектора.
Чтобы идентификация была как можно более тщательной, в поток вводили хлориды все возможных элементов с разными свойствами.
Резерфордий (курчатовий) неизменно осаждался вместе с гафнием.
Степень окисления Кu в этом соединении +4 значительное количество его изотопов с массой 261 и 260.
Однако из — за малого периода полураспада курчатовия нельзя надеяться получить его в ощутимых количествах.
Изотопы
Известны изотопы с массовыми числами 257Rf — 261Rf и периодами полураспада соответственно 4,5 ± 1,0; 0,01; 4,5 ± 1,5; около 0,1 и около 65 сек.
Резерфордий (Курчатовий) получен (1964) в Дубне (СССР) группой сов. физиков во главе с Г. Н. Флеровым при бомбардировке изотопа 242Рu ускоренными ионами 22Ne.
В 1969 амер. ученые А. Гиорсо и др. сообщили о получении в Беркли (США) изотопов 104-го элемента с массовыми числами 257Rf, 258Rf и 261Rf.
Литература
Флеров Г. Н., Друин В. А., Плеве А. А. Устойчивость тяжелых ядер и граница периодической системы элементов. «Успехи физических наук»

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.