Теория:
Степень окисления лоуренсия (Lr) в химических соединениях проявляет единственно стабильную степень окисления +3.
Это обусловлено завершением 5f-семейства актиноидов и достижением стабильной электронной конфигурации, характерной для элементов III группы.
Кроме того, выделяют показатель 0, который относится к лоуренсию в виде простого вещества (серебристо-белый радиоактивный металл).
Например для наиболее стабильной СО +3: в соединении LrCl3 (хлорид лоуренсия III) заряд иона равен +3.
В этом состоянии лоуренсий химически напоминает лютеций (лантаноид) и актиний.
Для сравнения, другие СО: стабильные соединения в иных степенях окисления для лоуренсия пока не получены, что делает его химию более предсказуемой по сравнению с предыдущими актиноидами.
- Почему +3? Атом лоуренсия отдает три валентных электрона (7s2 и 6p1 или 7s2 и 5f14 в зависимости от трактовки возбуждения), достигая наиболее энергетически выгодного состояния для элементов данной группы.
- Почему другие СО практически не встречаются? Лоуренсий является последним актиноидом, и его конфигурация достаточно стабильна для поддержания трехвалентного состояния.

Рис. 1. Основная степень окисления лоуренсия: 0 и +3.
Состояние +3 является единственным надежно установленным в химии этого элемента.
Важно заметить, что лоуренсий — крайне нестабильный элемент с очень коротким периодом полураспада.
Работы проводятся в специализированных ядерных лабораториях с использованием ускорителей частиц.
На свойства этого элемента влияют релятивистские эффекты, которые становятся критически важными для элементов конца 7-го периода.
Содержание страницы
- 1. Почему +3 — самая устойчивая степень окисления у лоуренсия
- 2. Степень окисления лоуренсия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему лоуренсий предпочитает заряд +3?
- 4. 4 способа определить степень окисления лоуренсия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления лоуренсия
- 6. Шпаргалка для лоуренсия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +3 — самая устойчивая степень окисления у лоуренсия
Стабильность трехвалентного состояния лоуренсия определяется завершенностью подгруппы III-B и стремлением достичь конфигурации инертного газа (с учетом заполненных f-оболочек).
- В простом веществе (Lr0): Заряд равен 0. Конфигурация:
[Rn] 5f14 7s2 7p1. - В трехвалентном ионе (Lr+3): Лоуренсий теряет 3 внешних электрона. Конфигурация:
[Rn] 5f14.
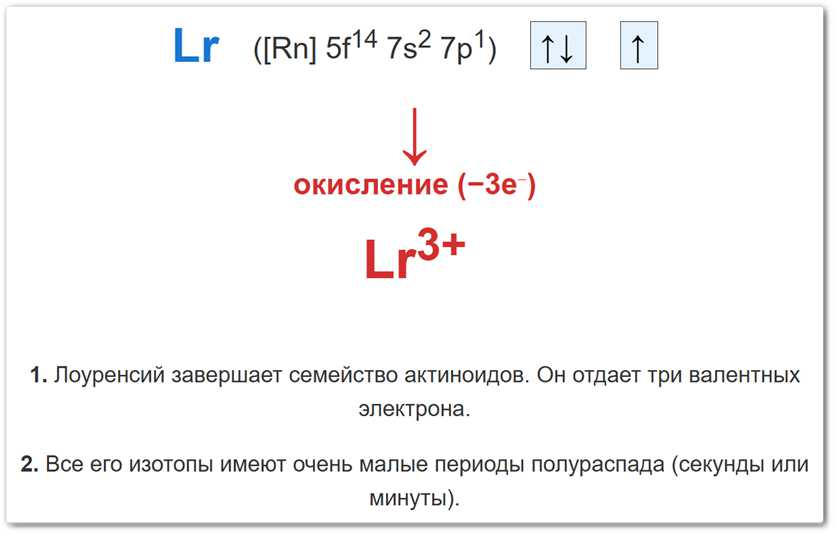
Рис. 2. Схема образования степени окисления +3: удаление валентных электронов и переход к конфигурации 5f14.
Степень окисления лоуренсия в соединениях
В химических исследованиях лоуренсий проявляет строго определенный характер:
- Хлорид лоуренсия(III) (LrCl3): Lr +3.
- Оксид лоуренсия(III) (Lr2O3): Lr +3.
Высшая степень окисления
Высшая степень окисления Lr равна +3. Это состояние единственное, которое можно считать химически подтвержденным.
Низшая степень окисления
Характерна степень окисления 0 в металлическом состоянии.
Промежуточные степени окисления
Степень окисления лоуренсия в веществах не проявляет других значимых состояний.
Важно: Лоуренсий является мостиком между актиноидами и переходными элементами 4-й группы, поэтому его изучение помогает понять пределы периодического закона.
Почему лоуренсий предпочитает заряд +3?
Характер взаимодействия продиктован его положением в конце ряда актиноидов:
- Положительная СО (+): Металл, легко теряет электроны.
- Заполненный f-слой: Конфигурация 5f14 — это «магический» уровень стабильности.
4 способа определить степень окисления лоуренсия
По таблице Менделеева
- Семейство: f-элемент (завершающий).
- Валентные электроны: 3 (7s2 7p1).
- Атомная масса: ~262 а.е.м.
По валентности (Число связей)
Валентность лоуренсия стабильно равна III, что определяет его способность образовывать три химические связи с типичными анионами.
Примеры:
- В LrCl3 (хлорид лоуренсия): Лоуренсий связан с тремя атомами хлора. Каждая связь — ковалентная полярная или ионная (в зависимости от условий), валентность Lr = III.
- В LrF3 (фторид лоуренсия): Лоуренсий образует три связи с наиболее электроотрицательным элементом — фтором, подтверждая свою стабильную трехвалентность.
- В Lr(OH)3 (гидроксид лоуренсия): Образует три связи с гидроксильными группами, проявляя свойства основания.
По электронной конфигурации
Электронная формула лоуренсия: [Rn] 5f14 7s2 7p1.
Как это работает (процесс ионизации):
- Для перехода в состояние +3 атом должен «отдать» три внешних электрона: два с 7s-подуровня и один с 7p-подуровня.
- Результат: После потери этих электронов у лоуренсия остается конфигурация
[Rn] 5f14, которая идентична конфигурации инертного газа радона с полностью заполненным f-слоем. - Наглядный итог: Эта «пустая» (без внешних электронов) структура является предельно стабильной, что объясняет, почему лоуренсий не стремится к другим степеням окисления. Это «энергетическая яма», из которой атом не хочет выходить.
По химическому соединению (Алгебраический расчет)
Пример для LrCl3: 3 хлора (-3), значит Lr = +3.
Примеры степеней окисления лоуренсия
| СО | Характеристика | Примеры |
|---|---|---|
| +3 | Единственная стабильная. | LrCl3 |
Шпаргалка для лоуренсия
- +3 — единственная стабильная СО.
- Релятивистские эффекты — определяют специфику его связей.
Пример решения задачи:
▶️ Дано:
Соединение: LrCl3 (хлорид лоуренсия III).
⌕ Найти:
Определите степень окисления (СО) лоуренсия.
✨ Решение:
В бинарных соединениях с хлором, галоген почти всегда проявляет заряд -1.
В молекуле LrCl3 содержится три атома хлора, что дает суммарный отрицательный заряд: 3 · (-1) = -3.
Так как молекула электрически нейтральна, сумма степеней окисления всех атомов должна быть равна 0. Обозначим СО лоуренсия за x:
x + 3 · (-1) = 0
x — 3 = 0
x = +3
✅ Ответ:
СО лоуренсия (Lr) в данном соединении равна +3.
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: он искусственно синтезированный радиоактивный элемент.
Часто задаваемые вопросы
Нет, экспериментально зафиксирована и подтверждена только степень окисления +3.
Это делает лоуренсий химически более однообразным по сравнению с предыдущими элементами ряда.
Как и у всех тяжелых актиноидов, это исключено его химической природой:
Низкая электроотрицательность: Лоуренсий является активным металлом, который отдает электроны, а не стремится их принять.
Металлическая природа: Его атомная структура не приспособлена к формированию анионов, что характерно только для неметаллов.
Лоуренсий — это «завершающий аккорд» ряда. Хотя он классифицируется как актиноид, его электронное строение начинает проявлять признаки, характерные для переходных металлов III-B группы.
Что делает его уникальным объектом для изучения влияния релятивистских эффектов на химию элементов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.