Теория:
Эрбий (Er) в периодической системе: 6‑й период, 3‑я группа (по устаревшей классификации — III B), атомная масса 167,26 а.е.м.
Занимает положение в 6‑м периоде, что определяет его принадлежность к семейству лантаноидов — редкоземельных металлов с уникальными оптическими и магнитными свойствами.
Будучи химическим аналогом других лантаноидов, он входит в состав большой группы f-элементов, расположенных после Лантана.
Нахождение Эрбия в 3‑й группе (согласно длиннопериодному варианту) и специфическое заполнение f-подуровня обуславливают его ключевые параметры:
Наиболее характерную валентность III.
А также способность проявлять парамагнитные свойства и специфическое розовое свечение при возбуждении его ионов.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Xe] 4f12 6s2.
На которой наглядно можно определить его положение как f-блочного элемента, где происходит последовательное заполнение 4f-подуровня.
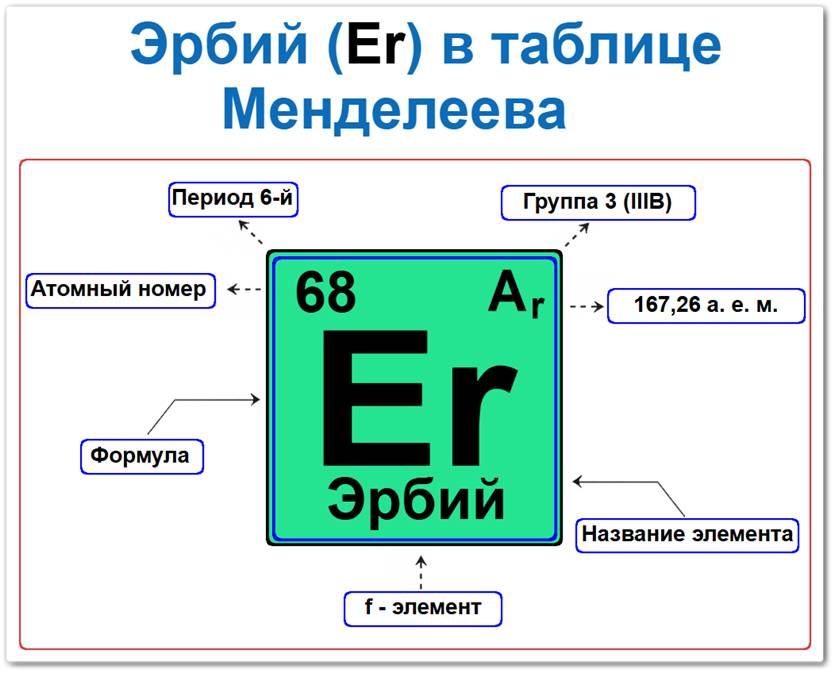
Эрбий в таблице Менделеева можно определить на основании закона периодичности: положение в ряду лантаноидов период 6, группа III / Лантаноиды, а также по его порядковому номеру (Z = 68).
Содержание страницы
- 1. Как определить положение Эрбия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 68)
- 3. Название и символ
- 4. Группа (3 / III B)
- 5. Период (6‑й)
- 6. Относительная атомная масса (Ar)
- 7. f‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Эрбия по Таблице Менделеева
- 9. Проверка знаний: Как определить эрбий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Эрбия в Таблице Менделеева
Локация эрбия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (формально 3-я группа, семейство лантаноидов).
- Период (горизонтальный ряд).
- Электронное семейство (эрбий — f‑элемент).
Порядковый номер / атомный номер (Z = 68)
- Служит уникальным кодом элемента в системе.
- В ядре — 68 протонов; в нейтральной оболочке — 68 электронов.
- Электронное строение: [Xe] 4f12 6s2.
Важно: Частично заполненная 4f-оболочка делает эрбий незаменимым в лазерных технологиях и оптоволоконной связи (усилители сигнала).
Название и символ
- Название: «эрбий» (назван в честь шведской деревни Иттербю, где был найден минерал гадолинит).
- Символ: Er.
- Примечание: Открыт Карлом Мосандером в 1843 году при исследовании иттриевой земли, найден в минерале гадолинит, получают из монацита.
Группа (3 / III B)
Расположен в 3‑й группе (лантаноиды обычно выносятся в отдельную строку внизу таблицы, но относятся к этой группе).
Химический потенциал:
- Валентность эрбия: типичная валентность III.
- Степень окисления: +3. Оксид эрбия (Er2O3) имеет характерный розовый цвет и используется для окрашивания стекла и эмалей.
Период (6‑й)
Находится в 6‑м периоде — его электроны распределены по шести энергетическим уровням.
Влияние на свойства:
- Лантаноидное сжатие: Как и у всех элементов этого ряда, у эрбия наблюдается уменьшение атомного радиуса, что влияет на его химическую активность.
- Парамагнетизм: Благодаря неспаренным электронам на f-орбитали, эрбий проявляет сильные магнитные свойства при низких температурах.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Er) ≈ 167,26 а.е.м.
- Определение: средневзвешенное значение массы стабильных изотопов, преобладающим из которых является Эрбий-166.
Все значения для всех элементов можно узнать в таблице атомных масс.
f‑Элемент (электронное семейство)
Застраивающимся является 4f‑подуровнь (4f12).
Специфика блока: Будучи f-элементом, эрбий демонстрирует глубокое залегание валентных электронов, что делает его химические свойства схожими с другими редкоземельными элементами, такими как гольмий или тулий.
Определение энергетических уровней Эрбия по Таблице Менделеева
Положение Эрбия (Er) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 6-й период (Количество этажей)
Эрбий находится в шестой строке таблицы. Номер периода определяет число электронных слоев.
- Итог: У Эрбия 6 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Эрбия — 68. Его 68 электронов распределены по уровням следующим образом:
Er ) 2 ) 8 ) 18 ) 30 ) 8 ) 2
3. 3-я группа (Химический характер)
Эрбий входит в семейство лантаноидов.
- f-элемент: Свойства определяются заполнением глубокого 4f-слоя.
- Место в блоке: Является «тяжелым» лантаноидом иттриевой группы.
Проверка знаний: Как определить эрбий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Эрбий (Er) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 68. Постоянная координата Эрбия.
- 2) 6-й период, лантаноиды. Указывает на принадлежность к редкоземельным f-элементам.
- 3) Серебристо-белый металл. Физическое состояние чистого элемента при нормальных условиях.
- 4) Ошибка. Галогены — это p-элементы 17-й группы.
- 5) Ошибка. Эрбий в 6-м периоде, он гораздо тяжелее железа.
- 6) Ошибка. Для эрбия наиболее характерна валентность III.
Часто задаваемые вопросы:
Эрбий расположен в 6-м периоде. Формально он относится к 3-й группе как часть семейства лантаноидов. Его порядковый номер — 68.
У эрбия 6 энергетических уровней, так как он находится в 6-м периоде.
Электронная схема: 2, 8, 18, 30, 8, 2.
Эрбий является f-элементом. Его свойства определяются постепенным заполнением внутреннего 4f-электронного подуровня.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.