В группу щелочных металлов входит следующий ряд металлов:
Это элементы 1-й группы (устаревшая классификация: главной подгруппе I группы периодической системы).
Содержание страницы
Что такое щелочные металлы
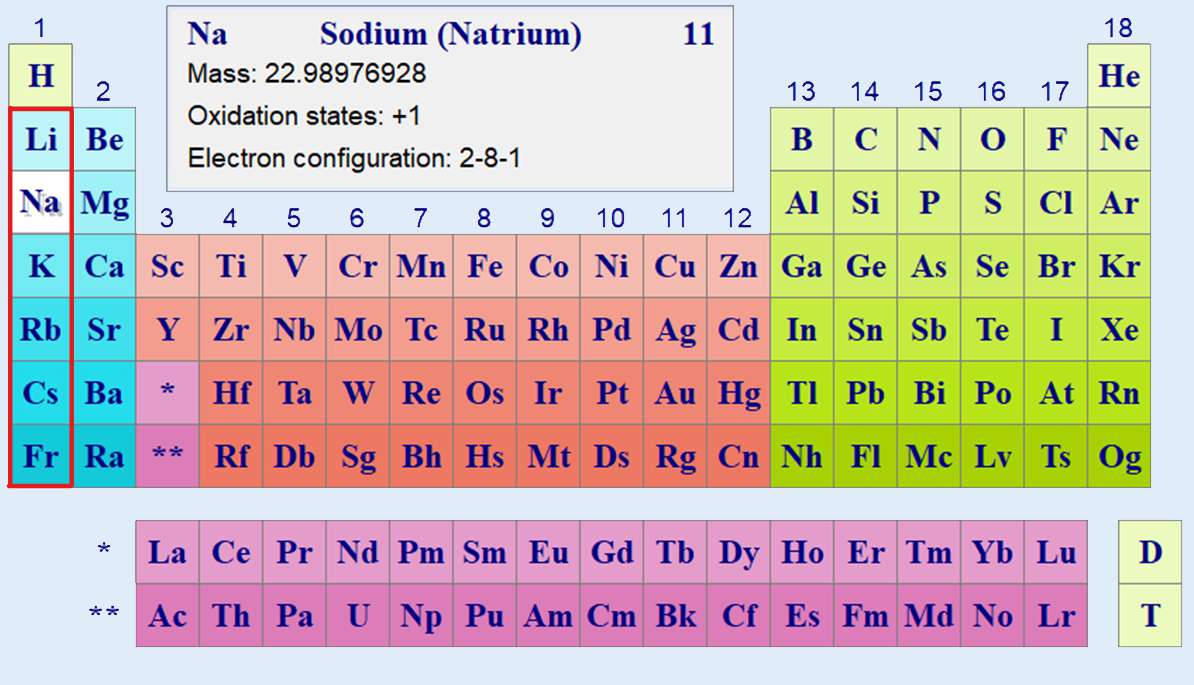
Все эти металлы сходны в том отношении, что на внешнем электронном слое их имеется один электрон (таблице).
Щелочные металлы относятся к числу s — элементов.
Электрон внешнего электронного слоя атома щелочного металла по сравнению с другими элементами того же периода наиболее удален от ядра.
То есть радиус атома щелочного металла наибольший по сравнению с радиусами атомов других элементов того же периода.
Таблица распределения электронов по энергетическим уровням у атомов щелочных металлов.
| Элемент | Заряд ядра | Число электронов на энергетических уровнях | Радиус атома | ||||||
| Литий Li | + 3 | 2 | 1 | ||||||
| Натрий Na | + 11 | 2 | 8 | 1 | |||||
| Калий К | + 19 | 2 | 8 | 8 | 1 | ||||
| Рубидий Rb | + 37 | 2 | 8 | 18 | 8 | 1 | |||
| Цезий Cs | + 55 | 2 | 8 | 18 | 18 | 8 | 1 | ||
| Франций Fr | + 87 | 2 | 8 | 18 | 32 | 18 | 1 | ||
В связи с этим валентный электрон внешнего слоя атомов щелочных металлов легко отрывается, превращая их в положительные однозарядные ионы.
Этим обусловлено то, что соединения щелочных металлов с другими элементами построены по типу ионной связи.
В окислительно-восстановительных реакциях щелочные металлы ведут себя как сильные восстановители, и эта способность возрастает от металла к металлу с увеличением заряда ядра атома.
Среди металлов щелочные металлы проявляют наиболее высокую химическую активность. В ряду напряжений все щелочные металлы располагаются в начале ряда.
Электрон внешнего электронного слоя является единственным валентным электроном, поэтому щелочные металлы в любых соединениях одновалентны.
Степень окисления щелочных металлов обычно +1.
Таблица физических свойств щелочных металлов.
| Элемент | Порядковый номер | Атомный вес | Температура плавления, °С | Температура кипения, °С | Плотность, г/смЗ | Твердость по шкале |
| Литий | 3 | 6,94 | 186 | 1336 | 0,53 | 0,6 |
| Натрий | 11 | 22,997 | 98 | 880 | 0,97 | 0,4 |
| Калий | 19 | 39,1 | 63 | 760 | 0,86 | 0,5 |
| Рубидий | 37 | 85,48 | 38,5 | 700 | 1,53 | 0,3 |
| Цезий | 55 | 132,91 | 28 | 670 | 1,9 | 0,2 |
Типичными представителями щелочных металлов являются натрий и калий.
➡️ 26. Составьте общую характеристику щелочных металлов по следующему плану:
а) сходство и различие в строении атомов щелочных металлов;
б) особенности поведения щелочных металлов в окислительно-восстановительных реакциях;
в) тип кристаллической решетки в соединениях щелочных металлов;
г) особенности изменения физических свойств металлов в зависимости от радиуса атома. (См. Ответ)
Натрий
Электронная конфигурация атома натрия ls22s22p63s1. Структура его внешнего слоя:

Натрий встречается в природе только в виде солей. Наиболее распространенной солью натрия является поваренная соль NaCl, а также минерал сильвинит КCl · NaCl и некоторые сернокислые соли.
Например глауберова соль Na2SO4 · 10H2O, встречающаяся в больших количествах в заливе Каспийского моря Кара-Богаз-Гол.
Из поваренной соли NaCl металлический натрий получают путем электролиза расплава этой соли. Установка для электролиза изображена на рис. 2.
В расплавленную соль опускают электроды. Анодное и катодное пространство разделено диафрагмой, которая изолирует образующийся хлор от натрия, чтобы не произошло обратной реакции.
Положительный ион натрия принимает с катода электрон и превращается в нейтральный атом натрия. Нейтральные атомы натрия собираются на катоде в виде расплавленного металла.
Происходящий на катоде процесс можно изобразить следующей схемой:
Na+ + Na0.
Поскольку на катоде происходит принятие электронов, а всякое принятие электронов атомом или ионом является восстановлением, то ионы натрия на катоде восстанавливаются.
На аноде ионы хлора отдают электроны, т. е. происходит процесс окисления и выделение свободного газообразного хлора, что можно изобразить следующей схемой:
Cl— — е— → Cl0
Полученный металлический натрий имеет серебристо-белый цвет, легко режется ножом.
Срез у натрия, если его рассмотреть сразу после разреза, имеет яркий металлический блеск, но быстро тускнеет вследствие крайне быстрого окисления металла.

Рис. 2. Схема установки для электролиза расплава поваренной соли. 1 — кольцевой катод; 2 — колокол для выведения газообразного хлора из анодного пространства.
Если натрий окислять в небольшом количестве кислорода при температуре около 180°, то получается окись натрия:
4Na + О2 = 2Na2O.
При горении в кислороде получается перекись натрия:
2Na + O2 = Na2O2.
При этом натрий сгорает ослепительно желтым пламенем.
В связи с легкой и быстрой окисляемостью натрия его хранят под слоем керосина или парафина, причем парафин предпочтительнее.
Так как в керосине все же растворяется некоторое количество воздуха и окисление натрия хотя и медленно, но все же происходит.
Натрий может давать соединение с водородом — гидрид натрия NaH, в котором водород проявляет степень окисления — 1.
Это соле подобное соединение, которое по характеру химической связи и величине степени окисления отличается от летучих гидридов элементов главных подгрупп IV—VII группы.
Металлический натрий может реагировать не только с кислородом и водородом, но и с многими простыми и сложными веществами.
Например, при растирании в ступке с серой натрий бурно реагирует с ней, образуя сульфид натрия:
2Na + S = Na2S
Реакция сопровождается вспышками, поэтому ступку нужно держать подальше от глаз и обернуть руку полотенцем.
Для реакции следует брать небольшие кусочки натрия.
Натрий энергично сгорает в хлоре с образованием хлорида натрия, что особенно хорошо наблюдать в хлор-кальциевой трубке, в которой через расплавленный и сильно разогретый натрий пропускают ток хлора:
2Na + Сl2 = 2NaCl
Натрий реагирует не только с простыми, но и со сложными веществами/
Примером может служить вода Н2О, вытесняя из нее водород, так как является весьма активным металлом, в ряду напряжений стоит намного левее водорода и легко вытесняет последний из воды.
Пример:
2Na + 2Н2O = 2NaOH + H2
Загоревшийся щелочной металл нельзя тушить водой. Лучше всего засыпать его порошком кальцинированной соды.
В присутствии натрия бесцветное пламя газовой горелки окрашивается в желтый цвет.
Металлический натрий можно использовать как катализатор в органическом синтезе, например при производстве синтетического каучука из бутадиена.
Он служит исходным веществом для получения других соединений натрия, например перекиси натрия.
➡️ 27. Докажите с помощью приведенных в тексте уравнений реакций с участием металлического натрия, что он ведет себя как восстановитель. (См. Ответ)
28. Почему натрий нельзя хранить на воздухе?
29. Ученик опустил в раствор сульфата меди кусочек натрия, надеясь вытеснить из соли металлическую медь. Вместо металла красного цвета получился студенистый голубой осадок.
Опишите происшедшие реакции и напишите их уравнения в молекулярной и ионной формах. Как следовало изменить условия реакции, чтобы реакция привела к желаемому результату?
Уравнения напишите в молекулярной, полной и сокращенной ионной формах.
30. В сосуд с 45 мл воды поместили 2,3 г металлического натрия. Какова концентрация раствора едкого натра, образовавшегося по окончании реакции.
31. Какие средства можно применять при тушении загоревшегося натрия? Дайте обоснованный ответ. (См. Ответ)
Кислородные соединения натрия. Едкий натр
Кислородными соединениями натрия, как уже было сказано, являются окись натрия Na2O и перекись натрия Na2O2.
Окись натрия Na2O особого значения не имеет.
Она энергично реагирует с водой, образуя едкий натр:
Na2O + Н2O = 2NaOH
Перекись натрия Na2О2 — желтоватый порошок.
Ее можно рассматривать как своеобразную соль перекиси водорода, ибо структура ее такая же, как у Н2O2. Как и перекись водорода, перекись натрия является сильнейшим окислителем.
При действии воды она образует щелочь и перекись водорода:
Na2O2 + Н2O = Н2O2 + 2NaOH
Перекись водорода образуется и при действии разбавленных кислот на перекись натрия:
Na2O2 + H2SO4 = Н2O2 + Na2SO4
Все указанные выше свойства перекиси натрия позволяют использовать ее для отбелки все возможных материалов.
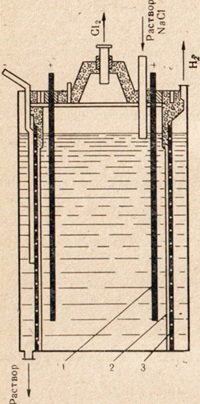
Рис. 3. Схема установки для электролиза раствора поваренной соли. 1 — анод; 2 — диафрагма, разделяющее анодное и катодное пространство; 3 —катод.
Очень важным соединением натрия является гидроокись натрия, или едкий натр, NaOH. Его называют также каустической содой, или просто каустиком.
Для получения едкого натра используют поваренную соль — наиболее дешевое природное соединение натрия, подвергая ее электролизу, но в этом случае применяют не расплав, а раствор соли (рис. 3).
На рис. 3 показано, что анодное и катодное пространство разделено диафрагмой.
Это сделано с той целью, чтобы образующиеся продукты не вступали между собой во взаимодействие.
Например:
Сl2 + 2NaOH = NaClO + NaCl + Н2O.
Едкий натр — твердое кристаллическое вещество белого цвета, прекрасно растворимое в воде.
При растворении едкого натра в воде выделяется большое количество тепла и раствор сильно разогревается.
Едкий натр необходимо хранить в хорошо закупоренных сосудах, чтобы предохранить его от проникновения водяных паров, под действием которых он может сильно увлажниться.
А также двуокиси углерода, под действием которой едкий натр может постепенно превратиться в карбонат натрия:
2NaOH + СO2 = Na2CO3 + Н2O.
Едкий натр — типичная щелочь, поэтому меры предосторожности при работе с ним такие же, как и при работе с любыми другими щелочами.
Едкий натр применяется во многих отраслях промышленности.
Например:
- Для очистки нефтепродуктов.
- Производства мыла из жиров.
- В бумажной промышленности.
- В производстве искусственного волокна и красителей.
- Производстве медикаментов и др. (рис. 4).
▷ Запишите в тетрадь области применения едкого натра.
Из солей натрия следует отметить в первую очередь поваренную соль NaCl, которая служит основным сырьем для получения едкого натра и металлического натрия, соду Na2CO3, сульфат натрия Na2SO4, нитрат натрия NaNO3 и др.
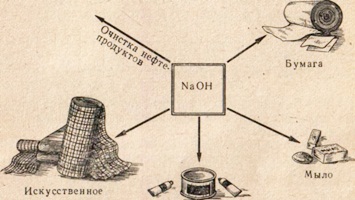
Рис. 4. Применение едкого натра.
➡️32. Опишите способ получения едкого натра электролизом поваренной соли. (См. Ответ)
33. Едкий натр можно получить действием на карбонат натрия гашеной известью.
Составьте молекулярную и ионные формы уравнения этой реакции, а также рассчитайте, сколько соды, содержащей 95% карбоната, потребуется для получения 40 кг едкого натра.
34. Почему при хранении раствора едкого натра в склянках с притертыми пробками пробки «заедают» и их нельзя вынуть?
Если же в течение некоторого срока подержать склянку опрокинутой в воду, то пробка свободно вынимается. Объясните, приведя уравнения реакций, что за процессы имеют место в данном случае.
35. Напишите уравнения реакций в молекулярной и ионных формах, характеризующих свойства едкого натра как типичной щелочи.
36. Какие меры предосторожности следует соблюдать при работе с едким натром? Какие меры первой помощи следует оказать при ожогах едким натром? (См. Ответ)
Калий
Калий К — также довольно распространенный щелочной металл, отличающийся от натрия величиной атомного радиуса (четвертый период) и потому обладающий большей химической активностью, чем натрий.
Электронная конфигурация атома калия:
1s22s22p63s23p64s1.
Структура его внешнего электронного слоя:
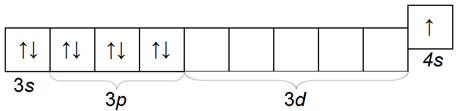
Калий — мягкий металл, который хорошо режется ножом. Во избежание окисления его, как и натрий, хранят под слоем керосина.
С водой калий реагирует еще более бурно, чем натрий, с образованием щелочи и с выделением водорода, который загорается:
2К + 2Н2O = 2КОН + Н2.
При сжигании в кислороде (при этом для сжигания рекомендуется брать еще более мелкие кусочки металла, чем для сжигания натрия) он, подобно натрию, сгорает очень энергично с образованием перекиси калия.
Следует отметить, что в обращении калий гораздо опаснее натрия. Сильный взрыв может произойти даже при разрезании калия, поэтому обращаться с ним нужно еще осторожнее.
Гидроокись калия, или едкое кали КОН — белое кристаллическое вещество. Едкое кали во всех отношениях сходно с едким натром.
Они широко применяются в мыловаренной промышленности, но его получение обходится несколько дороже, поэтому такого применения, как NaOH, оно не находит.
Соли калия следует отметить особо, так как некоторые из них широко используются в качестве удобрения.
Таковы хлорид калия КСl, нитрат калия KNO3, который является также азотным удобрением.
➡️ 37. Чем объяснить то, что едкое кали химически активнее едкого натра? (См. Ответ)
38. В кристаллизатор с водой опустили кусочек калия. После того как реакция закончилась, туда же поместили немного гидроокиси цинка в виде белого студенистого осадка.
Осадок исчез, а при испытании раствора фенолфталеином последний окрасился в малиновый цвет. Какие химические процессы здесь произошли?
Какие вещества находятся в растворе? Дайте обоснованный ответ.
39. Почему калий, как и все щелочные металлы, относят к семейству s-элементов? (См. Ответ)
Статья на тему Щелочные металлы

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.