Химические свойства углерода
- При обычных условиях углерод химически инертен. При нагревании его активность увеличивается.
- Способность образовывать длинные цепочки из одноименных атомов.
- Проявляет аморфные свойства: аморфный углерод, менее активен графит, самый инертный — алмаз.
- Имеет промежуточную степень окисления, равную 0. Проявляет как окислительные свойства так и восстановительные свойства.
- Реагирует с неметаллами:
в избытке кислорода сгорает с образованием оксида углерода (IV);
в условиях недостатка кислорода образуется оксид углерода (II). - Реагирует с оксидами металлов:
способен восстанавливать многие металлы из их оксидов. - Реагирует с металлами: при высокой температуре углерод реагирует с металлами, образуя карбиды, в присутствии никелевого катализатора углерод взаимодействует с водородом, образуя метан, при взаимодействии с кремнием при высокой температуре углерод образует карбид кремния.

Содержание страницы
- 1. Углерод свойства
- 1.1. Что такое углерод
- 1.2. Графит
- 1.3. Аморфный углерод
- 1.4. Противогаз
- 1.5. Химические свойства углерода
- 1.6. Водяной газ (СО)
- 1.7. Окислы углерода
- 1.8. Применение окиси углерода
- 1.9. Газификация угля
- 1.10. Двуокись углерода СО2
- 1.11. Угольная кислота и ее соли
- 1.12. Карбонаты и бикарбонаты
- 1.13. Круговорот углерода в природе
- 1.14. Вывод
Углерод свойства
К элементам главной подгруппы IV группы принадлежат углерод С, кремний Si, германий Ge, олово Sn, свинец Рb.
Все они относятся к р-элементам, так как у них достраивается р-электронная оболочка внешнего слоя (табл.).
С увеличением заряда ядра радиус атома возрастает и заметно уменьшается электроотрицательность.
В связи с этим от углерода к свинцу заметно усиливаются металлические свойства.
Так, свинец обладает хорошо выраженными металлическими свойствами, в то время как углерод причисляют к неметаллам.
Четырех электронный внешний слой и малые атомные радиусы углерода и кремния способствуют образованию ковалентных связей, которые типичны для этих элементов.
Особенностью как углерода, так и кремния является способность образовывать длинные цепочки из одноименных атомов, что приводит к большому многообразию органических и кремнийорганических веществ.
Углерод и кремний могут образовывать как две, так и четыре валентные связи.
Максимальная степень окисления элементов главной подгруппы IV группы равна +4. Это говорит о том, что для их атомов условно возможна отдача 4 электронов.
Принять на внешний слой они также способны не более электронов.
В окислительно-восстановительных реакциях они ведут себя как восстановители.
| Элемент | Заряд ядра | Число электронов на энергетических уровнях | Радиус атома, Å | ||||||
| K | L | M | N | O | P | Q | |||
| Углерод С | + 6 | 2 | 4 | 4 | 4 | 4 | 4 | 0,77 | |
| Кремний Si | +15 | 2 | 8 | 18 | 18 | 18 | |||
| Германий Ge | +32 | 2 | 8 | 18 | 32 | ||||
| Олово Sn | +50 | 2 | 8 | 18 | |||||
| Свинец Рb | +82 | 2 | 8 | ||||||
Высшие окислы этих элементов проявляют кислотные свойства.
Им соответствуют кислоты, представляющие собой очень слабые электролиты.
Это говорит о том, что среди главных подгрупп IV—VII группы подгруппа углерода объединяет элементы с наименее выраженными неметаллическими свойствами.
Прочность летучих гидридов заметно уменьшается от углерода СН4 к свинцу РbН4.
Нельзя не отметить характер свойств окислов, в которых элементы проявляют степень окисления +2.
Если углерод образует при этом несолеобразующий окисел СО, то окись свинца РbО обладает хорошо выраженными амфотерными свойствами.
➡️ 1. Среди элементов группы углерода укажите:
а) элемент с наименьшим атомным радиусом;
б) элемент с наиболее выраженными металлическими свойствами;
в) формулы высших окислов элементов группы углерода;
г) формулы высших кислородных кислот, соответствующих названным окислам;
д) формулы низших окислов;
е) изменение устойчивости летучих водородных соединений (написать ряд формул и стрелкой указать направление уменьшения устойчивости). (См. Ответ).
Что такое углерод
Атомный вес углерода 12,011. Внешний электронный слой атома углерода имеет 4 электрона, его электронная конфигурация 2s22p2, распределение электронов по орбиталям.
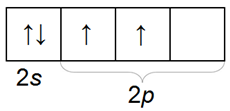
Среди элементов подгруппы углерод обладает наибольшим значением электроотрицательности.
Углерод имеет три аллотропных видоизменения — алмаз, графит и аморфный углерод.
Алмаз и графит встречаются в природе, а аморфный углерод может быть получен лишь искусственным путем.
Алмаз — твердое кристаллическое вещество, тугоплавкое и химически мало активное. Чистый алмаз — бесцветные прозрачные кристаллы.
Среди минералов алмаз обладает наивысшей твердостью, равной 10, плотность его 3,514.
Такая высокая твердость объясняется строением его кристаллической решетки атомного типа, в которой атомы углерода находятся на одинаковом расстоянии друг от друга (см. рис. Структура алмаза).
Благодаря твердости алмаз широко применяется для резки стекла, бурения твердых пород, в машинах для волочения проволоки, шлифовальных дисках и т. д.
Для этих целей используют алмазы, загрязненные разными примесями.
Чистые бесцветные кристаллы подвергают огранке и шлифовке алмазным порошком и превращают в бриллианты. Чем больше граней, тем лучше «играет» бриллиант.
Бриллианты бывают чаще всего небольшими, их вес измеряется каратами (1 карат равен 0,2 г). Но встречаются и крупные бриллианты.
Графит
Графит — мелкокристаллический минерал, в кристаллической решетке которого расстояние между атомами одинаково лишь в двух направлениях, а в третьем намного больше.
Это делает кристаллы графита непрочными, а сам минерал мягким. Твердость графита равна 1, плотность 2,22, температура плавления около 3000°.
Графит обладает хорошей электропроводностью, поэтому применяется для изготовления электродов, обкладок для электролитических ванн.
Порошок графита, смешанный с минеральным маслом, является хорошей смазкой. Поскольку графит мягче бумаги и может оставлять на ней след, его применяют для изготовления карандашных грифелей, туши, типографской краски, копировальной бумаги.
Высокая термостойкость графита позволяет изготавливать из него огнеупорные тигли.
Графит удается получать искусственным путем — нагреванием кокса до 2500— 3000°.
➡️ 2. Какого типа кристаллические решетки имеют алмаз и графит?
3. Объясните с точки зрения электронной конфигурации электронных слоев, почему углерод может образовывать как две, так и четыре валентные связи. (См. Ответ).
Аморфный углерод
Существует мнение, что получаемый искусственно аморфный углерод (сажа, древесный уголь) не является самостоятельным аллотропным видоизменением, так как его микрокристаллическая структура такая же, как у графита.
Аморфный углерод в виде древесного угля получается при сухой перегонке древесины в виде очень легкой хрупкой пористой массы.
Структура аморфного углерода очень сходна со структурой графита, но кристаллы в нем расположены беспорядочно.
Огромная поверхность древесного угля обусловливает характерное для него явление адсорбции.
Молекулы углерода, находящиеся на поверхности кусочка угля, притягивают к себе молекулы веществ из окружающей его среды, преодолевая энергию теплового движения молекул.
Ясно, что чем больше поверхность, тем сильнее идет адсорбция, поэтому измельченный адсорбент лучше адсорбирует.
Если тщательно измельчить древесный уголь, а затем поместить его под колпак, где находятся пары брома, то можно заметить, как постепенно окраска брома слабеет и, в конце концов, исчезает.
Если порошок угля взболтать в пробирке с раствором марганцовокислого калия, фуксина или с настойкой чая, то вскоре эти растворы обесцвечиваются.
Если прокипятить адсорбент вместе с адсорбированным на его поверхности веществом в чистой воде, то окраска раствора появляется вновь, так как тепловое движение молекул усиливается и они срываются с поверхности адсорбента — про исходит десорбция.
Следует отметить также, что явление катализа, которое было рассмотрено выше, тесно связано с явлением адсорбции.
➡️ 4. Какое явление называется адсорбцией? (См. Ответ)
5. Где еще имеет месте явление адсорбции, помимо процессов, связанных с древесным углем?
6. Дайте объяснение явлению десорбции и укажите причины, способствующие этому явлению. (См. Ответ).
Противогаз
При обработке перегретым водяным паром из пор угля удаляются имеющиеся там иногда посторонние примеси, увеличивается пористость угля. Такой уголь называется активированным.
Активированный уголь очень широко применяется, в частности, в противогазе, впервые предложенном акад.
Н. Д. Зелинским для защиты дыхательных путей от ядовитых газов, находящихся в воздухе.
Впервые такой противогаз был применен во время первой мировой войны (рис.).
Противогаз состоит из резиновой маски или шлема, плотно облегающего лицо и голову, гофрированной резиновой трубки, соединяющей маску с коробкой, содержащей очищающие воздух вещества.
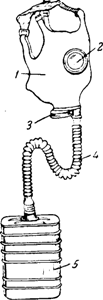
Система клапанов пропускает вдыхаемый воздух в маску только через коробку, а выдыхаемый — прямо в окружающее пространство.
Противогазная коробка содержит расположенные слоями противодымный фильтр, задерживающий твердые и капельные частицы, химический поглотитель, химически связывающий поступающие в коробку отравляющие вещества, и активированный уголь.
Активированный уголь иногда дается в виде суспензии в воде внутрь в случае попадания в желудок ядовитых веществ.
Рис. Противогаз: 1- резиновая маска, 2- очки, 3- выдыхательный клапан, 4 — гофрированная трубка, 5 — поглотительная коробка
Древесный уголь применяется также для изготовления черного пороха.
Аморфный углерод в виде кокса применяется в металлургии. Получают кокс в коксохимических печах из каменного угля.
Это твердое пористое вещество, представляющее собой почти чистый углерод. Кокс является прекрасным топливом и хорошим восстановителем.
Сажа получается при сжигании газообразных веществ с высоким процентом содержания углерода.
В виде сажи аморфный углерод широко применяется в резиновой промышленности и в полиграфии для изготовления типографской краски.
Сажа наиболее высокого качества получается при сжигании газообразного топлива, например ацетилена.
➡️ 7. Составьте и заполните следующую таблицу: (См. Ответ)
| Аморфный углерод | ||||
| Алмаз | Графит | Древесный уголь | Сажа | Кокс |
Химические свойства углерода
Следует отметить, что главным свойством углерода является его восстанавливающая способность. Углерод — один из лучших восстановителей.
Он легко восстанавливает металлы из их окислов при нагревании:
и легко сгорает в кислороде, образуя окись или двуокись углерода:
2С + O2 = 2СО—
С + О2 = СО2
Сплавляясь с металлами, углерод образует карбиды, имеющие очень своеобразное строение молекул.
Например, особенно широко применяющийся в технике карбид кальция СаС2 имеет следующее строение:
С водородом углерод соединяется только при температуре около 1200°, образуя органическое соединение метан СН4:
С + 2Н2 = СН4
➡️ 8. Рассчитайте, какое количество меди можно восстановить из ее окиси СuО с помощью 24 кг углерода, если потери меди составляют 5%. (См. Ответ).
Водяной газ (СО)
При пропускании перегретого водяного пара через раскаленный уголь последний восстанавливает из воды водород, в результате чего образуется водяной газ:
С + Н2О = СО + Н2
Несмотря на высокую восстановительную способность углерода, применение его как восстановителя не всегда удобно, так как он является твердым веществом.
Гораздо удобнее использовать газообразные восстановители. Тогда контакт между восстановителем и восстанавливаемым веществом становится более полным.
В связи с этим углерод целесообразно переводить в окись углерода, сохраняющую его восстановительные свойства и являющуюся в то же время газообразным веществом.
➡️ 9. Какой объем водяного газа (условия нормальные) можно получить при пропускании водяного пара через 5 грамм-атомов углерода? (См. Ответ)
10. Нитрат меди прокалили до полного прекращения выделения бурого газа, после чего смешали с измельченным углем и снова прокалили. Что получилось в результате реакции? Дайте ответ, обосновав его уравнениями реакций. (См. Ответ).
Окислы углерода
Известны два окисла углерода, в которых он проявляет различные степени окисления: СО и СО2.
Окись углерода (II) СО, или, как ее называют, угарный газ, представляет собой бесцветный газ, не имеющий запаха. Температура кипения —191,5º.
Она немного легче воздуха и крайне ядовита. Ядовитость окиси углерода объясняется тем, что в соединении с гемоглобином крови, с которой она вступает в контакт при попадании в легкие.
Она образует карбоксигемоглобин, который является прочным соединением, не обладающим способностью вступать в реакцию с кислородом.
Таким образом, гемоглобин крови выводится из строя, и при сильном отравлении человек может погибнуть от кислородного голодания.
Окись углерода может проникнуть в помещение, отапливаемое печами, в том случае, если слишком рано закрывается дымоход и не успевшая сгореть окись углерода попадает в жилое помещение.
Химические свойства окиси углерода весьма разнообразны.
Это горючий газ, который легко сгорает голубым пламенем в кислороде и на воздухе с образованием двуокиси углерода:
2СО + О2 = 2СО2
Углерод в этой реакции окисляется, переходя из С+2 в С+4, т. е. проявляет восстановительные свойства. Следовательно, окись углерода можно применять как восстановитель.
Действительно, окисью углерода можно восстанавливать металлы из окислов:
FeO + СО = СО2 + Fe
Следует отметить также, что окись углерода принадлежит к числу несолеобразующих окислов.
➡️11. Элемент свинец Рb, относящийся также к главной подгруппе IV группы, может образовывать окисел, в котором проявляет степень окисления +2; углерод также может образовывать окисел, где проявляет такую же степень окисления.
Сравните химические свойства этих двух окислов и иллюстрируйте их уравнениями реакций. (См. Ответ).
Применение окиси углерода
Горючесть окиси углерода, а также восстановительные свойства делают ее весьма ценным топливом и восстановителем во многих производственных процессах.
Особенно в металлургии, поэтому окись углерода специально получают в печах, которые называются газогенераторами (рис. ).
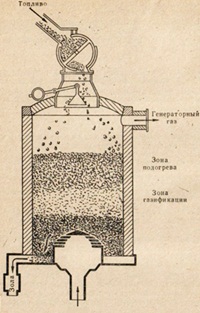
Рис.. Схема газогенератора
Газогенератор представляет собой печь, в которую сверху засыпают кокс. Снизу кокс поджигают, а для поддержания горения кокса снизу же подают воздух.
При соприкосновении кислорода воздуха с раскаленным углем последний сгорает с образованием двуокиси углерода:
С + O2 = СО2
Проходя через последующие соли угля, двуокись углерода восстанавливается до окиси углерода:
СO2 + С = 2СO
В результате из газогенератора выходит генераторный газ следующего состава:
СО + СO2 + N2 (азот воздуха).
Этот газ называется воздушным. Воздушный газ содержит лишь одно горючее вещество СО, а двуокись углерода СО2 и азот являются балластом.
Для того чтобы в газе не было балласта, через генератор пропускают перегретый водяной пар, который, вступая в реакцию с углеродом, образует водяной газ:
С + Н2О ⇄ СО + Н2
Водяной газ балласта не имеет, так как окись углерода и водород горят и являются хорошими восстановителями.
Но при длительном пропускании водяного пара через уголь последний охлаждается и перестает работать.
Для того чтобы этого не происходило, через газогенератор пропускают попеременно воздух и водяной пар, получая при этом смешанный газ.
Генераторные газы широко используются в технике.
➡️12. Какой объем водяного газа получится при пропускании водяного пара через 36 кг угля? (См. Ответ)
13. Напишите уравнения реакций, происходящих при восстановлении окисла железа (III) водяным газом.
14. Как можно разделить газы, входящие в состав воздушного генераторного газа?
15. Воздушный генераторный газ пропустили через раствор гидроокиси кальция. Как изменился состав газовой смеси? Подтвердите уравнениями реакций.
16. Чем отличается смешанный газ от воздушного? Укажите состав компонентов смешанного газа. (См. Ответ).
Газификация угля
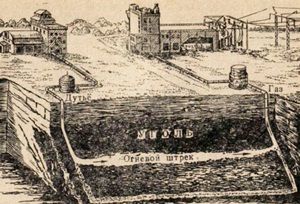
Рис. Схема подземной газификации угля.
Д. И. Менделеевым в 1888 г. был предложен способ подземной газификации угля. Заключается он в следующем.
В угольном пласте (рис.) с поверхности вниз пробуривают две скважины на расстоянии 25—30 м одна от другой. С помощью электронагревателей угольный пласт внизу поджигают.
При пропускании воздуха в дутьевую скважину между ней и газоотводной скважиной прогорает канал, по которому газы идут в газоотводную скважину и по ней поднимаются на поверхность.
В самой нижней части пласта, как в газогенераторе, происходит сгорание угля до двуокиси углерода.
Несколько выше двуокись углерода восстанавливается до окиси углерода, а еще выше под действием тепла разогретого угольного пласта осуществляется сухая перегонка, продукты которой также выводятся через газоотводную скважину.
Продукты сухой перегонки являются весьма ценными. В дальнейшем выходящий газ отделяют от них, после чего его можно использовать по назначению.
Генераторный газ используют в металлургии, в производстве стекла и керамики, в газовых турбинах и двигателях внутреннего сгорания, в быту.
Окись углерода и водород широко применяются в промышленности органического синтеза — при получении аммиака, хлористого водорода, искусственного топлива, моющих средств и т. д.
➡️ 17. Рассчитайте расход угля в газогенераторе, если в результате образовалось 112 л водяного газа. (См. Ответ).
Двуокись углерода СО2
Двуокись углерода СО2 является высшим углеродным окислом, молекулярный вес ее 44 у. е. (она более чем в полтора раза тяжелее воздуха). Температура кипения (возгонки) —78,5°.
Двуокись углерода при сильном охлаждении превращается в твердую снегообразную массу — «сухой лед».
Сухой лед при нормальном давлении в жидкость не переходит, а возгоняется, что представляет большое удобство при хранении скоропортящихся продуктов:
- Во-первых, отсутствует влага.
- Во-вторых, атмосфера двуокиси углерода задерживает рост бактерий и плесневых грибков.
Двуокись углерода — типичный кислотный окисел, обладающий всеми характерными свойствами.
➡️18. Напишите уравнения химических реакций, характеризующих свойства двуокиси углерода как кислотного окисла. (См. Ответ)
Двуокись углерода довольно хорошо растворима в воде: в одном объеме воды растворяется один объем СО2.
При этом происходит взаимодействие ее с водой с образованием весьма нестойкой угольной кислоты:
Н2О + СО2 ⇄ Н2СО3
При повышении давления растворимость двуокиси углерода резко возрастает. На этом основано применение СО2 в изготовлении шипучих напитков.
➡️ 19. Зная закономерности смещения равновесия, укажите, в каком направлении можно сместить равновесие в реакции
СО2+ Н2О ⇄ Н2СО3
а) повышая давление;
б) повышая температуру. (См. Ответ)
Двуокись углерода не поддерживает горения и дыхания и в ее атмосфере животные погибают не от отравления, а от отсутствия кислорода.
Только магний, горящий при очень высокой температуре, может гореть в двуокиси углерода, разлагая ее и тем самым восстанавливая углерод:
2Mg + СО2 = 2MgO + С
В то же время двуокись углерода необходима зеленым растениям для процесса фотосинтеза.
Обогащение атмосферы двуокисью углерода в теплицах, парниках усиливает образование органического вещества растением.
В земной атмосфере содержится 0,04% двуокиси углерода. Небольшое содержание двуокиси углерода в воздухе стимулирует деятельность дыхательного центра.
Обычно двуокись углерода получают, воздействуя на соли угольной кислоты какой-нибудь более сильной кислотой:
СаСО3 + 2НСl = СаСl2 + Н2СO3
Этот процесс осуществляют в лаборатории в аппарате Киппа, заряжая его мрамором и соляной кислотой.

Рис.. Пенный огнетушитель. 1— резервуар с водным раствором соды; 2 —ампула с серной кислотой; 3 — ударник; 4 —железная сетка; 5 — выходное отверстие; б — рукоятка
Аналогичный способ получения двуокиси углерода применяется в так называемых пенных огнетушителях (рис.).
Такой огнетушитель представляет собой стальной баллон, заполненный раствором соды Na2CO3. В этот раствор опущена стеклянная ампула с серной кислотой.
Над ампулой укреплен ударник, которым в случае надобности можно разбить ампулу, и тогда серная кислота начнет взаимодействовать с содой по уравнению:
Na2CO3 + H2SO4 = Na2SO4 + H2CO3
Выделяющаяся при этом в большом количестве двуокись углерода образует обильную пену, которая давлением газа выбрасывается через отверстие в боковой стенке и, покрывая горящий предмет, прекращает доступ к нему кислорода воздуха.
Для промышленных целей двуокись углерода получают при разложении известняка:
СаСO3 = СаО + СО2
Двуокись углерода образуется при горении угля, а также выделяется при брожении сахаров и в других процессах.
➡️ 20. Можно ли пенный огнетушитель наполнить вместо раствора соды раствором другого карбоната, а серную кислоту заменить другой кислотой. Приведите примеры. (См. Ответ)
21. Через йодную воду пропустили смесь газов, состоящую из двуокиси углерода, сероводорода и сернистого газа. Каков состав газовой смеси на выходе? Что содержится в растворе?
22. Какой объем двуокиси углерода получится при сжигании 112 л окиси углерода?
23. Какой объем окиси углерода образуется при окислении 4 молей углерода?
24. Сколько двуокиси углерода можно получить при разложении 250 г известняка, содержащего 20% примесей, если выход СО2 равен 80% от теоретического?
25. Сколько весит 1 м3 смеси газов, состоящей на 70% из окиси углерода и 30% из двуокиси углерода? (См. Ответ).
Угольная кислота и ее соли
Двуокись углерода является ангидридом угольной кислоты. Угольная кислота Н2СО3 сама по себе весьма непрочное вещество.
Она существует только в водных растворах.
При попытке выделить ее из этих растворов она легко распадается на воду и двуокись углерода:
H2CО3 ⇄ Н2О + СО2
H2CО3 ⇄ H+ + HCO—3 ⇄ 2H+ + СО23—
Угольная кислота является очень слабым электролитом; тем не менее, будучи двухосновной, она образует два ряда солей:
- Средние — карбонаты.
- Кислые — бикарбонаты.
Углекислые соли интересны тем, что при действии на них кислоты выделяется двуокись углерода:
К2СО3 + 2НСl = 2КСl + Н2СО3
Н2СО3 ⇄ СО2 + Н2О
➡️26. Приведенное уравнение напишите в ионной форме, а также приведите еще два уравнения реакций, иллюстрирующих действие кислот на карбонаты.
27. Напишите уравнение реакции действия соляной кислоты на бикарбонат магния в молекулярной и ионной формах. (См. Ответ).
Карбонаты и бикарбонаты
При обработке двуокисью углерода и водой карбонаты превращаются в бикарбонаты.
При нагревании происходит обратное превращение:
СаСО3 + СО2 + Н2О (обычные условия) ⇄ Са(НСО3)2 (нагревание)
Переход нерастворимого карбоната в растворимый бикарбонат приводит к вымыванию карбоната из земной коры, в результате чего образуются пустоты — пещеры.
Карбонаты большей частью в воде нерастворимы, за исключением карбонатов щелочных металлов и аммония. Бикарбонаты растворимы лучше.
Среди карбонатов особого внимания заслуживает карбонат кальция СаСО3, встречающийся в трех видах в виде:
- Мрамора.
- Известняка.
- Мела.
Кроме того, в соединении с карбонатом магния он входит в состав горной породы доломита MgCО3 · CaCО3.
Несмотря на одинаковый химический состав, физические свойства этих пород совершенно разные.
Мрамор — твердое, кристаллическое вещество магматического происхождения. Он постепенно выкристаллизовался внутри остывающей магмы.
Часто мрамор бывает окрашен примесями в различные цвета.
Мрамор очень хорошо полируется и поэтому широко используется как отделочный материал для облицовки строительных сооружений и в скульптуре.
Известняк — осадочная порода органического происхождения. Нередко в известняке можно обнаружить остатки древних животных, главным образом моллюсков в известковых раковинах.
Иногда они бывают довольно крупными, а иногда видны лишь под микроскопом. За миллионы лет известняк уплотнился и стал настолько твердым, что его применяют как строительный материал.
Но в настоящее время он постепенно вытесняется более дешевыми, легкими и удобными искусственными материалами. Известняк используется главным образом для получения извести.
Мел — мягкая осадочная порода белого цвета. Применяется в строительстве для побелки.
При изготовлении зубного порошка мел сначала растворяют в кислоте, а затем снова осаждают, так как в природном веществе попадаются мельчайшие твердые частицы кремнезема, которые могут поцарапать зубную эмаль.
Бикарбонат кальция Са(НСО3)2 в природе встречается в растворенном состоянии. Образуется при действии воды в сочетании с двуокисью углерода на известняк.
Присутствие этой соли придает воде временную (карбонатную) жесткость.
Исключительный интерес представляет сода Na2CО3, встречающаяся иногда в природе в так называемых содовых озерах.
Но в настоящее время добывание соды из природных источников вытесняется более дешевым искусственным получением этого продукта.
Если сода содержит кристаллизационную воду, то она называется кристаллической содой Na2CО3 · 10Н2О, если же не содержит ее, то кальцинированной содой.
Сода очень широко применяется в мыловаренной, текстильной, бумажной и стекольной отраслях промышленности.
Двууглекислая сода, или бикарбонат натрия, или питьевая сода, NaHCО3 применяется при выпечке кондитерских изделий как разрыхлитель теста, а также в медицине при повышенной кислотности желудка, изжоге, диабете и т. д.
Карбонат калия K2CO3, или поташ, как и сода, применяется в мыловаренной промышленности и в производстве тугоплавкого стекла.
Следует отметить, что углерод образует так называемые органические соединения, количество и разнообразие которых далеко превосходят соединения всех остальных элементов, вместе взятых.
Детальное изучение соединений углерода выделено в самостоятельную область, называемую органической химией.
➡️28. Как отличить друг от друга представленные в твердом виде карбонат натрия, сульфат натрия, нитрат натрия? (См. Ответ)
29. В одну фарфоровую чашку поместили карбонат кальция, в другую — нитрат калия, в третью — хлорид натрия и начали прокаливать, забыв отметить, в какой чашке какая соль.
Как можно, наблюдая процесс прокаливания и изучив продукты реакции, распознать взятые соли?
30. Как осуществить ряд превращений:
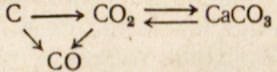
31. Каким образом в природе происходит превращение карбоната кальция в бикарбонат?
32. 2 кг карбоната кальция подвергли прокаливанию. Вес остатка после прокаливания оказался равным 1 кг 800 г. Какой процент карбоната подвергся разложению?
33. Как освободить карбонат кальция от примесей нитрата кальция?
34. Как, имея в своем распоряжении только соляную кислоту, распознать карбонат бария, сульфит бария и сульфат бария?
35. Окисью углерода, полученной из 5 кг угля, восстановили окись железа (III). Сколько железа при этом получено? (См. Ответ).
Круговорот углерода в природе
Углерод — жизненно важный элемент для животных и растений. Растения, используя двуокись углерода воздуха и энергию солнца, создают органические вещества.
Травоядные животные, питающиеся растениями, используя эти уже готовые вещества, в свою очередь служат пищей для хищников.
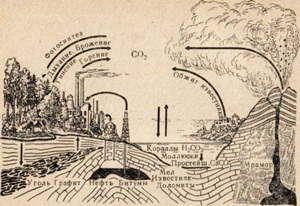
Рис.. Круговорот углерода в природе
Растения и животные, отмирая, гниют, окисляясь и частично превращаясь в двуокись углерода, которая снова потребляется растениями, частично же постепенно разлагаются в почве, образуя разные виды топлива.
При горении топлива выделяется двуокись углерода, которая поступает в атмосферу и потребляется растениями (рис. ).
Такой круговорот может осуществляться только благодаря процессу фотосинтеза.
Вывод
Углерод занимает уникальное место в периодической таблице как элемент с выдающимися физическими и химическими свойствами.
Его способность образовывать ковалентные связи делает его основой органической химии и жизни в целом.
Структурные разновидности — алмаз, графит и аморфный углерод — показывают многообразие форм, в которых углерод может существовать, каждая из которых имеет свои уникальные свойства и области применения.
Алмаз, с его исключительной твердостью и стабильностью, используется в технологии и ювелирном деле, тогда как графит благодаря своей мягкости и проводимости находит применение в электронике и повседневных инструментах.
Эти различные модификации подчеркивают особую роль углерода в науке и промышленности.
Кроме того, его многообразие позволяет углероду участвовать в ряде химических реакций, делая его важным элементом для исследователей и изобретателей.
Изучение углерода и его соединений открывает новые горизонты для будущих технологий и устойчивого развития, подтверждая его статус ключевого элемента на нашей планете.


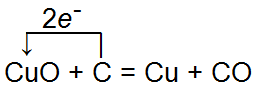
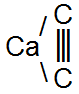
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.