
Содержание страницы
Кремний физические и химические свойства
Химический знак кремния Si, атомный вес 28,086, заряд ядра +14. Кремний, как и углерод, располагается в 14-й группе (устаревшая классификация: главной подгруппе IV группы, в третьем периоде).
Это аналог углерода.
Электронная конфигурация электронных слоев атома кремния:
1s22s22p63s23p2
Строение внешнего электронного слоя:
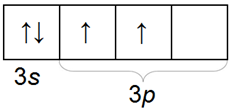
Структура внешнего электронного слоя аналогична структуре атома углерода.
Кремний встречается в виде двух аллотропных видоизменений — аморфного и кристаллического.
Аморфный кремний — порошок буроватого цвета, обладающий несколько большей химической активностью, чем кристаллический.
При обычной температуре реагирует с фтором:
Si + 2F2 = SiF4
при 400° — с кислородом:
Si + O2 = SiO2
в расплавах — с металлами:
2Mg + Si = Mg2Si
Кремний свойства
Кристаллический кремний — твердое хрупкое вещество с металлическим блеском. Он обладает хорошей тепло- и электропроводностью, легко растворяется в расплавленных металлах, образуя сплавы.
Сплав кремния с алюминием называется силумином, сплав кремния с железом — ферросилицием. Плотность кремния 2,4. Температура плавления 1415°, температура кипения 2360°.
Кристаллический кремний — вещество довольно инертное и в химические реакции вступает с трудом.
С кислотами, несмотря на хорошо заметные металлические свойства, кремний не реагирует, а со щелочами вступает в реакцию, образуя соли кремниевой кислоты и водород:
Si + 2КОН + Н2О = K2SiO2 + 2H2
➡️ 36. В чем сходство и в чем различие электронных структур атомов кремния и углерода?
37. Как объяснить с точки зрения электронной структуры атома кремния, почему металлические свойства более характерны для кремния, чем для углерода?
38. Перечислите химические свойства кремния. (См. Ответ)
Кремний в природе Двуокись кремния
В природе кремний распространен очень широко. Примерно 25% земной коры приходится на кремний. Значительная часть природного кремния представлена двуокисью кремния (песок) SiO2.
В очень чистом кристаллическом состоянии двуокись кремния встречается в виде минерала, называемого горным хрусталем.
Двуокись кремния и двуокись углерода по химическому составу являются аналогами, однако двуокись углерода — это газ, а двуокись кремния — твердое вещество.
В отличие от молекулярной кристаллической решетки СO2 двуокись кремния SiO2 кристаллизуется в виде атомной кристаллической решетки.
Каждая ячейка которой представляет собой тетраэдр с атомом кремния в центре и атомами кислорода по углам.
Это объясняется тем, что атом кремния имеет больший радиус, чем атом углерода, и вокруг него могут разместиться не 2, а 4 кислородных атома.
Различием в строении кристаллической решетки объясняется различие свойств этих веществ.
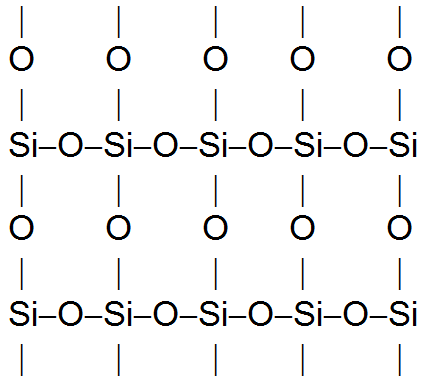
На рис. показаны внешний вид кристалла природного кварца, состоящего из чистой двуокиси кремния, и ее структурная формула.
Рис. Структурная формула двуокиси кремния.
Кристаллическая двуокись кремния наиболее часто встречается в виде песка, который имеет белый цвет, если не загрязнен глинистыми примесями желтого цвета.
Помимо песка, двуокись кремния часто встречается в виде очень твердого минерала — кремния (гидратированная двуокись кремния).
Кристаллическая двуокись кремния, окрашенная в различные примеси, образует драгоценные и полудрагоценные камни — агат, аметист, яшму.
Почти чистая двуокись кремния встречается также в виде кварца и кварцита. Свободной двуокиси кремния в земной коре 12%, в составе различных горных пород — около 43%.
В общей сложности более 50% земной коры состоит из двуокиси кремния.
Кремний входит в состав самых различных горных пород и минералов — глины, гранитов, сиенитов, слюд, полевых шпатов и пр.
Твердая двуокись углерода, не плавясь, возгоняется при —78,5°. Температура плавления двуокиси кремния около 1.713°. Она весьма тугоплавка. Плотность 2,65.
Коэффициент расширения двуокиси кремния очень мал. Это имеет очень большое значение при применении посуды из кварцевого стекла.
В воде двуокись кремния не растворяется и с ней не реагирует, несмотря на то, что это кислотный окисел и ему соответствует кремниевая кислота H2SiO3.
Двуокись углерода в воде, как известно, растворима. С кислотами, кроме плавиковой кислоты HF, двуокись кремния не реагирует, со щелочами дает соли.

Рис. Кристалл природного кварца.
При накаливании двуокиси кремния с углем происходит восстановление кремния, а затем его соединение с углеродом и образование карборунда по уравнению:
SiO2 + 2С = SiC + СО2.
Карборунд обладает высокой твердостью, к кислотам устойчив, а щелочами разрушается.
➡️ 39. По каким свойствам двуокиси кремния можно судить о ее кристаллической решетке? (См. Ответ)
40. В виде каких минералов двуокись кремния встречается в природе?
41. Что такое карборунд? (См. Ответ)
Кремниевая кислота. Силикаты
Кремниевая кислота H2SiO3 является кислотой очень слабой и малоустойчивой.
При нагревании она постепенно разлагается на воду и двуокись кремния:
H2SiO3 = H2O + SiO2
В воде кремниевая кислота практически нерастворима, но может легко давать коллоидные растворы.
Кремниевая кислота образует соли, которые называются силикатами. Силикаты широко встречаются в природе.
Природные силикаты — это довольно сложные вещества.
Состав их обычно изображается как соединение нескольких окислов.
Если в состав природных силикатов входит окись алюминия, они называются алюмосиликатами.
Таковы белая глина, (каолин) Al2O3 · 2SiO2 · 2H2O, полевой шпат К2O · Al2O3 · 6SiO2, слюда К2O · Al2O3 · 6SiO2 · 2Н2O.
Многие природные силикаты в чистом виде являются драгоценными камнями, например аквамарин,топаз, изумруд и др.
Из искусственных силикатов следует отметить силикат натрия Na2SiO3 — один из немногих растворимых в воде силикатов.
Его называют растворимым стеклом, а раствор — жидким стеклом.
Силикаты широко применяются в технике. Растворимым стеклом пропитывают ткани и древесину для предохранения их от воспламенения.
Жидкое стекло входит в состав огнеупорных замазок для склеивания стекла, фарфора, камня.
Силикаты и алюмосиликаты являются основой в производстве стекла, фарфора, фаянса, цемента, бетона, кирпича и различных керамических изделий. В растворе силикаты легко гидролизуются.
➡️ 42. Что такое алюмосиликаты? Чем они отличаются от силикатов?
43. Что такое жидкое стекло и для каких целей оно применяется? (См. Ответ)
Стекло
Сырьем для производства стекла являются сода Na2CO3, известняк СаСO3 и песок SiO2.
Все составные части стеклянной шихты тщательно очищают, смешивают и сплавляют при температуре около 1400°. В процессе сплавления протекают следующие реакции:
Na2CO3 + SiO2= Na2SiO3 + CO2↑
CaCO3 + SiO2 = CaSiO3+ CO2↑
Фактически в состав стекла входят силикаты натрия и кальция, а также избыток SO2, поэтому состав обычного оконного стекла: Na2O · CaO · 6SiO2.
Стеклянную шихту нагревают при температуре 1500° до тех пор, пока полностью не удалится двуокись углерода. Затем стекло охлаждают до температуры 1200°, при которой оно становится вязким.
Как всякое аморфное вещество, стекло размягчается и затвердевает постепенно, поэтому оно является хорошим пластическим материалом.
Вязкую стеклянную массу пропускают через щель, в результате чего образуется стеклянный лист.
Горячий стеклянный лист вытягивают валками, доводя до определенных размеров и постепенно охлаждая током воздуха.
Затем его обрезают по краям и разрезают на листы определенного формата.
➡️ 44. Приведите уравнения реакций, протекающих при получении стекла, и состав оконного стекла. (См. Ответ)
Стекло — вещество аморфное, прозрачное, в воде практически нерастворимо, но если измельчить его в мелкую пыль и смешать с небольшим количеством воды, то в полученной смеси с помощью фенолфталеина можно обнаружить щелочь.
При длительном хранении щелочей в стеклянной посуде избыток SiO2 в стекле очень медленно реагирует со щелочью и стекло постепенно утрачивает прозрачность.
Стекло стало известно людям более чем за 3000 лет до нашей эры.
В древности получали стекла почти такого же состава, как и в настоящее время, но древние мастера руководствовались лишь собственной интуицией.
В 1750 г. М. В. Ломоносов сумел разработать научные основы получения стекла. За 4 года М. В. Ломоносов собрал много рецептов изготовления разных стекол, особенно цветных.
На построенной им стекольной фабрике было изготовлено большое количество образцов стекла, которые сохранились до наших дней.
В настоящее время используются стекла разного состава, обладающие различными свойствами.
Кварцевое стекло состоит из почти чистой двуокиси кремния и выплавляется из горного хрусталя.
Его очень важной особенностью является то, что коэффициент расширения у него незначительный, почти в 15 раз меньше, чем у обычного стекла.
Посуду из такого стекла можно раскалить докрасна в пламени горелки и после этого опустить в холодную воду; при этом никаких изменений со стеклом не произойдет.
Кварцевое стекло не задерживает ультрафиолетовых лучей, а если окрасить его никелевыми солями в черный цвет, то оно будет задерживать все видимые лучи спектра, но для ультрафиолетовых лучей останется прозрачным.
На кварцевое стекло не действуют кислоты и вода, но щелочи его заметно разъедают. Кварцевое стекло более хрупко, чем обычное.
Лабораторное стекло содержит около 70% SiО2, 9% Na2О, 5% К2О 8% СаО, 5% Аl2O3, 3% В2O3 (состав стекол приводится не для запоминания).
В промышленности находят применение стекла иенское и пирекс.
Иенское стекло содержит около 65% SiО2, 15% В2O3, 12% ВаО, 4% ZnO, 4% Аl2O3.
Оно прочно, устойчиво к механическим воздействиям, имеет малый коэффициент расширения, устойчиво к щелочам.
Стекло пирекс содержит 81% SiO2, 12% В2O3, 4% Na2O, 2% Аl2O3, 0,5% As2O3, 0,2% К2O, 0,3% СаО.
Оно обладает такими же свойствами, как иенское стекло, но в еще большей степени, особенно после закалки, зато менее устойчиво к щелочам.
Из стекла пирекс изготовляют предметы домашнего обихода, подвергающиеся нагреванию, а также детали некоторых промышленных установок, работающие при низких и высоких температурах.
Разные качества стеклу придают некоторые добавки.
Например, примеси окислов ванадия дают стекло, полностью задерживающее ультрафиолетовые лучи.
Получают также и стекло, окрашенное в различные цвета. Еще М. В. Ломоносов изготовил несколько тысяч образцов цветного стекла разной окраски и оттенков для своих мозаичных картин.
В настоящее время методы окраски стекла детально разработаны.
Соединения марганца окрашивают стекло в фиолетовый цвет, кобальта — в синий.
Золото, распыленное в массе стекла в виде коллоидных частиц, придает ему рубиновую окраску и т. д.
Свинцовые соединения придают стеклу блеск, подобный блеску горного хрусталя, поэтому оно называется хрустальным. Такое стекло легко поддается обработке, огранке.
Изделия из него очень красиво преломляют свет. При окраске этого стекла различными добавками получается цветное хрустальное стекло.
Если расплавленное стекло смешать с веществами, которые при разложении образуют большое количество газов, то последние, выделяясь, вспенивают стекло, образуя пеностекло.
Такое стекло очень легкое, хорошо обрабатывается, является прекрасным электро- и тепло-изолятором. Оно было впервые получено проф. И. И. Китайгородским.
Вытягивая из стекла нити, можно получить так называемое стекловолокно.
Если пропитать уложенное слоями стекловолокно синтетическими смолами, то получается очень прочный, не поддающийся гниению, прекрасно обрабатывающийся строительный материал, так называемый стеклотекстолит.
Интересно, что чем тоньше стекловолокно, тем выше его прочность. Стекловолокно также применяется для изготовления спецодежды.
Стеклянная вата является ценным материалом, через который можно фильтровать сильные кислоты и щелочи, не фильтрующиеся через бумагу.
Кроме того, стеклянная вата является хорошим теплоизолирующим веществом.
➡️ 44. От чего зависят свойства стекол разных видов? (См. Ответ)
Керамика
Из алюмосиликатов особенно важна белая глина — каолин, являющаяся основой для получения фарфора и фаянса.
Производство фарфора — чрезвычайно древняя отрасль хозяйства. Родина фарфора — Китай. В России фарфор был получен впервые в XVIIIв. Д, И. Виноградовым.
Сырьем для получения фарфора и фаянса, помимо каолина, служат песок и вода.
Смесь каолина, песка и воды подвергают тщательному тонкому размолу в шаровых мельницах, затем отфильтровывают избыток воды и хорошо вымешанную пластичную массу направляют на формовку изделий.
После формовки изделия подвергают сушке и обжигу в туннельных печах непрерывного действия, где их сначала разогревают, затем обжигают и, наконец, охлаждают.
После этого изделия проходят дальнейшую обработку — покрытие глазурью, нанесение рисунка керамическими красками. После каждой стадии изделия обжигают.
В результате фарфор получается белым, гладким и блестящим. В тонких слоях он просвечивает. Фаянс порист и не просвечивает.
Из красной глины формуют кирпичи, черепицу, глиняную посуду, керамические кольца для насадки в поглотительных и промывных башнях разных химических производств, цветочные горшки.
Их также обжигают, чтобы они не размягчались водой, стали механически прочными.
Цемент. Бетон
Соединения кремния служат основой для получения цемента — вяжущего материала, незаменимого в строительстве. Сырьем для получения цемента являются глина и известняк.
Эту смесь обжигают в огромной наклонной трубчатой вращающейся печи, куда непрерывно загружают сырье.
После обжига при 1200—1300° из отверстия, расположенного на другом конце печи, непрерывно выходит спекшаяся масса — клинкер.
После размола клинкер превращается в цемент. В состав цемента входят главным образом силикаты.
Если цемент смешать с водой до образования густой кашицы, а затем оставить на некоторое время на воздухе, то вода вступит в реакцию с веществами цемента, образуя кристаллогидраты и другие твердые соединения, что приводит к затвердеванию («схватыванию») цемента.
Такой цемент уже не переводится в прежнее состояние, поэтому до употребления цемент стараются беречь от воды.
Процесс твердения цемента является длительным, и настоящую прочность он приобретает лишь через месяц
Правда, существуют разные сорта цемента. Рассмотренный нами обычный цемент называется силикатным, или портландцементом.
Из глинозема, известняка и двуокиси кремния изготовляют быстро твердеющий глиноземистый цемент.
Если смешать цемент со щебнем или гравием, то получается бетон, являющийся уже самостоятельным строительным материалом. Щебень и гравий называются наполнителями.
Бетон обладает высокой прочностью и выдерживает большие нагрузки. Он водостоек, огнестоек. При нагревании почти не теряет прочности, так как теплопроводность его очень мала.
Бетон морозостоек, ослабляет радиоактивные излучения, поэтому его используют как строительный материал для гидротехнических сооружений, для защитных оболочек ядерных реакторов.
Бетоном обмуровывают котлы.
Если смешать цемент с пенообразователем, то образуется пронизанный множеством ячеек пенобетон.
Такой бетон является хорошим звуко-изолятором и еще меньше, чем обычный бетон, проводит тепло.
Если бетоном залить стальной каркас, то получится железобетон. Каркас называется арматурой. Из железобетона изготовляют блоки и панели для домостроения, трубы, мосты, перекрытия, шпалы.
➡️ 46. Составьте и заполните следующую таблицу. (См. Ответ)
Силикатная промышленность
| Стекло | Керамика | Цемент, бетон | ||||||
| Сырье | Виды | Применение | Сырье | Виды | Применение | Сырье | Виды | Применение |
Статья на тему Кремний химические свойства

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.