Вода это уникальное вещество, которое состоит из молекул, каждая из которых содержит один атом кислорода и два атома водорода.
Она играет ключевую роль в жизни всех организмов на планете, будучи не только основным составным элементом клеток, но и необходима для проведения многих жизненно важных процессов.
Вода имеет ряд физических свойств, которые делают ее уникальным веществом.
Например, она обладает высокой теплоемкостью, что позволяет ей служить стабилизатором температуры на планете и в организмах живых существ.
Кроме того, вода обладает способностью растворять многие вещества, что позволяет ей служить средой для химических реакций и транспортировать питательные вещества и отходы в организмах.

Что такое вода
Это важнейшие производные кислорода которые являются его соединения с водородом — вода Н2О и перекись водорода Н2О2.
Рассмотрим оба соединения и в первую очередь наиболее распространенное из них — воду.
О строении молекулы воды и полярном характере связи между атомами водорода и кислорода говорилось в физические свойства воды.
Молекулярный вес воды равен 18. В газообразном состоянии (в виде пара) вода легче воздуха, средний молекулярный вес которого 29.
Однако в обычных условиях вода — это жидкость, которая обладает значительно большей плотностью.
Это объясняется тем, что молекулы воды объединены (ассоциированы) между собой дополнительно особым видом связи — водородной связью.
Водородная связь в молекуле воды
Водородная связь названа так потому, что обязательно требует наличия иона водорода. В молекуле воды, где общие электронные пары сильно смещены к кислороду, атомы водорода практически лишены электронов и представляют собой оголенное ядро.
Такое ядро (у водорода это протон) притягивается электронными оболочками атомов кислорода соседних молекул, и образуется связь между молекулами.
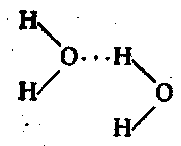
В отличие от остальных видов химической связи, обозначаемых в структурных формулах черточками, водородная связь обозначается пунктиром:
Водородная связь отличается от химической.
Она намного слабее последней. Однако водородную связь нельзя считать просто межмолекулярным сцеплением, она намного прочнее.
Водородная связь может возникать не только между молекулами воды. Она часто встречается в органических веществах.
Вопросы по теме вода
- Объясните механизм образования водородной связи.
- Перечислите известные вам типы химической связи.
- По какому типу химической связи построена молекула воды?
- Чем вызвана ассоциация молекулы воды? (См. Ответ)
По физическим свойствам вода — это жидкость, не имеющая цвета, вкуса и запаха.
Наибольшую плотность (1 г/см3) вода имеет при 4°.
При понижении и повышении температуры плотность воды уменьшается (поэтому лед плавает на воде).
Температура плавления льда 0° и кипения воды 100° являются основными точками стоградусной шкалы температур.
Вода является прекрасным растворителем жидкостей, газов и твердых веществ. Вода очень плохо проводит электрический ток.
Удельная теплоемкость воды самая большая среди всех твердых и жидких веществ.
Температура воды при замерзании напрямую зависит от растворенных в ней солей.
Вода в природе
Вода очень широко распространена в природе. Примерно 3/4 поверхности земного шара заняты водой.
Это океаны, моря, наземные текучие пресные воды, озера, пресные и соленые, ледники, подземные воды, водяной пар.
Постоянно в большем или меньшем количестве присутствующий в атмосфере, а также кристаллизационная вода, входящая в состав кристаллогидратов.
Поскольку вода является хорошим растворителем, в природных водах всегда содержатся в растворенном виде разнообразные вещества.
Морская вода содержит в растворенном состоянии множество различных солей, в том числе хлорид натрия NaCl, сульфат магния MgSO4 и др., которые придают ей горько-соленый вкус.
Подземные воды, протекающие по горным породам, растворяют различные вещества, и эти растворы, выходящие на поверхность, называются минеральными источниками.
Особенно много минеральных источников на Кавказе. С воды углекислых источников улучшают пищеварение и кровообращение.
В этих водах растворен под давлением углекислый газ. Сернистые воды в Мацесте и Пятигорске бывают холодными и горячими, содержат сульфиды и сероводород.
Сероводородные ванны понижают кровяное давление, улучшают работу сердца. Железистые воды Железноводска, Липецка рекомендуются для принятия внутрь при малокровии.
Известковые воды Кисловодска применяются при заболеваниях почек, воды теплых источников Забайкалья и Туркестана используются в натуральном виде для ванн при общей слабости организма, нервных заболеваниях, кожных болезнях и пр.
Если подземные воды находятся вблизи очагов вулканической деятельности, то вода выходит на поверхность горячей в виде так называемых гейзеров.
Считают, что в глубинах земной коры имеется огромное количество горячей воды. Ее можно использовать как очень дешевый источник тепловой энергии.
С воды началась жизнь на земле которую мы знаем сейчас, является средой для жизни водных организмов, но она; необходима решительно всем живым организмам, которые без воды не могут существовать.
Протоплазма любой клетки представляет собой коллоидный раствор белка в воде. В составе тела человека находится 65% воды.
Если организм человека потеряет 20% воды, то изменения, происходящие в клетках, становятся необратимыми, и человек погибает.
Без пищи человек может прожить 30-40 суток, а без воды,— не более 7 суток. Жизнь растений без воды также невозможна.
Вода для зеленых растений является необходимым компонентом для фотосинтеза.
Вопросы по теме вода в природе
- В какой состоянии и где вода встречается в природе? Запишите это в тетрада.
- Что представляют собой минеральные источники состав состав их воды, каково применение в медицине? (См. Ответ)
Химические свойства воды
Вода является безразличным окислом. Вода — чрезвычайно слабый электролит, диссоциирующий по схеме:
Н2О ⇄ Н+ + ОН—
Некоторые наиболее активные металлы (Na, К, Са, Ва, Аl) могут вытеснять из воды водород:
2Na + 2Н2O = 2NaOH + H2↑
2Na + 2Н+ + 2OH— = 2Na+ + 2OН— + H2↑
2Na + 2H+ = 2Na+ + H2↑
Раскаленное железо разлагает воду с выделением водорода и образованием окалины:
3Fe + 4Н2O (перегретый пар) = Fe3O4 + 4Н2
Элементы, обладающие более сильными, чем кислород, окислительными свойствами.
Например хлор, вытесняют кислород из воды:
Cl02 + H2O-2 = 2HCl-1 + [O0]
Cl02 + 2е— → 2Сl-1
О-2 — 2e— → O0
Раскаленный уголь разлагает воду, образуя водяной газ, представляющий собой в основном смесь водорода с окисью углерода:
С + Н2О = СО + Н2
Вода может реагировать с основными и кислотными окислами, образуя основания и кислоты.
Выделение тепла при растворении в воде едких щелочей и серной кислоты объясняется также происходящими между водой и этими веществами химическими реакциями присоединения воды.
Вода может вступать в реакцию с солями, образуя кристаллогидраты.
Например, медный купорос, имеющий голубой цвет, является продуктам соединения белого сульфата меди с водой по-уравнению:
CuSO4 + 5H2O = СuSO4 = 5H2O + Q
Вода является веществом, весьма стойким химически, однако может разлагаться под действием электрического тока.
Вода активно вступает в реакции гидролиза со сложными неорганическими и органическими веществами.
Вопросы по теме химические свойства воды
- Почему воду относят к числу безразличных окислов? (См. Ответ)
- Вполне ли правильно выражение «натрий растворяется в воде»?
- Напишите уравнения реакций взаимодействия с водой основных и кислотных окислов. С какими из них вода не реагирует?
- Для какой дели воду подвергают электролизу?
- Вода реагирует с солями с образованием кристаллогидратов. Напишите уравнение реакции образования кристаллогидрата. Какого иного характера взаимодействие возможно между водой и солями?
- В сосуд с 200 г воды поместили 9,2 г натрия. Какое вещество при этом образовалось? Растворимо ли оно? Если растворимо, то какова его процентная концентрация в полученном растворе?
- К 50 г 30% серной кислоты добавили 5 г серного ангидрида. Какой стала концентрация серной кислоты?
- Среди перечисленных в свойств воды укажите те, которые можно использовать для получения водорода.
- Какой объем водорода может быть получен при взаимодействии 5 кг железа с перегретым паром, если 10% веса железа приходится на окалину, а 20% полученного водорода теряются?
- Сколько окиси меди можно восстановить водородом, полученным в предыдущей задаче? (См. Ответ)
Вода, входящая в состав кристаллов, называется кристаллизационной водой. Она химически связана с веществом и придает кристаллу соответствующие свойства.
Например медный кynopoc, CuSО4 · 5H2O в виде кристаллогидрата с пятью молекулами воды имеет ярко-голубую окраску, которую он теряет при прокаливании вследствие удаления кристаллизационной воды.
Природный гипс CaSО4 · 2H2О при слабом нагревании отделяет одну молекулу воды, превращаясь в соединение состава 2CaSО4 · H2O, называемое полуводным гипсом.
Этот гипс обладает способностью «схватываться», т. е. при смешивании с водой присоединять к себе недостающую молекулу воды и затвердевать, образуя двуводный гипс CaSО4 · 2H2О:
2CaSО4 · H2O + 3H2O = 2(CaSO4 · 2H2O)
Эта реакция нашла широкое применение в медицине при наложении гипсовых повязок.
Однако если гипс прокалить до полного удаления воды:
CaSO4 · 2H2O2= CaSO4 + 2Н2O

то реакция становится необратимой и вода к сульфату кальция больше не присоединяется.
Рис. Обезвоживание медного купороса 1- медный купорос 2- выделяемая при нагревании вода
Что такое кристаллогидраты
Кристаллогидраты — это химические соединения соли с водой. Их причисляют к комплексным соединениям. Можно назвать еще много кристаллогидратов, например глауберову соль:
Na2SО4 · 10H2O, железный купорос FeSО4 · 7H2Ои др.
- Сколько нужно взять воды и кристаллогидрата Na2SO4 · 10H2O, чтобы приготовить 200 г 3% раствора сульфата натрия? (См. Ответ)
- В лаборатории для абсолютирования спирта применяют безводный сульфат меди, с которым кипятят спирт, пока сульфат меди не приобретет голубую окраску. Какая реакция происходит При этом? Насколько увеличится вес 25 г сульфата меди, если считать, что 75% сульфата превратилось в медный купорос?
- Сколько процентов воды содержалось в спирте, если абсолютированию подверглось 150 г спирта.
20 a FеSО4 · 7H2O растворили 180 г воды. Какова концентрация полученного раствора? - Что такое двуводный гипс, полуводный гипс? Какое применение они находят в медицине?
Какая вода называется кристаллизационной? (См. Ответ)
Способы очистки природных вод
Природная вода не всегда удовлетворяет всем требованиям, которые к ней предъявляются человеком. Поэтому для различных целей вода подвергается разной обработке.
Питьевая вода должна быть частой, прозрачной, без запаха и не содержать болезнетворных бактерий.
Природная вода, предназначенная для питья, поступает на водоочистительные станции городского водопровода, где ока проходит через систему очистных сооружений (рис. 46).
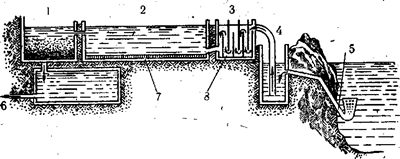
Сначала она проходит через металлические фильтры для очистки от механических примесей, затем поступает в отстойники, где постепенно оседают загрязняющие ее мелкие частицы.
Рис. Система очистных сооружений водоочистительной станции. 1-фильтр; 2-отстойник; 3-смесители; 4 — перекачка; 5 — засос воды; 6 — хлорирование; 7 —осадок; 8 — добавление квасцов.
Для ускорения их оседания в отстойники обычно добавляют коагулянт — вещество, заставляющее взвеси и коллоидные частицы коагулировать и оседать.
В качестве коагулянта применяется хлорид алюминия AlCl3 или сульфат алюминия Al2(SO4)3.
После отстаивания вода фильтруется через песок, костный уголь и тканевые фильтры, после чего в ней остаются растворимые соли и микроорганизмы, среди которых могут оказаться болезнетворные бактерии.
Для их уничтожения в воду добавляют немного хлорной воды в количестве, которое убивает бактерий, но безвредно для человека.
После этого вода поступает в так называемые резервуары чистой воды, где выдерживается некоторое время для того, чтобы полностью проявилось действие хлора.
Очищенная вода по водопроводу поступает к потребителям.
В сельских местностях обычно вода не проходит такой сложной системы очистки, а берется прямо из колодцев или других природных водоемов.
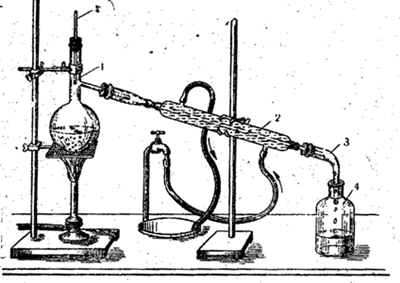
Рис. Прибор для перегонки воды.
1- колба Вюрца с водой; 2-водяной холодильник Либиха: 3 — алонж; 4- сосуд-приёмник для дистиллированной, воды; 5 — термометр.
Такую воду необходимо кипятить, а в случае массовых желудочно-кишечных заболеваний в нее нужно добавлять небольшое количество раствора хлорной извести.
В химических лабораториях и медицине применяется дистиллированная вода. Для полного удаления солей воду перегоняют в так называемых перегонных кубах.
Принцип перегонки воды можно наблюдать на лабораторной установке (рис. выше). Вода кипит в колбе.
Получающийся, пар по газоотводной трубке поступает в водяной холодильник Либиха 2, где пар конденсируется и стекает через алонж 3 в сосуд-приемник 4.
Полученная вода называется дистиллированной. Она совершенно не содержит солей и ее вредно применять для питья. Дистиллятор устроен по тому же принципу (рис. ниже).

Рис. Дистиллятор
- Что такое дистилляция и для каких целей используют дистиллированную воду?
- Какие требования предъявляют к питьевой воде?
- Каким образом можно очистить воду: а) от механических загрязнений; б) от растворенных солей; в) от коллоидных частиц? (См. Ответ)
Перекись водорода
Перекись водорода — более богатый кислородом окисел по сравнению с водой. Формула перекиси H2О2, но это не значит, что в данном соединении кислород одновалентен.
В молекуле перекиси водорода между двумя атомами кислорода имеется одна общая электронная пара.
Соединенные таким образом атомы кислорода содержатся не только в перекиси водорода, но и в любой другой перекиси и называются «перекисной цепочкой»
Наличие перекисной цепочки делает молекулу непрочной.
Действительно, при самых незначительных воздействиях — хранении в освещенном помещении, нагревании, действии катализатора МnО2 — перекись водорода разлагается, превращаясь в воду, с выделением кислорода:
2Н2О2 = 2Н2O + О2
Эта реакция может сопровождаться взрывом.
30% раствор перекиси водорода носит название пергидроля.
При попадании на кожу он может причинить сильные ожоги. Чистая перекись водорода имеет плотность 1,46 г/с3 и температуру замерзания —1,7°.
Раствор перекиси водорода имеет кислую реакцию, что дает основание рассматривать ее как весьма слабую двухосновную кислоту.
Некоторые перекиси металлов, например Na2O2; ВаО2, можно рассматривать не только как окислы, но и как своеобразные соли перекиси водорода.
Из этих соединений можно получить перекись водорода действием более сильной кислоты:
ВаО2 + H2SO4 = BaSO4 + H2O2
О поведении перекиси водорода в окислительно-восстановительных реакциях. При взаимодействии с органическими веществами перекись водорода ведет себя как окислитель.
Безводная перекись водорода вызывает ожоги и самовоспламенение горючих материалов.
При ожогах перекисью водорода на коже появляется характерное белое пятно» а затем может образоваться язва.
Мерой первой помощи, как и при ожогах кислотами, является промывание большим количеством воды.
Перекись водорода применяют как дезинфицирующее средство в медицине для полосканий, промываний и как кровоостанавливающее средство в виде 3% раствора.
Кроме того, ее используют для отбеливания волос, шерсти, шелка, рога и т. д.
Перекись водорода используют также для реставрации картин, написанных свинцовыми белилами, которые постепенно темнеют на воздухе, так как под действием сероводорода воздуха в краске образуется сульфид свинца черного цвета.
Перекись водорода окисляет сульфид свинца в сульфат но схеме:
PbS + H2O2 → PbSO4 + H2O
Такие картины протирают слабым раствором перекиси водорода.
Хранить перекись водорода следует в склянках темного стекла в прохладном помещении, в темноте, чтобы замедлить постоянно идущий распад.
Вопросы по теме перекись водорода
- Приведите примеры реакций, в которых перекись водорода проявляла бы свойства окислителя. (См. Ответ)
- Приведите примеры реакций, в которых перекись водорода проявляла бы свойства восстановителя.
- Где и как следует хранить перекись водорода в лабораторий? Почему?
- Каковы меры первой помощи при ожогах перекисью водорода?
- В присутствии двуокиси марганца из перекиси водорода можно получить кислород. Нарисуйте прибор, в котором можно использовать этот процесс.
- Сколько граммов перекиси бария потребуется для получения 5 молей чистой перекиси водорода?
- Перекись водорода диссоциирует по типу кислот. Напишите уравнение двуступенчатой диссоциации этой кислоты.
- Где и как применяется перекись водорода в как это связано с её свойствами? (См. Ответ)
Воздух
Наша планета окружена воздухом, который необходим для дыхания всем живущим на земле существам. За сутки человек пропускает через свои легкие около 13 000 л воздуха.
Воздушная оболочка земли носит название атмосферы (от слов «атмос» — воздух, «сфайра» — шар). В воздухе содержится 78% (объемных) азота, 21% кислорода, 0,96%
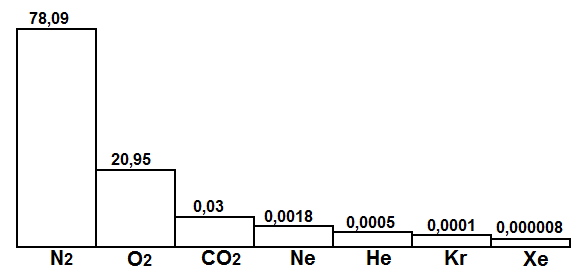
Инертных газов, главным образом аргона и неона, а так же гелия, криптона и ксенона, 0,03—0,04% двуокиси углерода и 0,01% водорода.
Рис. Диаграмма состава воздуха
Состав воздуха приведен на рисунке. Средний молекулярный вес воздуха равен 29 у. е.
Помимо этого, в состав атмосферы входят случайные примеси, а также переменные составляющие — водяной пар, окислы азота, озон.
А также пыль и местные загрязнения воздуха, возникающие иногда при интенсивной работе предприятий в определенном районе, а также при работе транспорта.
Количество пыли в воздухе может быть очень велико, особенно в больших городах. Пыль нарушает прозрачность воздуха и способствует образованию туманов, так как на пылинках конденсируются капельки воды.
В воздухе могут находиться различные микроорганизмы. Среди них могут быть и болезнетворные.
Отсюда ясно, какое значение имеет очистка воздуха в городах, как,важно следить за тем, чтобы воздух не загрязняли промышленные предприятия и транспорт.
Для очистки воздуха внутри помещений применяются специальные аппараты кондиционирования воздуха: его фильтруют, увлажняют до нужного состояния, избавляют от пыли и бактерий и поддерживают наиболее благоприятную температуру.
1 м3 воздуха при 0° весит 1,293 кг, с увеличением высоты плотность воздуха становится меньше. При —193° воздух переходит в жидкое состояние.
Поскольку воздух— это смесь газов с разными температурами кипения, его можно разделить на составные части по температурам кипения или, как говорят, подвергнуть фракционной перегонке.
Широко используется энергия сжатого воздуха, который получают повышением давления атмосферного воздуха с помощью компрессоров.
При вдувании сжатого воздуха в домну подача кислорода увеличивается и горение становится более интенсивным.
Жидкий воздух представляет собой голубоватую мутную жидкость. Голубую окраску придает ему жидкий кислород.
А мутным он бывает потому, что при температуре жидкого воздуха углекислота становится твердой. Если ее отфильтровать, то воздух будет прозрачным.
Под влиянием низкой температуры жидкого воздуха некоторые тела приобретают особые, совершенно новые свойства.
Например, свинец приобретает упругость стали, ртуть становится настолько твердой, что изготовленным из нее молотком можно забивать гвозди, резина становится хрупкой, как стекло, и от удара разбивается на части.
Многие металлы при температуре жидкого воздуха приобретают свойства сверхпроводимости. Если возбудить в металлическом кольце электрический ток, то подключенный к нему гальванометр очень долго будет показывать наличие электрического тока.
Интересно, что большая часть бактерий в жидком воздухе не погибает, а погружается в состояние анабиоза.
Если пропитать жидким воздухом горючий материал, который в обычном воздухе либо не воспламеняется, либо горит очень слабо, например опилки или угольный порошок.
То при поджигании они моментально сгорают с выделением большого количества газов, поэтому жидкий воздух широко применяют при взрывных работах.
Для этого картонные патроны набивают опилками, укладывают во взрывные камеры, пропитывают жидким воздухом и поджигают. Происходит сильный взрыв.
Если взрыв не произошел, то через некоторое время воздух из патрона испаряется, и он снова становится безопасным в отличие от любой другой взрывчатки.
Получают жидкий воздух при высоком давлении и низкой температуре.
Сжатый воздух используется в пневматических приборах и различном пневматическом оборудовании, а так-же при кессонных работах.
Кессон
Кессон — это огромный воздухо- и водонепроницаемый бетонный ящик, внутри которого могут находиться несколько человек.
С одной стороны кессон открыт. Его опускают открытой стороной в воду до самого дна, укрепляют грузом, чтобы он не всплывал, и сжатым воздухом вытесняют из него воду.
Для вытеснения воды давление воздуха в кессоне доводят до 4 атм. При таком давлении воздух в большом количестве растворяется в крови.
При резком уменьшении давления, например при подъеме на поверхность, избыток его быстро выходит из крови в виде пузырьков, которые могут закупорить кровеносные сосуды и даже дойти до сердца.
В тяжелых случаях эта так называемая кессонная болезнь может привести к смертельному исходу.
Поэтому подъем из кессона осуществляется постепенно, чтобы растворенный воздух выходил небольшими порциями.
Вопросы на тему воздух
- Правильно ля называть воздух смесью газов? Дайте обоснованный ответ. (См. Ответ)
- Какой объем воздуха будет израсходован на сжигание 31 г. фосфора.
- Какой объем займут при нормальных условиях 2 кг воздуха?
- Перечислите, где применяется воздух в технике. (См. Ответ)
Список литературы
- Гаврилов Л.Н. «Основы гидрологии».
- Дубенский В.М. «Формирование и очистка воды».
- Зенгин Т.Н. «Химия и технология воды».
- Иванов А.П. «Экология водных систем».
- Колесникова Е.И. «Экономика водных ресурсов».
- Лебесов И.А. «Методы анализа воды».
- Марченко О.В. «Водные ресурсы и их использование».
- Никонов Г.С. «Охрана водных экосистем».
- Овсянникова Л.Д. «Гидрохимия воды».
- Павлов А.М. «Физические свойства воды».
- Романова Н.И. «Подземные воды».
- Сидоров В.П. «Водоснабжение и водоотведение».
- Тихонова Е.С. «Инженерная геология воды».
- Устинов С.Н. «Гидравлика и гидротехника».
- Федоров Д.А. «Климат и водные ресурсы».


Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.