Амины аминокислоты и белки
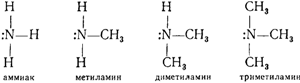
Амины по строению их молекул являются производными аммиака. Их можно рассматривать как продукты замещения одного, двух или всех трех атомов водорода в аммиаке углеводородными радикалами.
Ниже для сравнения приведены формулы аммиака и некоторых аминов:
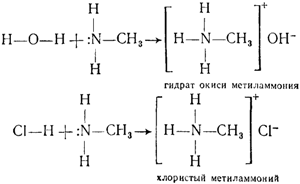
Сходство в строении определяет и сходство свойств. Подобно аммиаку, амины могут присоединять к себе протоны, отнимая их от других молекул. Например, от молекул воды или от молекул кислот:
Об одном из наиболее важных аминов — анилине С6Н5NН2 уже было сказано раньше .
Большое значение в природных процессах имеют аминокислоты, в молекулах которых содержатся аминогруппы —NH2 и карбоксильные группы —СООН.
Примером простейшей аминокислоты может служить амино-уксусная кислота NH2—СН2—СООН. Строение других природных аминокислот можно выразить формулой
NH2—СН—СООН
|
R
где R — углеводородный радикал.
Аминокислоты образуются при гидролизе белков, сложнейших органических соединений, без которых невозможна жизнь.
В состав белков входят углерод, водород, кислород, азот, а часто и другие элементы — сера, фосфор, железо. Молекулярные веса белков очень велики — от 15 000 до нескольких миллионов. Белки содержатся во всех тканях организмов, в крови, костях. Все энзимьи(ферменты) представляют собой сложные белковые вещества. Кожа, волосы, шерсть, перья, рога, копыта, когти образованы белками.
Проблема строения и синтеза белков полностью пока еще не решенаЭ Важные исследования в этой области были проведены Н. Д. Зелинским и его учениками.
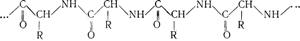
В настоящее время установлено, что молекулы белков построены из большого числа остатков 25—30 различных аминокислот, которые во многих белках связаны так:
Указанную структуру имеют, в частности, белки шелка.
Полученные данные послужили предпосылкой для синтеза новых веществ, имеющих такие же связи между отдельными структурными единицами молекул, как и белки.
Так были, получены синтетические полиамидные волокна — капрон и найлон, по некоторым свойствам превосходящие природный шелк.
Капрон
Является поликонденсатом аминокапроновой кислоты
NH2—СН2—СН2—СН2—СН2—СН2—СООН
Ниже изображена часть молекулы этого вещества: —NH—(СН2)5—СО—NH—(СН2)5—СО—
Найлон или анид
Получается конденсацией двухосновной адипиновой кислоты НООС—(СН2)4—СООН и гексаметилен-диамина NH2—(СН2)6—NH2.
Строение молекулы найлона может быть изображено следующим образом:
[—CO-(CH2)4-CO-NH-(CH2)6-NH—]x
Производство искусственных и синтетических волокон (получивших общее название — химические волокна) относится к тем отраслям химической промышленности, которые в последнее время развивались особенно быстро. Достаточно указать, что мировое производство этих волокон в 1957 г. достигло 2900 тыс. т и составило 25% от общего производства всех видов текстильного волокна.
В Советском Союзе производство искусственного волокна в 1940 г. составляло всего лишь 11 тыс. т. В послевоенные годы производство химических волокон всех видов приобрело значительно большие размеры и в 1959 г. достигло 179 тыс. т.
Развитие промышленности искусственного и химического волокна имеет огромное значение для увеличения производства товаров народного потребления и различных видов промышленной продукции. К концу семилетия 1959—1965 гг. производство химических волокон в нашей стране намечено увеличить в 4 раза.
Вы читаете, статья на тему Амины аминокислоты и белки