Амины это соединения аммиака, в которых один или несколько атомов водорода замешены углеводородными радикалами.
Амины бывают:
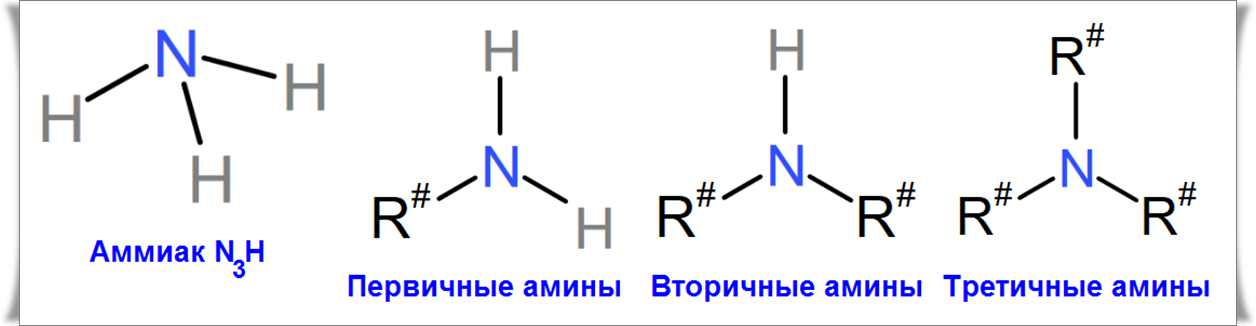
1. Первичными (R—NH2).
2. Вторичными (R2 — NH).
3. Третичными (R3N).
Содержание страницы
- 1. Что такое амины
- 1.1. Простейшие амины
- 1.2. Получение аминов
- 1.3. Анилин
- 1.4. Аминокислоты
- 1.5. Белки
- 1.6. Быстрые ответы?
Что такое амины
Атом азота в аминах находится в sp3-гибридизации, три из них образуют связи с тремя атомами водорода или другими группами.
Так как амины имеют неподеленную пару для атома азота, при этом проявляют некоторые свойства органических соединений.
Простейшие амины
Простейшие амины с алифатическими радикалами (метиламин, этиламин) растворимы в воде и подобно аммиаку, образуют основания.
Амины с ароматическим радикалом (анилин) в воде не растворимы, но также проявляют свойства оснований:
R — NH2 + Н2О ⇄ R — NH3OH ⇄ R — NH+3 + ОН—
R — NH2 + HCl ⇄ R — NH3Cl—,
R — NH2 + HNO2 + HCl → R — N ≡ NCl + 2Н2О.
Получение аминов
Получают амины таким образом:
R — NO2 + 3Н2 → R — NH2 + 2Н2О,
R — Cl + NH3 → R — NH2 + HCl,
R — ОН + NH3 (катализатор) → R — NH2 + Н2О.
Анилин
Анилин (C6H5NH2) — это бесцветная жидкость, которая на воздухе буреет вследствие окисления до нитробензола. Кипит при 184°С.
В воде не растворяется, но в присутствии кислот переходит в водную фазу благодаря образованию соответствующей соли:
C6H5NH2 + H2SO4 → C6H5NH3HSO4.
Получают анилин восстановлением нитробензола или из хлорбензола:
C6H5NO2 + 3Н2 → C6H5NH2 + 2Н2О,
С6Н5Сl + NH3 → C6H5NH3Cl.
Анилин является основным сырьем анилино-красочной промышленности.
Аминокислоты
Аминокислоты — соединения, которые содержат карбоксильную и аминогруппу. Аминокислоты твердые вещества.
У них аминогруппа может быть в любом положении к карбоксильной группе (α, β, δ, γ и т.д.).
Так как в аминокислотах содержит две функциональные группы, которые проявляют кислотные и основные свойства, то они являются амфотерными и могут образовывать диполярные ионы:
2H2NCH2COOH + Fe → Fe(H2NCH2COO)2 + Н2,
2H2NCH2COOH + СаО → Са(H2NCH2COO)2 + Н2О,
H2NCH2COOH + NaOH → H2NCH2COONa + Н2О,
HOOCCH2NH2 + НСl → НООССН2NH3Сl—,
H2NCH2COOH ⇄ H3NCH2COO—.
Альфа-аминокислоты входят в состав белков. Важнейшие из них глицин (гликоль, а-аминоуксусная кислота) H2N-CH2-COOH.
Аланин (α-амино-пропионовая кислота) СН3—СН(NH2)—СООН.
Валин (α-аминоизовалериановая кислота) СН3—СН(CH3)—СН(NH2)—СООН.
Лейцин (α-аминоизокапроновая кислота) CH3—CH(CH3)—CH2—CH(NH2)—СООН.
Изолейцин (2-амино-З-метилпентановая кислота) СН3—СН2—СН—СН—СООН и др.
Для производства синтетических так называемых полиамидных волокон используют аминокапроновую, аминоэнантовую кислоты или смесь гексаметилендиамина с двухосновными кислотами.
Например, адипиновой кислоты:
НООС-(СН2)4-СООН.
Образование капрона можно представить следующей схемой:
HOOC—(CH2)5NH2 + HOOC—(CH2)5NH2 + HOOC—(CH2)5NH2 → …—CO—(CH2)5NH—CO—(CH2)5NH— … —CO—(CH2)5NH—…
Белки
Белки это природные вещества очень сложного строения. С ними связаны все жизненные процессы.
Белки делятся на простые, или протеины, и сложные, или протеиды. Протеиды, кроме аминокислот, содержат и другие вещества (фосфорные кислоты, углеводы и др.).
Каждый белок характеризуется строгой последовательностью аминокислот и пространственной структурой.
При потреблении белков вместе с едой они под действием ферментов разлагаются на отдельные аминокислоты, которые под действием других ферментов превращаются в белки, характерные для того или другого организма.
Белковые аминокислоты называются еще нуклеиновыми, поскольку они входят в ядро клетчатки и протоплазмы.
Некоторые белки растворяются в воде, образуя коллоидные растворы.
Быстрые ответы?
Формулу можно рассматривать так: R—NХ; где Х атомы водорода, разделяются на три группы: первичными (R—NH2), вторичные (R2 — NH); третичными (R3N).
Простейшие амины водорастворимы, но по мере перехода к более сложным соединениям водорастворимость уменьшается.
В зависимости от длины цепочки атомов в органическом радикале амины могут быть газообразными, жидкими или твердыми веществами.
В зависимости от соединения, могут быть рассмотрены разные способы, например анилин может быть получен восстановлением нитробензола или из хлорбензола.
