Теория:
Натрий (Na) в периодической системе: 3‑й период, 1‑я группа (по устаревшей классификации — I A), атомная масса 22,989 а.е.м.
Занимает положение в 3‑м периоде, что определяет его принадлежность к s-элементам и семейству щелочных металлов.
Натрий — один из самых распространенных элементов в земной коре и важнейший компонент мирового океана.
В свободном виде из-за колоссальной активности не встречается, в природе находится в виде солей, самая известная из которых — поваренная соль (NaCl).
Будучи химическим элементом s-блока, он располагается в крайней левой части таблицы Менделеева, находясь под литием и над калием, обладая ярко выраженными металлическими свойствами.
Нахождение Натрия в 1‑й группе и наличие одного валентного электрона обуславливают его ключевые параметры:
Постоянную валентность I.
А также широчайшее применение в пищевой промышленности (соль), медицине (физраствор), металлургии и даже в уличном освещении (желтые натриевые лампы).
Структура атома подтверждается его электронной формулой (конфигурацией):
1s2 2s2 2p6 3s1 (или [Ne] 3s1).
На которой наглядно можно определить его положение как s-блочного элемента, имеющего один единственный электрон на внешнем 3s-подуровне.
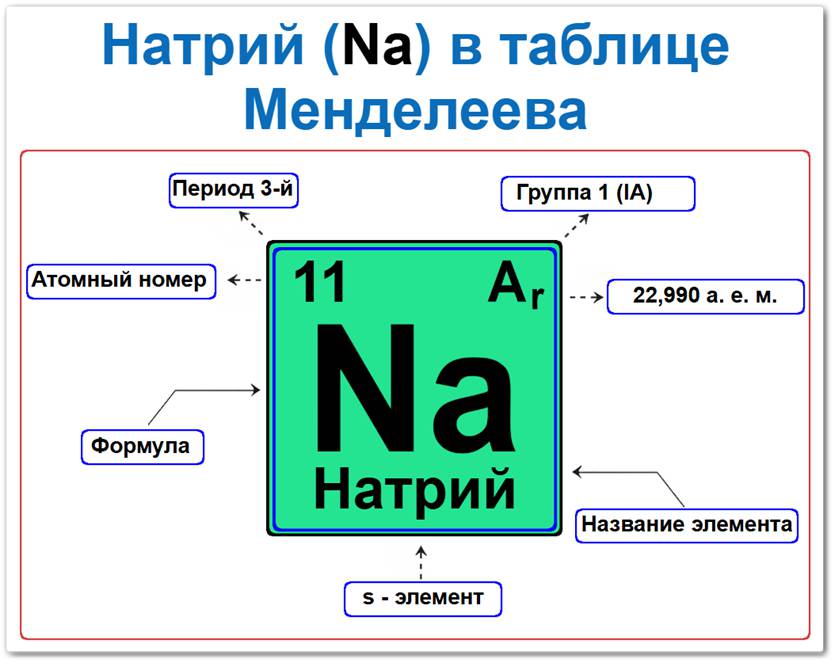
Натрий элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду щелочных металлов период 3, группа 1, а также по его порядковому номеру (Z = 11).
Содержание страницы
- 1. Как определить положение Натрия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 11)
- 3. Название и символ
- 4. Группа (1 / I A)
- 5. Период (3‑й)
- 6. Относительная атомная масса (Ar)
- 7. s‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Натрия по Таблице Менделеева
- 9. Проверка знаний: Как определить натрий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Натрия в Таблице Менделеева
Локация натрия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (1-я группа, щелочные металлы).
- Период (горизонтальный ряд).
- Электронное семейство (натрий — s‑элемент).
Порядковый номер / атомный номер (Z = 11)
- Служит уникальным кодом элемента в системе.
- В ядре — 11 протонов; в нейтральной оболочке — 11 электронов.
- Электронное строение: 2, 8, 1.
Важно: Для мастера натрий интересен прежде всего своими соединениями. Каустическая сода (гидроксид натрия) — это мощнейшее средство для очистки инструментов от старой краски и жира. В старых справочниках по столярному делу растворы соды советовали для обезжиривания древесины перед склейкой.
Название и символ
- Название: «натрий» (от др.-еврейского neter — «сода, щелок»).
- Символ: Na (Natrium).
- Примечание: Натрий настолько мягкий, что его можно резать обычным ножом. На свежем срезе он блестит как серебро, но за считанные секунды тускнеет, покрываясь слоем оксида на воздухе.
Группа (1 / I A)
Расположен в 1‑й группе. В периодической системе натрий находится в одной вертикальной колонке с литием (сверху) и калием (снизу) и относится к (подгруппе щелочных металлов).
Химический потенциал:
- Валентность натрия: всегда постоянна и равна I.
- Степень окисления натрия: +1. Натрий реагирует с водой настолько бурно, что выделяющийся водород может взорваться. Поэтому в лабораториях его хранят в банках с керосином.
Период (3‑й)
Находится в 3‑м периоде — его электроны распределены по трем энергетическим уровням.
Влияние на свойства:
- Химическая активность: Натрий активнее лития, но менее активен, чем калий. Чем больше радиус атома в этой группе, тем легче он отдает свой электрон.
- Биологическое значение: Ионы натрия — это главные «электрики» нашего тела. Они отвечают за передачу нервных импульсов, без которых мышцы не могли бы сокращаться.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Na) ≈ 22,989 а.е.м.
- Определение: Натрий в природе представлен только одним стабильным изотопом — Натрий-23.
Все значения для всех элементов можно узнать в таблице атомных масс.
s‑Элемент (электронное семейство)
Заполняется внешний 3s‑подуровень (3s1).
Специфика блока: Элементы s-блока первой группы являются самыми типичными металлами. Они обладают низкой плотностью (натрий легче воды и плавает на её поверхности во время реакции).
Определение энергетических уровней Натрия по Таблице Менделеева
Положение Натрия (Na) в системе Менделеева мгновенно раскрывает его строение.
1. 3-й период (Количество этажей)
- Итог: У Натрия 3 энергетических уровня.
2. Список «жильцов» (Распределение электронов)
Атомный номер Натрия — 11. Его 11 электронов распределены по уровням:
Na ) 2 ) 8 ) 1
3. 1-я группа (Химический характер)
- s-элемент: Один валентный электрон делает его сверхактивным «донором».
- Металлические свойства: Выражены очень сильно; типичный представитель щелочных металлов.
Проверка знаний: Как определить натрий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Натрий (Na) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 11. Заряд ядра и общее число электронов.
- 2) 3-й период, 1-й группа. Его точные координаты.
- 3) s-элемент. Отражает заполнение внешней оболочки.
- 4) Ошибка. Инертные газы — это 18-я группа.
- 5) Ошибка. Натрий исключительно мягкий.
Часто задаваемые вопросы:
Натрий расположен в 3-м периоде, 1-й группе. Порядковый номер — 11.
У натрия 3 энергетических уровня. Схема: 2, 8, 1.
Он моментально вступает в реакцию с влагой на коже, образуя едкую щелочь, которая вызывает химические ожоги.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.