Теория:
Прометий (Pm) в периодической системе: 6‑й период, 3‑я группа (по устаревшей классификации — III B), атомная масса 145 а.е.м. (у наиболее стабильного изотопа).
Занимает положение в 6‑м периоде, что определяет его принадлежность к семейству лантаноидов — редкоземельных металлов.
Прометий уникален тем, что это единственный лантаноид, не имеющий стабильных изотопов и полностью радиоактивный.
Будучи химическим аналогом других лантаноидов, он входит в состав большой группы f-элементов, расположенных после Лантана.
Нахождение Прометия в 3‑й группе (согласно длиннопериодному варианту) и специфическое заполнение f-подуровня обуславливают его ключевые параметры:
Наиболее характерную валентность III.
А также способность солей прометия светиться в темноте бледно-голубым или зеленоватым светом из-за собственного радиоактивного излучения.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Xe] 4f5 6s2.
На которой наглядно можно определить его положение как f-блочного элемента, где происходит последовательное заполнение 4f-подуровня.
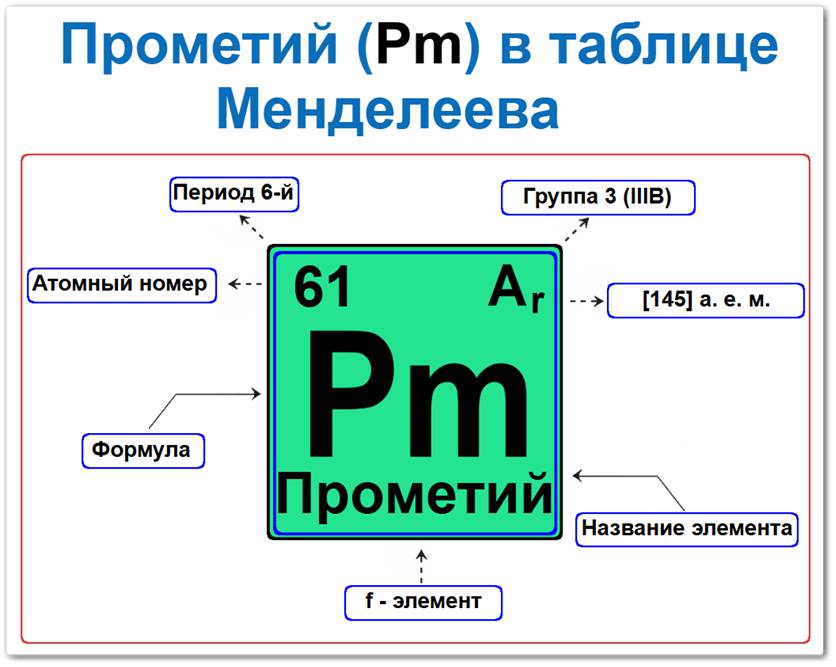
Прометий в таблице Менделеева можно определить на основании закона периодичности: положение в ряду лантаноидов период 6, группа III / Лантаноиды, а также по его порядковому номеру (Z = 61).
Содержание страницы
- 1. Как определить положение Прометия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 61)
- 3. Название и символ
- 4. Группа (3 / III B)
- 5. Период (6‑й)
- 6. Относительная атомная масса (Ar)
- 7. f‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Прометия по Таблице Менделеева
- 9. Проверка знаний: Как определить прометий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Прометия в Таблице Менделеева
Локация прометия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (формально 3-я группа, семейство лантаноидов).
- Период (горизонтальный ряд).
- Электронное семейство (прометий — f‑элемент).
Порядковый номер / атомный номер (Z = 61)
- Служит уникальным кодом элемента в системе.
- В ядре — 61 протон; в нейтральной оболочке — 61 электрон.
- Электронное строение: [Xe] 4f5 6s2.
Важно: Прометий не встречается в земной коре в заметных количествах, так как все его изотопы радиоактивны. Он получается искусственно в ядерных реакторах.
Название и символ
- Название: «прометий» (назван в честь титана Прометея, похитившего огонь у богов и передавшего его людям).
- Символ: Pm.
- Примечание: Существование элемента было предсказано Мозли, но окончательно выделен он был только в 1945 году из продуктов деления урана.
Группа (3 / III B)
Расположен в 3‑й группе (лантаноиды обычно выносятся в отдельную строку внизу таблицы, но относятся к этой группе).
Химический потенциал:
- Валентность прометия: типичная валентность III.
- Степень окисления: +3. Соли прометия используются в производстве миниатюрных атомных батареек и люминесцентных красок.
Период (6‑й)
Находится в 6‑м периоде — его электроны распределены по шести энергетическим уровням.
Влияние на свойства:
- Радиоактивность: В отличие от большинства лантаноидов, прометий нестабилен. Наиболее долгоживущий изотоп Pm-145 имеет период полураспада 17,7 лет.
- Металлические свойства: Прометий — серебристо-белый металл, который светится в темноте из-за высокой радиоактивности (радиолюминесценция).
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Pm) ≈ 145 а.е.м.
- Определение: Так как у прометия нет стабильных изотопов, в таблице обычно указывается массовое число самого устойчивого изотопа (Прометий-145).
Все значения для всех элементов можно узнать в таблице атомных масс.
f‑Элемент (электронное семейство)
Застраивающимся является 4f‑подуровнь (4f5).
Специфика блока: Будучи f-элементом, прометий по химическим свойствам крайне похож на неодим и самарий, между которыми он расположен в таблице.
Определение энергетических уровней Прометия по Таблице Менделеева
Положение Прометия (Pm) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 6-й период (Количество этажей)
Прометий находится в шестой строке таблицы. Номер периода определяет число электронных слоев.
- Итог: У Прометия 6 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Прометия — 61. Его 61 электрон распределен по уровням следующим образом:
Pm ) 2 ) 8 ) 18 ) 23 ) 8 ) 2
3. 3-я группа (Химический характер)
Прометий входит в семейство лантаноидов.
- f-элемент: Свойства определяются заполнением глубокого 4f-слоя.
- Радиогенный элемент: В природе обнаруживается только в следовых количествах в урановых рудах.
Проверка знаний: Как определить прометий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Прометий (Pm) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 61. Указывает на количество протонов в ядре.
- 2) 6-й период, лантаноиды. Показывает положение в блоке редкоземельных f-элементов.
- 3) Валентность III. Характерная черта большинства лантаноидов.
- 4) Ошибка. Прометий — металл, а не газ.
- 5) Ошибка. Элемент 6-го периода, значительно тяжелее углерода.
- 6) Ошибка. Прометий — f-элемент.
Часто задаваемые вопросы:
Прометий расположен в 6-м периоде. Относится к семейству лантаноидов (3-я группа). Его порядковый номер — 61.
У прометия 6 энергетических уровней, так как он находится в 6-м периоде.
Электронная схема: 2, 8, 18, 23, 8, 2.
Это единственный элемент среди лантаноидов, который не имеет ни одного стабильного изотопа — он полностью радиоактивен.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.