Теория:
Калий (K) в периодической системе: 4‑й период, 1‑я группа (по устаревшей классификации — I A), атомная масса 39,0983 а.е.м.
Занимает положение в 4‑м периоде, что определяет его принадлежность к активным щелочным металлам.
Калий чрезвычайно активен и в природе встречается исключительно в виде соединений, входя в состав многих минералов (сильвин, карналлит) и морской воды.
Будучи химическим элементом s-блока, он располагается в крайней левой колонке таблицы Менделеева, открывая четвертый период и возглавляя группу щелочных металлов вместе с литием и натрием.
Нахождение Калия в 1‑й группе и наличие одного валентного электрона на внешнем уровне обуславливают его ключевые параметры:
Постоянную валентность I.
А также широкое применение в сельском хозяйстве (калийные удобрения), стекольной промышленности (тугоплавкое стекло) и производстве жидкого мыла.
Структура атома подтверждается его электронной формулой (конфигурацией):
1s2 2s2 2p6 3s2 3p6 4s1 (или [Ar] 4s1).
На которой наглядно можно определить его положение как s-блочного элемента, начинающего заполнение 4-го энергетического уровня.
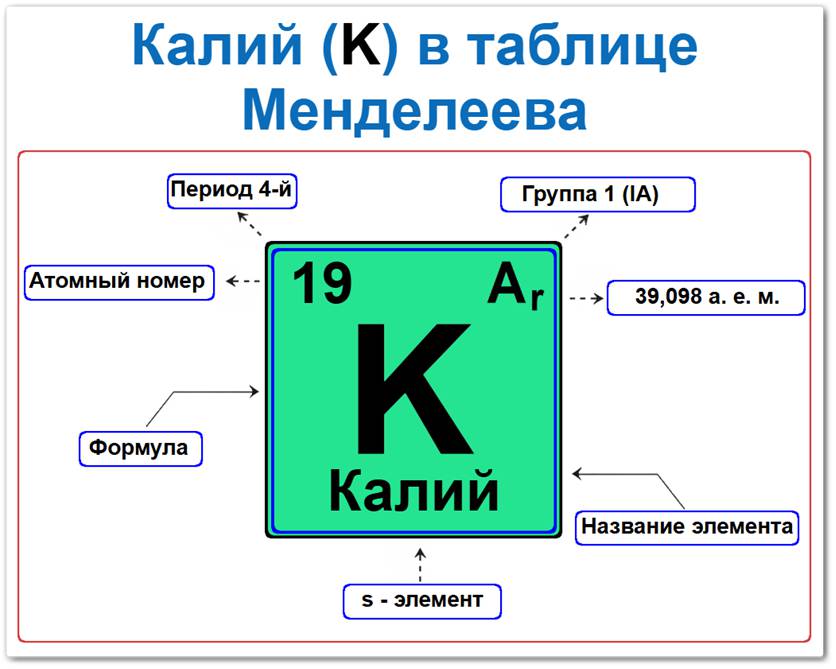
Калий элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду наиболее активных металлов период 4, группа 1, а также по его порядковому номеру (Z = 19).
Содержание страницы
- 1. Как определить положение Калия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 19)
- 3. Название и символ
- 4. Группа (1 / I A)
- 5. Период (4‑й)
- 6. Относительная атомная масса (Ar)
- 7. s‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Калия по Таблице Менделеева
- 9. Проверка знаний: Как определить калий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Калия в Таблице Менделеева
Локация калия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (1-я группа, подгруппа калия).
- Период (горизонтальный ряд).
- Электронное семейство (калий — s‑элемент).
Порядковый номер / атомный номер (Z = 19)
- Служит уникальным кодом элемента в системе.
- В ядре — 19 протонов; в нейтральной оболочке — 19 электронов.
- Электронное строение: [Ar] 4s1.
Важно: Высокая химическая активность калия требует его хранения под слоем керосина или минерального масла, так как на открытом воздухе он мгновенно окисляется, а при контакте с водой — воспламеняется.
Название и символ
- Название: «калий» (от арабского «аль-кали» — зола, так как поташ добывали из древесной золы).
- Символ: K.
- Примечание: Элемент был впервые выделен Гемфри Дэви в 1807 году путем электролиза. Это очень мягкий металл серебристо-белого цвета, который легко режется ножом.
Группа (1 / I A)
Расположен в 1‑й группе. В периодической системе калий находится в одной вертикальной колонке с натрием (сверху) и рубидием (снизу) и относится к (щелочным металлам).
Химический потенциал:
- Валентность калия: постоянная валентность I.
- Степень окисления: +1. Калий является одним из самых мощных восстановителей в химии.
Период (4‑й)
Находится в 4‑м периоде — его электроны распределены по четырем энергетическим уровням.
Влияние на свойства:
- Химическая активность: Бурно реагирует с водой, кислородом и галогенами.
- Техническое значение: Соединения калия незаменимы в медицине (регуляция сердечного ритма) и в пиротехнике (бертолетова соль).
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(K) ≈ 39,0983 а.е.м.
- Определение: среднее значение массы природных изотопов, основным из которых является стабильный Калий-39.
Все значения для всех элементов можно узнать в таблице атомных масс.
s‑Элемент (электронное семейство)
Идет заполнение внешнего 4s‑подуровня (4s1).
Специфика блока: Как типичный s-металл первой группы, калий обладает низкой плотностью (легче воды) и окрашивает пламя в характерный бледно-фиолетовый (фиалковый) цвет.
Определение энергетических уровней Калия по Таблице Менделеева
Положение Калия (K) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 4-й период (Количество этажей)
Номер периода определяет число электронных слоев.
- Итог: У Калия 4 энергетических уровня.
2. Список «жильцов» (Распределение электронов)
Атомный номер Калия — 19. Его 19 электронов распределены по уровням следующим образом:
K ) 2 ) 8 ) 8 ) 1
3. 1-я группа (Химический характер)
Калий — элемент главной подгруппы I группы (щелочной металл).
- s-элемент: Один электрон на внешнем слое делает его крайне реакционноспособным.
- Металлические свойства: Очень мягкий, легкий, обладает высокой электропроводностью.
Проверка знаний: Как определить калий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Калий (K) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 19. Соответствует заряду ядра (количеству протонов).
- 2) 4-й период, 1-й группа. Координаты калия в таблице.
- 3) s-элемент. Электронная конфигурация внешнего слоя — 4s1.
- 4) Ошибка. Калий — активный металл, а не газ.
- 5) Ошибка. Калий — элемент главной подгруппы (IA).
- 6) Ошибка. Калий всегда одновалентен.
Часто задаваемые вопросы:
Калий расположен в 4-м периоде, в 1-й группе (главная подгруппа). Его порядковый номер — 19.
Поскольку калий находится в 4-м периоде, у него 4 энергетических уровня.
Электронная схема: 2, 8, 8, 1.
Калий является s-элементом. В его атоме заполняется внешний s-подуровень.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.