Теория:
Европий (Eu) в периодической системе: 6‑й период, 3‑я группа (по устаревшей классификации — III B), атомная масса 151,96 а.е.м.
Занимает положение в 6‑м периоде, что определяет его принадлежность к семейству лантаноидов — редкоземельных металлов, обладающих уникальными фотолюминесцентными и магнитными свойствами.
Будучи химическим аналогом других лантаноидов, он входит в состав большой группы f-элементов, расположенных после Лантана.
Нахождение Европия в 3‑й группе (согласно длиннопериодному варианту) и специфическое заполнение f-подуровня обуславливают его ключевые параметры:
Характерные валентности II и III (в отличие от большинства лантаноидов, Европий очень стабилен в степени окисления +2).
А также способность интенсивно поглощать тепловые нейтроны и испускать яркое красное свечение в составе люминофоров.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Xe] 4f7 6s2.
На которой наглядно можно определить его положение как f-блочного элемента с наполовину заполненным 4f-подуровнем (ровно 7 электронов), что придает ему особую химическую активность.
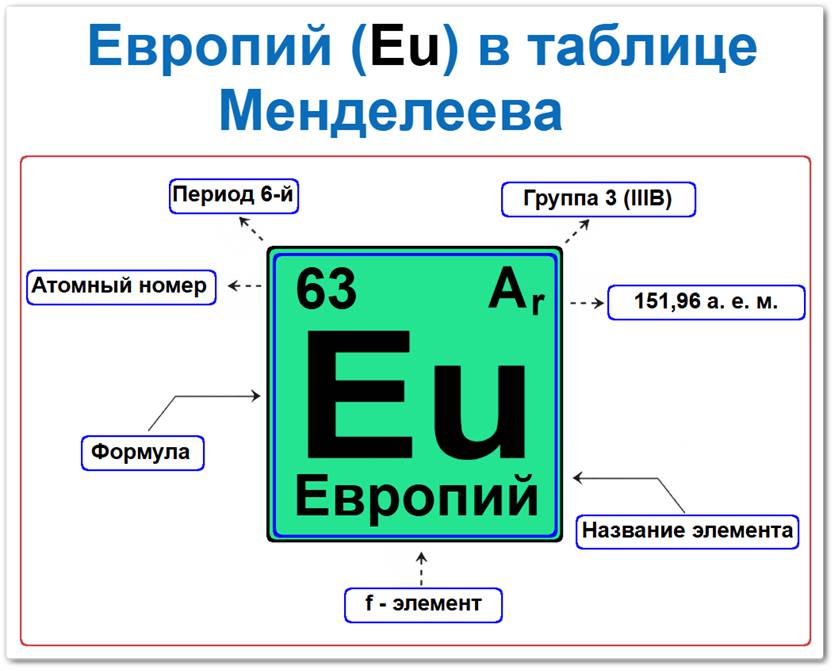
Европий в таблице Менделеева можно определить на основании закона периодичности: положение в ряду лантаноидов период 6, группа III / Лантаноиды, а также по его порядковому номеру (Z = 63).
Содержание страницы
- 1. Как определить положение Европия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 63)
- 3. Название и символ
- 4. Группа (3 / III B)
- 5. Период (6‑й)
- 6. Относительная атомная масса (Ar)
- 7. f‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Европия по Таблице Менделеева
- 9. Проверка знаний: Как определить европий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Европия в Таблице Менделеева
Локация европия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (формально 3-я группа, семейство лантаноидов).
- Период (горизонтальный ряд).
- Электронное семейство (европий — f‑элемент).
Порядковый номер / атомный номер (Z = 63)
- Служит уникальным кодом элемента в системе.
- В ядре — 63 протона; в нейтральной оболочке — 63 электрона.
- Электронное строение: [Xe] 4f7 6s2.
Важно: Европий — один из самых химически активных лантаноидов. На воздухе он быстро окисляется, напоминая по активности щелочноземельные металлы.
Название и символ
- Название: «европий» (назван в честь части света Европы).
- Символ: Eu.
- Примечание: Открыт Эженом Демарсе в 1901 году, выделен из самариевой земли. Является ключевым компонентом для создания красного цвета в экранах телевизоров и смартфонах.
Группа (3 / III B)
Расположен в 3‑й группе (лантаноиды обычно выносятся в отдельную строку внизу таблицы, но относятся к этой группе).
Химический потенциал:
- Валентность европия: проявляет валентности II и III.
- Степень окисления: +2, +3. Соединения европия используются в защитных метках банкнот евро для проверки подлинности в УФ-лучах.
Период (6‑й)
Находится в 6‑м периоде — его электроны распределены по шести энергетическим уровням.
Влияние на свойства:
- Атомный радиус: Среди лантаноидов европий выделяется аномально большим атомным радиусом из-за стабильности наполовину заполненной f-оболочки.
- Металлические свойства: Это мягкий металл, который можно резать ножом, он легко реагирует с водой, вытесняя водород.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Eu) ≈ 151,96 а.е.м.
- Определение: средневзвешенное значение массы природных изотопов (Европий-151 и Европий-153).
Все значения для всех элементов можно узнать в таблице атомных масс.
f‑Элемент (электронное семейство)
Застраивающимся является 4f‑подуровнь (4f7).
Специфика блока: У европия f-слой заполнен ровно наполовину (7 из 14), что делает его уникальным среди f-элементов и обуславливает его способность легко переходить в состояние +2.
Определение энергетических уровней Европия по Таблице Менделеева
Положение Европия (Eu) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 6-й период (Количество этажей)
- Итог: У Европия 6 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Европия — 63. Его 63 электрона распределены по уровням следующим образом:
Eu ) 2 ) 8 ) 18 ) 25 ) 8 ) 2
3. 3-я группа (Химический характер)
- f-элемент: Свойства определяются состоянием 4f-слоя.
- Место в блоке: Относится к «легким» лантаноидам (цериевая группа).
Проверка знаний: Как определить европий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Европий (Eu) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 63. Точное место Европия.
- 2) 6-й период, f-элемент. Правильная классификация в блоке лантаноидов.
- 3) Активный металл. Физико-химическое свойство, отличающее европий от «ленивых» тяжелых лантаноидов.
- 4) Ошибка. Инертные газы — p-элементы 18-й группы.
- 5) Ошибка. Европий намного тяжелее и сложнее элементов 2-го периода.
- 6) Ошибка. Это типичный металл.
Часто задаваемые вопросы:
Европий расположен в 6-м периоде, 3-й группе (ряд лантаноидов). Его порядковый номер — 63.
У европия 6 энергетических уровней. Электронная схема: 2, 8, 18, 25, 8, 2.
Он более химически активен, имеет больший радиус атома и очень часто проявляет стабильную валентность II.
