Теория:
Осмий (Os) в периодической системе: 6‑й период, 8‑я группа (по устаревшей классификации —VIII B), атомная масса 190,23 а.е.м.
Занимает положение в 6‑м периоде, что определяет его уникальную природу как самого плотного простого вещества при нормальных условиях.
Будучи химическим гомологом (аналогом) железа и рутения, он возглавляет группу платиновых металлов своего периода.
Благодаря высокой энергии связи между атомами в кристаллической решетке, осмий обладает исключительной твердостью и самой высокой температурой плавления среди платиноидов.
Его нахождение в 8‑й группе (ранее — побочная подгруппа VIII группы) задает ключевые параметры:
Максимально возможную валентность VIII.
А также способность образовывать летучий и крайне токсичный оксид OsO4.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Xe] 4f14 5d6 6s2.
На которой наглядно можно определить его положение как d-блочного элемента, находящегося в середине 5d-подуровня.
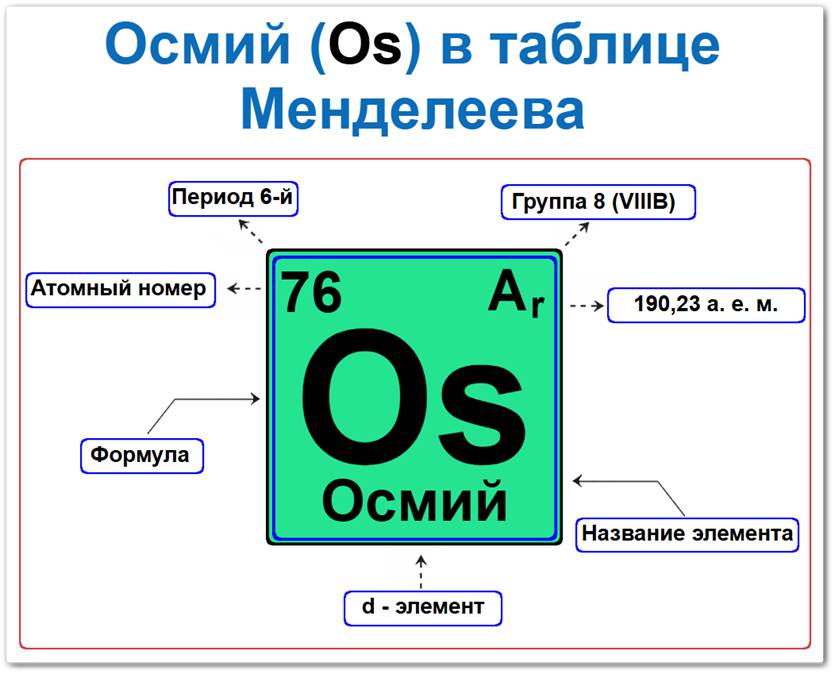
Осмий в таблице Менделеева можно определить на основании закона периодичности: положение в группе (6‑й) и периоде (8 / VIII B), а также порядкового номера / атомный номер (Z = 76).
Содержание страницы
- 1. Как определить положение Осмия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 76)
- 3. Название и символ
- 4. Группа (8 / VIII B)
- 5. Период (6‑й)
- 6. Относительная атомная масса (Ar)
- 7. d‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Осмия по Таблице Менделеева
- 9. Проверка знаний: Как определить осмий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Осмия в Таблице Менделеева
Локация осмия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (вертикальный ряд, семейство железа).
- Период (горизонтальный ряд).
- Электронное семейство (осмий — d‑элемент).
Порядковый номер / атомный номер (Z = 76)
- Служит уникальным кодом элемента в системе.
- В ядре — 76 протонов; в нейтральной оболочке — 76 электронов.
- Электронное строение: [Xe] 4f14 5d6 6s2.
Важно: Наличие шести d-электронов позволяет осмию проявлять широкий спектр степеней окисления, достигая рекордного значения +8.
Название и символ
- Название: «осмий» (от греческого «osme» — запах); из-за резкого запаха его тетраоксида.
- Символ: Os.
- Примечание: Открыт в 1803 году Смитсоном Теннантом в осадке после растворения платины.
Группа (8 / VIII B)
Расположен в 8‑й группе; по классической классификации — побочная подгруппа VIII группы (триада платиновых металлов).
Химический потенциал:
- Валентность осмия: проявляет валентности от II до VIII.
- Степень окисления: наиболее устойчивые +4 и +8. Четырехокись осмия OsO4 является сильным окислителем.
Период (6‑й)
Находится в 6‑м периоде — его электроны распределены по шести энергетическим уровням.
Влияние на свойства:
- Плотность: Положение в 6-м периоде и эффект лантаноидного сжатия делают его самым тяжелым (плотным) элементом — 22,59 г/см3.
- Твердость: Прочные металлические связи обеспечивают высокую износостойкость сплавов на его основе.
Относительная атомная масса (Ar)
- Ar(Os) ≈ 190,23 а.е.м.
- Определение: средневзвешенное значение массы семи стабильных изотопов.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
d‑Элемент (электронное семейство)
Застраивающимся является 5d‑подуровень (5d6).
Специфика блока: Будучи d-элементом, осмий обладает типичными свойствами переходного металла: высокой каталитической активностью и способностью к комплексообразованию.
Все значения для всех элементов можно узнать в таблице атомных масс.
Определение энергетических уровней Осмия по Таблице Менделеева
Положение Осмия (Os) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 6-й период (Количество этажей)
Осмий находится в шестой строке таблицы. Номер периода определяет число электронных слоев.
- Итог: У Осмия 6 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Осмия — 76. Его 76 электронов распределены по уровням следующим образом:
Os ) 2 ) 8 ) 18 ) 32 ) 14 ) 2
3. 8-я группа (Химический характер)
Осмий входит в платиновую группу.
- d-элемент: Свойства зависят от заполнения 5d-орбиталей.
- Место в блоке: Является тяжелым аналогом рутения (Ru), превосходя его по плотности и химической стойкости.
Проверка знаний: Как определить осмий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Осмий (Os) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 76. Позволяет найти элемент в d-блоке 6-го периода.
- 2) 6-й период, 8-я группа. Определяет его принадлежность к платиновым металлам.
- 3) Самый плотный металл. Физическое свойство, связанное с атомным радиусом и массой в 6-м периоде.
- 4) Ошибка. Осмий — d-металл.
- 5) Ошибка. Осмий находится в 6-м периоде.
- 6) Ошибка. Масса осмия около 190,23.
Часто задаваемые вопросы:
Осмий расположен в 6-м периоде, 8-й группе. Его атомный номер — 76.
У осмия 6 энергетических уровней (согласно номеру периода).
Распределение: 2, 8, 18, 32, 14, 2.
Это результат сочетания большой атомной массы (6 период) и малого атомного радиуса, вызванного лантаноидным сжатием, что приводит к рекордной плотности упаковки атомов.
