
Проверка выполнений заданий и ответов на вопросы
2. Сходство в том, что те и другие принадлежат к числу р-элементов и внешний электронный слой у них близок к завершению.
Различие в том, что до завершения внешнего электронного слоя у галогенов недостает лишь одного электрона, а у элементов группы кислорода — двух.
В связи с этим у галогенов электроотрицательность выражена сильнее, чем , у элементов группы кислорода.
3. Шесть.
4. Ответ на этот вопрос ищите в тексте прочитанного отрывка.
5. Кислород, так как его атомный радиус наименьший.
6. В молекуле кислорода соседние атомы кислорода связаны между собой двумя общими электронными парами, в молекуле озона — только одной.
7. Ковалентная неполярная связь.
10. В кислороде тлеющая лучинка вспыхивает, в двуокиси углерода она гаснет, а водород, положенный лучинкой, сам сгорает.
11. 3055 л. Не забудьте учесть кислород, входящий в состав каменного угля.
12. Да, хватит.
13. 350 л кислорода. Не все компоненты горят.
15. Кислород легко освободить от примеси двуокиси углерода, пропуская его через известковую воду. Освободить двуокись углерода от примеси кислорода можно, поместив в нее раскаленный уголь.
16. 11,2% СО2.
17. Ответ в тексте прочитанного отрывка.
19. При прокаливании перманганата калия в числе других продуктов образуется двуокись марганца МnО2 (уравнение приведено в тексте параграфа).
20. 56 л.
23. В случае с бертолетовой солью. Обоснование -дайте самостоятельно.
24. 90%.
27. Иодкрахмальная бумага пропитана растворами KI и крах мала. Озон реагирует с иодидом калия; при этом образуется свободный иод (уравнение в тексте прочитанного отрывка).
28. См. ответ на вопрос 6 в данной главе.
32—33. Ответы найдите в тексте прочитанного отрывка.
36. Вода не вступает в реакции с другими веществами с образованием солей.
37. Нет. Обоснуйте ответ самостоятельно.
38. См. текст.
40. Гидролиз.
41. 7,7% NaOH. Не забудьте, что часть воды расходуется на реакцию с натрием.
42. 21,25%.
44. 295,3 л.
45. 3,2 кг.
46. 13,6 г.
47. Вес увеличился на 10,55 г. Спирт содержал 7% воды.
48. 5,5%.
54—55. Примеры можно найти на странице.
58. Получить кислород из перекиси водорода можно, например, приборе, изображенном на рис. 2.
59. 845 г ВаО2.
62. 133,3 л воздуха.
63. 1,545 м3.
69. В соединениях с водородом и металлами сера имеет степень окисления —2.
70. Соединения серы с металлами обычно являются ионными.
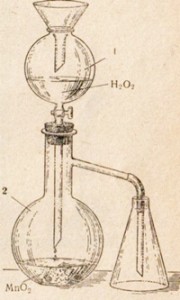
Рис. 2 Прибор для получения кислорода из перекиси водорода. 1 — капельная воронка с перекисью водорода; 2 — колба Вюрца с двуокисью марганца.
71. Сульфиды цинка и алюминия, будучи солями слабого основания и слабой кислоты, легко гидролизуются, поэтому не могут быть получены в растворах реакцией обмена.
Подтвердите это положение, приведя уравнения реакций гидролиза этих сульфидов. Докажите, что в растворе вместо осадков AlaS3 и ZnS образуются Аl(ОН)3 и Zn(OH)2.
72. 42,4 г FeS.
76. Объяснение такое же, как при взаимодействии с бромной водой (см. в тексте прочитанного отрывка).
77. Нет.
78. Уравнение записывайте с образованием средней соли.
80. а) рис. 2.
81. 9,1%.
82. Двуокись серы — кислотный окисел.
85. 716,8 л.
86. 28,2%.
94. Нет.
95. SО2 из ZnS получается обжигом, в результате которого образуются окись цинка и двуокись серы. Уравнение напишите самостоятельно. Остальные уравнения также напишите самостоятельно.
Серная кислота с карбонатом кальция образует малорастворимый сульфат кальция, который, осаждаясь на карбонате, прекращает доступ к нему серной кислоты, и реакция останавливается.
98. Задание выполните самостоятельно.
99—100. Ответы на эти вопросы найдите в тексте.
101. Это связано с активацией молекул. Подробнее см. в тексте.
102. В эндотермических процессах при образовании продукта реакции энергии выделяется меньше, чем требуется для первоначальной активации молекул, поэтому энергия поглощается и должен быть постоянный приток ее извне.
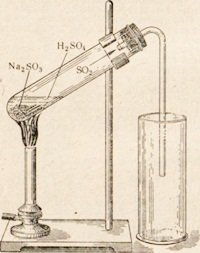
Рис. 2. Прибор для получения двуокиси серы из сульфита натрия.
103—104. Растирание и растворение увеличивают поверхность соприкосновения реагирующих веществ, что повышает скорость реакции.
105. Во-первых, реакция между CuSO4 и NaOH — ионная, поэтому она может протекать только в растворе. Во-вторых, растворение способствует увеличению поверхности.
106—109. Ответы на эти вопросы легко найти в тексте.
111. На химическое равновесие могут оказывать влияние три фактора—температура, давление, концентрация. Катализатор и увеличение поверхности влияют лишь на скорость химической реакции.
112. Сущность принципа Ле Шателье:
1) при увеличении давления в реакциях (а), (б), (в) равновесие будет смещено вправо, в сторону образования продуктов реакции, занимающих меньший объем.
В реакции (г) с увеличением давления равновесие будет смещаться влево в сторону образования твердого РСl5, занимающего меньший объем на реакцию (б) увеличение давления не повлияет.
2) повышение температуры в реакциях (а) и (в) повлечет смещение равновесия влево, так как тепло поглощается при обратной реакции.
В реакциях (б) и (г) равновесие сместится вправо, т. е. прямые реакции протекают с поглощением тепла.
117. 6,891 т моногидрата.
118. 255,1 кг
119. 90%.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.