Содержание страницы
Теория:
Молекулярная масса гидроксида кальция Ca(OH)2 это масса одной молекулы вещества, выраженная в атомных единицах массы.
Поэтому она рассчитывается как сумма атомных масс входящих в ее состав элементов.
Молекулярную массу каждого химического элемента можно найти в таблице химических элементов Менделеева.
Единицы расчета: атомная единица массы (а.е.м.) и грамм на моль (г/моль).
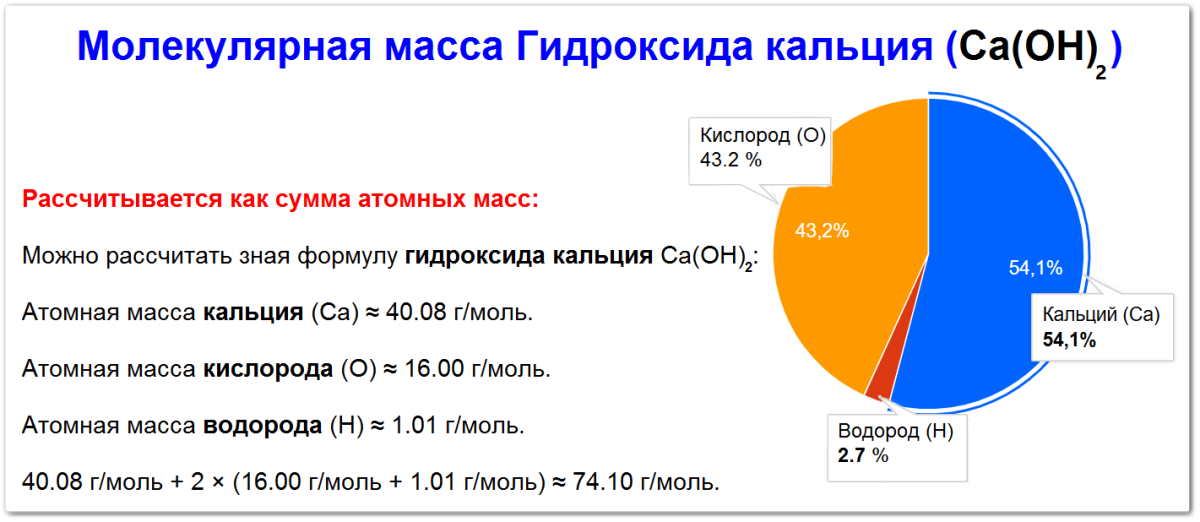
Как вычислить молекулярную массу гидроксида кальция
Молекулярная масса гидроксида кальция рассчитывается как сумма атомных масс входящих в его состав элементов:
Атомная масса кальция (Са) ≈ 40.08 г/моль.
Атомная масса кислорода (О) ≈ 16.00 г/моль.
Атомная масса водорода (Н) ≈ 1.01 г/моль.
Поэтому молекулярная масса составляет:
M(Ca(OH)2) = M(Ca) + 2 × (M(O) + M(H)).
M(Ca(OH)2) = 40.08 г/моль + 2 × (16.00 г/моль + 1.01 г/моль)
M(Ca(OH)2) = 40.08 г/моль + 2 × (17.01 г/моль).
M(Ca(OH)2) = 40.08 г/моль + 34.02 г/моль.
M(Ca(OH)2) = 74.10 г/моль.
Молярная масса гидроксида кальция Са(ОН)2 которая численно равна молекулярной массе, составляет примерно 74.10 г/моль.
Часто используют округленные значения атомных масс в этом случае молекулярная масса будет: 74 г/моль.
Процентное содержание элементов в гидроксиде кальция
Процентное содержание элементов в Ca(OH)2 рассчитывается на основе его молекулярной массы.
Для определения процентного содержания каждого элемента, используют округленные атомные массы:
1. Масса кальция (Ca) в 1 моле Ca(OH)2: 40.08 г.
Процентное содержание кальция:
(Масса Ca / Молярная масса Ca(OH)2) × 100% = (40.08 г / 74.10 г) × 100% ≈ 54.10%
2. Масса кислорода (O) в 1 моле Ca(OH)2: 2 атома × 16.00 г/моль = 32.00 г.
Процентное содержание кислорода:
(Масса O / Молярная масса Ca(OH)2) × 100% = (32.00 г / 74.10 г) × 100% ≈ 43.18%
3. Масса водорода (H) в 1 моле Ca(OH)2: 2 атома × 1.01 г/моль = 2.02 г.
Процентное содержание водорода:
(Масса H / Молярная масса Ca(OH)2) × 100% = (2.02 г / 74.10 г) × 100% ≈ 2.73%
Процентное содержание элементов в гидроксиде кальция (Ca(OH)2) составляет примерно:
- Кальций (Ca): 54.10%.
- Кислород (O): 43.18%.
- Водород (H): 2.73%.
Сумма процентов: 54.10% + 43.18% + 2.73% = 100.01% (небольшая погрешность связана с округлением атомных масс).
Пример решения, задача:
Задача № 1.
Дано: Какова масса 0,1 моль гидроксида кальция (Ca(OH)2)? Используйте молярную массу, 74 г/моль.
Решение: Масса (m) = Количество вещества (n) × Молярная масса (M) m(Ca(OH)2) = 0,1 моль × 74 г/моль = 7,4 г.
Ответ: 7,4 г.
Задача № 2.
Дано: Сколько моль гидроксида кальция (Ca(OH)2) содержится в образце массой 37 г? (Используйте молярную массу 74 г/моль).
Решение: Количество вещества (n) = Масса (m) / Молярная масса (M) n(Ca(OH)2) = 37 г / 74 г/моль = 0,5 моль.
Ответ: 0,5 моль.
Часто задаваемые вопросы
Относительная молекулярная масса гидроксида кальция (Ca(OH)2) рассчитывается как сумма относительных атомных масс входящих в его состав элементов:
Водород (H): 1.01
Кальций (Ca): 40.08
Кислород (O): 16.00
40.08 + 2 × (16.00 + 1.01) = 74.10
Для этого нужно сложить атомные массы входящих в ее состав элементов кальций, водород и кислород:
40.08 + 2 х (1.01 + 16) = 74.10 г/моль.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.