Содержание страницы
Теория:
Молекулярная масса нитрата калия это масса одной молекулы вещества, выраженная в атомных единицах массы (г/моль.).
Поэтому она рассчитывается как сумма атомных масс входящих в ее состав элементов.
Молекулярную массу каждого химического элемента можно найти в таблице химических элементов Менделеева.
Единицы расчета для определения: атомная единица массы (а.е.м.) и грамм на моль (г/моль).
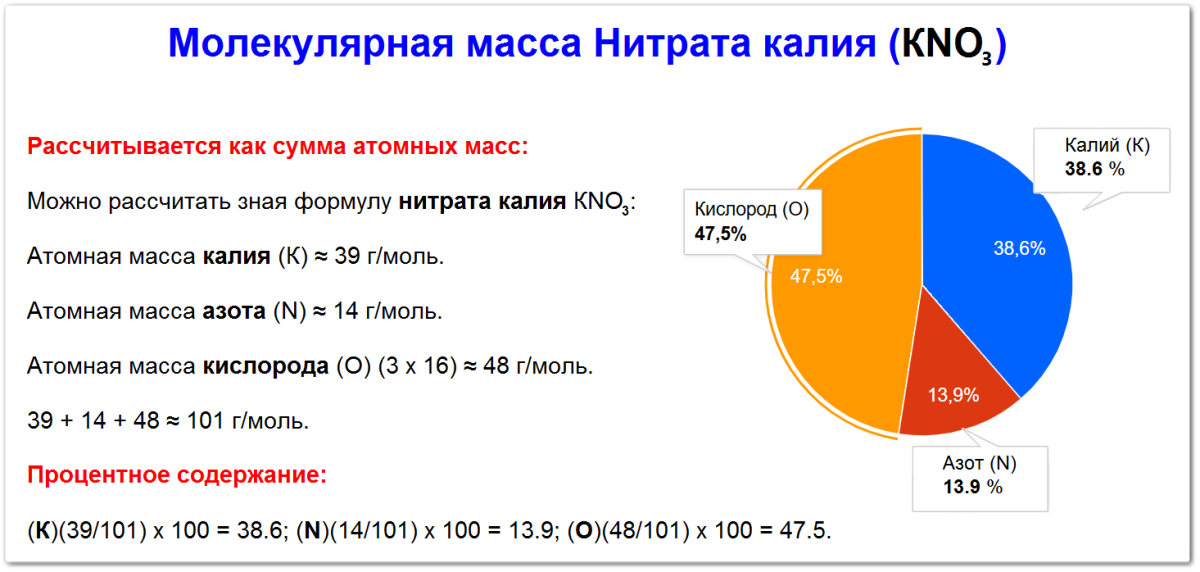
Как вычислить молекулярную массу нитрата калия
Молекулярная масса нитрата калия рассчитывается как сумма атомных масс входящих в его состав элементов:
Атомная масса калия (К) ≈ 39.10 а.е.м.
Атомная масса азота (N) ≈ 14.01 а.е.м.
Атомная масса кислорода (О) ≈ 15.99 а.е.м.
Поэтому молекулярная масса составляет:
Mr(KNO3) = Ar(K) + Ar(N) + (3 + Ar(O) = 39.10 + 14.01 + (3 х 15.99) = 39.10 + 14.01 + 47.97 ≈ 101.10
Молекулярная масса нитрата калия — молярная масса которая численно равна примерно 101.10 г/моль.
Часто используют округленные значения атомных масс (К = 39.10, N = 14.01, О = 47.97), в этом случае молекулярная масса будет: 101 г/моль.
Процентное содержание элементов в нитрате калия
Процентное содержание элементов в KNO3 рассчитывается на основе его молекулярной массы.
Молекулярная масса ≈ 101.10 а.е.м.
Если использовать округленные значения (K = 39, N = 14, О = 48 а.е.м.), то молекулярная масса будет ≈ 101 а.е.м.
Рассчитаем процентное содержание, используя округленные значения для простоты:
1. Масса калия (К):
- В молекуле KNO3 содержится 1 атом К.
- Общая масса K = 39 а.е.м.
2. Масса азота (N):
- В молекуле KNO3 содержится 1 атом N.
- Общая масса N = 14 а.е.м.
3. Масса кислорода (О):
- В молекуле KNO3 содержится 3 атома О.
- Масса О = 16 х 3 = 48 а.е.м.
3. Общая молекулярная масса (KNO3):
39 а.е.м. + 14 а.е.м. + 48 а.е.м. = 101 а.е.м.
4. Процентное содержание K:
- (Масса К / Молекулярная масса KNO3) × 100% = (39 / 101) × 100% ≈ 38.6 %
5. Процентное содержание N:
- (Масса N / Молекулярная масса KNO3) × 100% = (14 / 101) × 100% ≈ 13.8 %
6. Процентное содержание O:
- (Масса О / Молекулярная масса KNO3) × 100% = (48 / 101) × 100% ≈ 47.6 %
Таким образом, в нитрате калия содержится примерно:
- 38.6 % калия
- 13.8 % азота
- 47.6 % кислорода
Проверяем: 38.6 + 13.8 + 47.6 = 100 %
Если использовать более точные атомные массы, процентные содержания будут немного отличаться.
Пример решения:
Задача № 1.
Дано: Какова масса 0,2 моль нитрата калия (KNO3)? Используйте молярную массу, рассчитанную в предыдущей задаче.
Решение:
Масса (m) = Количество вещества (n) × Молярная масса (M)
m(KNO3) = 0,2 моль × 101 г/моль = 20,2 г.
Ответ: 20,2 г.
Задача №2.
Дано: Сколько моль нитрата калия (KNO3) содержится в образце массой 50,5 г? (Используйте молярную массу 101 г/моль).
Решение:
Количество вещества (n) = Масса (m) / Молярная масса (M)
n(KNO3) = 50,5 г / 101 г/моль = 0,5 моль.
Ответ: 0,5 моль.
Часто задаваемые вопросы
Относительная молекулярная масса (KNO3) равна 101.10

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.