Теория:
Степень окисления молибдена (Mo) в наиболее устойчивых соединениях чаще всего равна +6 и +4, а в свободном состоянии (простое вещество) — 0.
Промежуточные значения (-2, -1, +1, +2, +3, +5) также существуют, что делает молибден одним из самых химически гибких переходных металлов.
Это связано с несколькими ключевыми характеристиками атома молибдена:
- Заряд ядра (Z = 42): Определяет его положение в 6-й группе (побочная подгруппа VI группы) и классифицирует как тяжелый d-металл 5-го периода.
- Электронная конфигурация ([Kr] 4d5 5s1): Наличие шести валентных электронов позволяет атому проявлять широкий диапазон состояний. Эффект «провала» электрона создает стабильную полузаполненную d-оболочку.
- Электроотрицательность (2.16 по Полингу): Молибден обладает умеренной способностью удерживать электроны, что позволяет ему формировать как ионные, так и прочные ковалентные связи в высоких степенях окисления.
- Атомная масса (95.95): Значительный размер радиуса атома способствует образованию сложных кластерных соединений и многоядерных полимолибдатов.
Например: в триоксиде молибдена (MoO3) формула степень окисления металла достигает максимума, где он отдает все 6 валентных электронов, проявляя заряд +6.
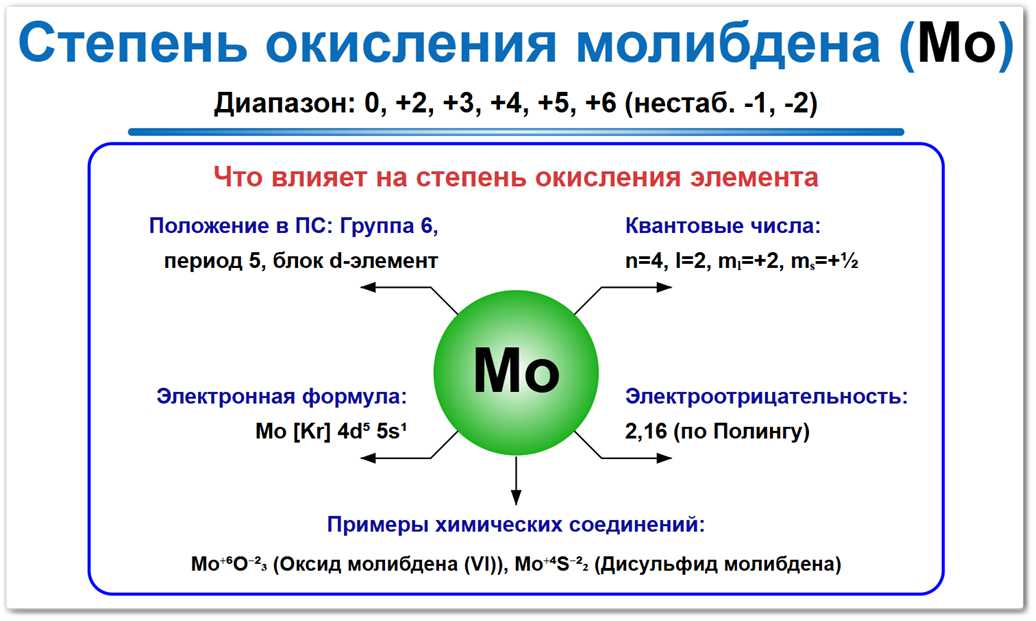
Рис. 1. Возможные степени окисления молибдена: от -2 до +6. Самые устойчивые — +4 и +6.
Обратите внимание, что для молибдена характерно образование «молибденовой сини» — смеси соединений, где металл одновременно находится в разных промежуточных состояниях.
На их формирование влияют электронное строение (4d5 5s1), положение в 6-й группе и значение электроотрицательности 2,16 по шкале Полинга.
Содержание страницы
- 1. Почему у молибдена переменные степени окисления?
- 2. Степень окисления молибдена в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления может быть разной?
- 4. Как определить степень окисления молибдена
- 4.1. По таблице Менделеева
- 4.2. По валентности
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления молибдена
- 6. Шпаргалка для молибдена
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у молибдена переменные степени окисления?
Причина многообразия состояний молибдена кроется в близости энергетических уровней 4d и 5s. Атом может задействовать их в реакциях как по отдельности, так и полностью.
- В простом веществе (Mo⁰): Заряд равен 0. Конфигурация:
5s [↑] 4d [↑][↑][↑][↑][↑]. - В высшем ионе (Mo+6): Молибден отдает все 6 электронов. Конфигурация:
[Kr](полная стабильность).

Рис. 2. Процесс окисления молибдена: переход от нейтрального атома к высшему состоянию окисления.
Степень окисления молибдена в соединениях
В зависимости от условий, молибден в соединениях проявляет степень окисления, которая диктует его химические свойства — от восстановительных до кислотных:
- Триоксид молибдена (MoO3): Mo +6, O -2.
- Диоксид молибдена (MoO2): Mo +4, O -2.
- Сульфид молибдена(IV) (MoS2): Mo +4, S -2.
- Хлорид молибдена(V) (MoCl5): Mo +5.
- Хлорид молибдена(III) (MoCl3): Mo +3.
- Карбонил молибдена (Mo(CO)6): Mo 0.
Высшая степень окисления
Высшая степень окисления молибдена равна +6. Она достигается при полном вовлечении всех шести электронов внешней оболочки в связь с сильными окислителями (кислород, фтор).
Низшая степень окисления
Для молибдена в веществах с металлами могут фиксироваться отрицательные значения, например -2 в редких карбонильных комплексах, но типичная низшая для расчетов в школе — 0.
Промежуточные степени окисления
Состояния +2, +3 и +5 часто встречаются в галогенидах и комплексных солях. Степень окисления молибдена в веществах такого типа делает их химически активными и склонными к реакциям окисления-восстановления.
Важно: Соединение MoS2 (молибденит) — это основной природный источник элемента, где степень окисления молибдена формула соединения четко указывает на заряд +4.
Почему степень окисления может быть разной?
Знак заряда и его величина зависят от партнера по реакции:
- Положительная СО (+): Проявляется с неметаллами. Благодаря степени окисления молибдена равной +6, он образует молибдаты (например, Na2MoO4).
- Нулевая СО (0): Характерна для металлического молибдена, который обладает сверхвысокой температурой плавления.
Как определить степень окисления молибдена
По таблице Менделеева
- Семейство: d-элемент.
- Валентные электроны: 6.
- Атомная масса молибдена: 95,95 а.е.м.
По валентности
Валентность молибдена в стабильных оксидах равна VI, что напрямую коррелирует с его высшим зарядом.
По электронной конфигурации
- Электронная формула молибдена: [Kr] 4d5 5s1. Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
- Атому молибдена степени окисления +6 достичь легко, так как подуровни 4d и 5s стремятся к полному опустошению для стабильности.
По химическому соединению (Алгебраический расчет)
Пример для молибдата аммония (NH4)2MoO4:
Группа (NH₄) имеет заряд +1, Кислород -2. Сумма равна 0.
2 · (+1) + x + 4 · (-2) = 0
2 + x — 8 = 0 ⇒ x = +6
Примеры степеней окисления молибдена
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +6 | Высшая, кислотные свойства. | MoO3, H2MoO4, MoF6 |
| +4 | Стабильная, амфотерная. | MoO2, MoS2 |
| +3, +5 | Промежуточные, восстановители. | MoCl3, MoCl5 |
| 0 | Металлическое состояние. | Mo (порошок или слиток) |
Шпаргалка для молибдена
- +6 — высшая СО, образует молибденовую кислоту.
- +4 — СО в самом распространенном минерале молибдените.
- Легирование — молибден в СО 0 делает сталь сверхпрочной.
Пример решения задачи:
▶️ Дано:
Соединение: MoCl5.
⌕ Найти:
Определите СО молибдена.
✨ Решение:
Хлор (Cl) имеет заряд −1. Уравнение: x + 5 · (−1) = 0 → x = +5.
✅ Ответ:
Mo(+5).
Проверка знаний
Показать ответы
Часто задаваемые вопросы
Наиболее устойчивым в водных растворах является состояние +6 в составе молибдат-ионов (MoO42-).
Это характерно для d-элементов середины периодов. У них много неспаренных электронов на 4d-подуровне, которые могут участвовать в образовании связей по одному или группами.
Это сложные продукты частичного восстановления молибдатов, в которых молибден проявляет одновременно степени окисления +5 и +6, что дает яркую синюю окраску.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.