Теория:
Степень окисления технеция (Tc) в наиболее устойчивых соединениях чаще всего принимает значения +7 и +4, а в свободном состоянии (простое вещество) она равна 0.
Будучи переходным металлом, технеций способен проявлять широкий диапазон состояний от -1 до +7.
Промежуточные значения (+1, +2, +3, +5, +6) встречаются реже и часто требуют специфических условий для стабилизации.
Это связано с несколькими ключевыми характеристиками атома технеция:
- Заряд ядра (Z = 43): Определяет его положение в 7-й группе (побочная подгруппа VII группы) и делает его первым искусственно полученным элементом в таблице Менделеева.
- Электронная конфигурация ([Kr] 4d5 5s2): Наличие семи валентных электронов обуславливает способность элемента отдавать их все, достигая высшей степени окисления.
- Электроотрицательность (1.9 по Полингу): Относительно невысокое значение позволяет технецию легко вступать в ковалентные и ионные связи, проявляя преимущественно положительные заряды.
- Атомная масса (98.906): У технеция нет стабильных изотопов. Радиоактивная природа элемента влияет на методы изучения его химических свойств в различных средах.
Например: в пертехнетате калия (KTcO4) формула степень окисления технеция достигает максимума, где он отдает 7 электронов, проявляя заряд +7.
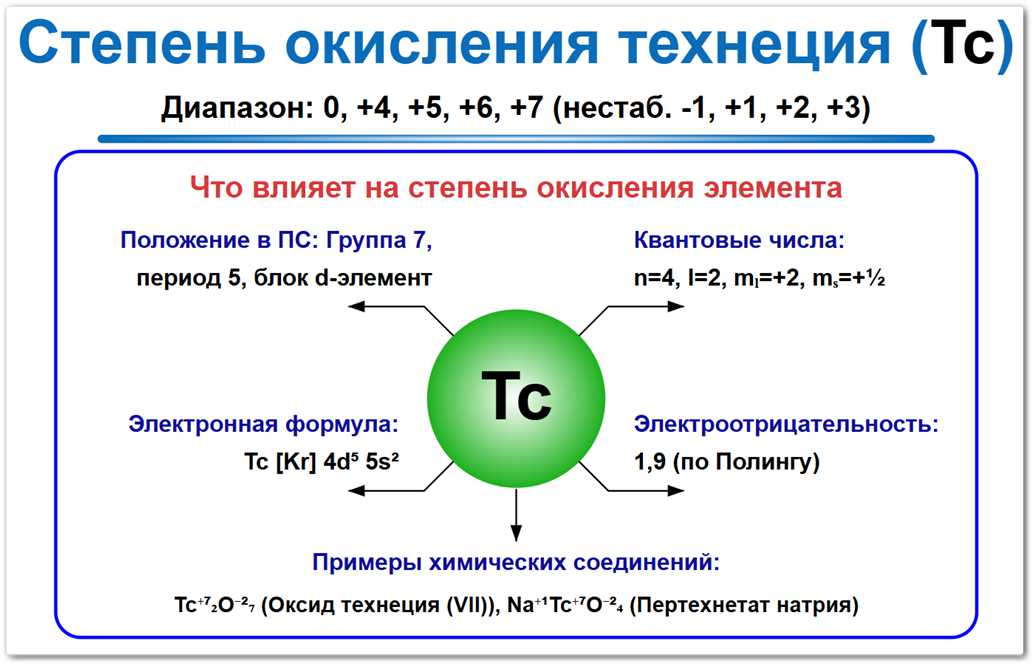
Рис. 1. Возможные степени окисления технеция: от -1 до +7. Наиболее устойчивые формы — +7 (пертехнетаты) и +4 (оксид), а также -3 крайне нестабильная.
Обратите внимание, что химия технеция во многом схожа с химией рения (Re), своего соседа по группе, что отражается на стабильности их высших оксидов.
На их формирование влияют электронное строение (4d5 5s2), положение в 7-й группе и значение электроотрицательности 1,9 по шкале Полинга.
Содержание страницы
- 1. Почему у технеция стабильная степень окисления?
- 2. Степень окисления технеция в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления технеция
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления технеция
- 6. Шпаргалка для технеция
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у технеция стабильная степень окисления?
Причина стабильности высших состояний технеция заключается в возможности полного освобождения 4d- и 5s-орбиталей, что приводит к достижению электронной конфигурации инертного газа.
- В простом веществе (Tc⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 4d [↑][↑][↑][↑][↑]. - В ионе (Tc+7): Технеций отдает все 7 валентных электронов. Конфигурация:
[Kr].

Рис. 2. Процесс окисления технеция: от металлического состояния до высшего катиона в составе солей.
Степень окисления технеция в соединениях
В зависимости от реагентов, технеций в соединениях проявляет степень окисления, определяющую его растворимость и химическую активность:
- Оксид технеция(VII) (Tc2O7): Tc +7, O -2.
- Диоксид технеция (TcO2): Tc +4, O -2.
- Пертехнетат натрия (NaTcO4): Tc +7.
- Гексафторид технеция (TcF6): Tc +6.
- Сульфид технеция(VII) (Tc2S7): Tc +7.
Высшая степень окисления
Высшая степень окисления технеция равна +7. Это значение полностью соответствует номеру группы (VII) в периодической системе и является наиболее устойчивым в окислительной среде.
Низшая степень окисления
Для технеция в металлоорганических комплексах возможна степень окисления -1, однако степени окисления технеция равны 0 в металлическом виде — это наиболее типичное низшее состояние для расчетов.
Промежуточные степени окисления
Степень окисления технеция в веществах может принимать значения +1, +2, +3, +5 и +6, но такие соединения часто склонны к диспропорционированию (самопроизвольному превращению в +4 и +7).
Важно: Анион [TcO4]⁻ (пертехнетат) — это основная химическая форма, в которой технеций существует в растворах, где степень окисления технеция формула соединения всегда +7.
Почему степень окисления чаще положительная?
Знак заряда определяется низкой электроотрицательностью металла по сравнению с неметаллами:
- Положительная СО (+): Технеций легко отдает электроны кислороду и галогенам, образуя устойчивые ковалентные связи.
- Нулевая СО (0): Характерна для компактного металла.
- Отрицательная СО (-): Редка, встречается только в сложных координационных соединениях с π-акцепторными лигандами.
Как определить степень окисления технеция
По таблице Менделеева
- Семейство: d-элемент.
- Валентные электроны: 7 (5 на d-подуровне и 2 на s-подуровне).
- Атомная масса технеция: 98 а.е.м. (для технеция-99).
По валентности (Число связей)
В отличие от металлов с постоянными значениями, валентность технеция переменна и в наиболее устойчивых соединениях чаще всего равна VII или IV.
Это означает, что атом технеция может образовывать различное количество химических связей, задействуя свои валентные электроны (4d5 5s2).
- В высшем оксиде (Tc2O7): Каждый атом технеция образует семь химических связей с атомами кислорода. В этом случае его валентность равна VII, а степень окисления технеция равна +7.
- В диоксиде технеция (TcO2): Атом технеция формирует четыре связи с кислородом. Здесь его валентность — IV, а СО технеция в соединениях такого типа составляет +4.
- В пертехнетат-ионе (TcO4—): Несмотря на отрицательный заряд иона, технеций связан семью связями с кислородом, поэтому его валентность остается VII.
По электронной конфигурации
- Электронная формула технеция: [Kr] 4d5 5s2. Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
- Атому технеция степени окисления +7 достичь энергетически выгодно при полном окислении.
По химическому соединению (Алгебраический расчет)
Пример для TcO2 (диоксид технеция):
Сумма СО равна 0. Обозначим Tc как x, Кислород равен -2.
x + 2 · (-2) = 0
x — 4 = 0 ⇒ x = +4
Технеций — один из тех элементов, которые могут проявлять практически все степени окисления от -1 до +7 благодаря семи валентным электронам (4d5 5s2).
Если мы делаем максимально подробную таблицу, то стоит добавить состояния +5, +2, +1 и -1, чтобы охватить всю химию элемента.
Примеры степеней окисления технеция
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +7 | Высшая / Типичная. Максимально устойчивое состояние. | Tc2O7, HTcO4, KTcO4 |
| +6, +5 | Промежуточные. Склонны к диспропорционированию. | TcF6, TcCl5, TcO3 (нестабилен) |
| +4 | Стабильная. Характерна для нерастворимых форм. | TcO2, TcS2, K2TcCl6 |
| +3, +2, +1 | Низкие. Проявляются в комплексных соединениях. | TcCl3, [Tc(H2O)6]2+, [Tc(CO)5Cl] |
| 0 | Металл. Состояние свободного атома. | Tc (компактный технеций) |
| -1 | Отрицательная. Редкая, только в металлоорганических комплексах. | HTc(CO)5 |
Шпаргалка для технеция
- +7 — главная СО, образует сильную технециевую кислоту.
- Медицина — изотоп Tc-99m в СО +7 часто используется для радиодиагностики.
- Коррозия — пертехнетат-ионы являются отличными ингибиторами коррозии стали.
Пример решения задачи:
▶️ Дано:
Соединение: NaTcO4.
⌕ Найти:
Определите СО технеция.
✨ Решение:
Натрий (Na) всегда +1, Кислород (O) -2. Уравнение: 1 + x + 4 · (-2) = 0 → 1 + x — 8 = 0 → x = +7.
✅ Ответ:
Tc(+7).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4.
Разбор ошибок:
3 — неверно: технеций не имеет стабильных изотопов и полностью радиоактивен.
Часто задаваемые вопросы
В присутствии кислорода и в водных растворах наиболее устойчива форма +7 (пертехнетат). В виде твердых оксидов очень стабильна форма +4 (TcO2).
Его максимальная степень окисления — +7.
Почему положительная: У технеция на внешних и предвнешних уровнях 7 электронов (4d5 5s2). Он может отдавать их (все или частично) более электроотрицательным элементам (например, кислороду в Tc2O7), приобретая положительный заряд.
Почему отрицательная: Это характерно для переходных металлов в соединениях с особыми лигандами (например, CO). Технеций может принимать электронную плотность на свои свободные орбитали, образуя степени окисления до -1 (в карбонильных комплексах типа [Tc(CO)5]—), чтобы достичь стабильной электронной конфигурации.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.