Теория:
Степень окисления осмия (Os) варьируется в беспрецедентно широком диапазоне: от -4 до +8.
Этот элемент, наряду с рутением, является рекордсменом периодической таблицы по способности достигать высшего положительного заряда.
Кроме того, выделяют значение 0, характерное для чистого благородного металла.
Например для наиболее стабильной СО +4: в соединении OsO2 (диоксид осмия) степень окисления металла равна +4. Это состояние является одним из самых устойчивых в твердой фазе.
Для сравнения, СО +8: встречается в печально известном летучем соединении OsO4 (тетраоксид осмия).
- Почему +8? Осмий — представитель 8-й группы. Его электронная конфигурация [Xe] 4f14 5d6 6s2 позволяет задействовать все восемь внешних электронов (два с 6s и шесть с 5d-подуровней) при взаимодействии с сильнейшими окислителями, такими как кислород.
- Почему +4 так часто встречается? Это «золотая середина» для химии осмия. Энергетически выгодно оставить заполненными часть d-орбиталей, что обеспечивает прочность связей в координационных соединениях и простых оксидах.
- Почему есть отрицательные СО? Как и другие металлы платиновой группы, осмий способен принимать электроны в специфических комплексах с π-акцепторными лигандами (например, карбонилами), достигая значений вплоть до -4.
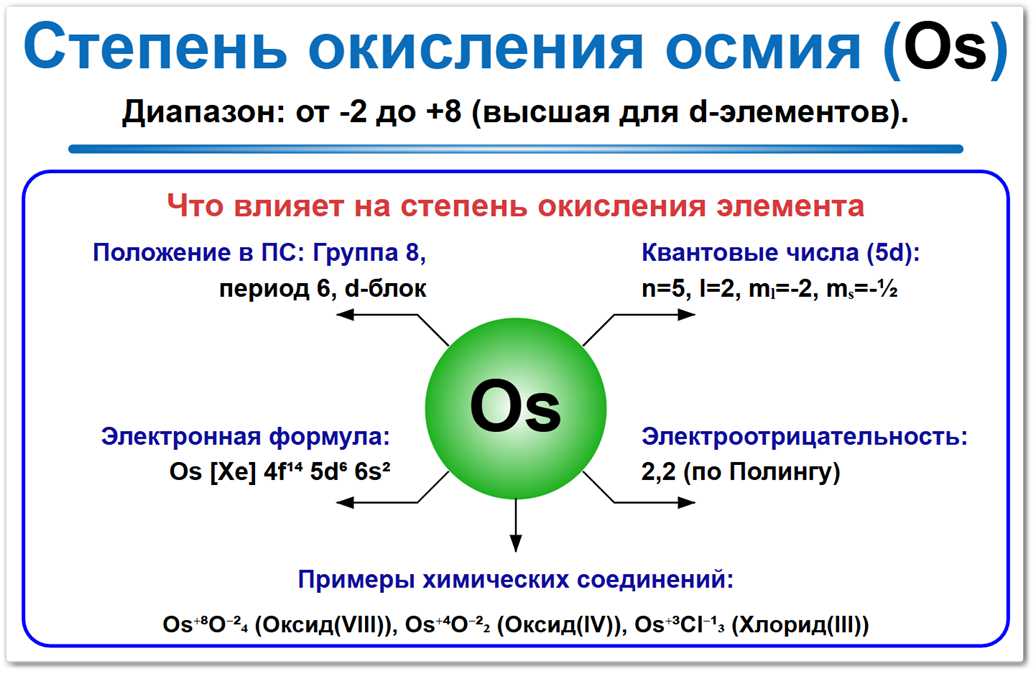
Наиболее устойчивые химические формы — +4 (диоксид) и +8 (тетраоксид), уникальные для платиноидов.
Обратите внимание, что химия осмия в высшей степени окисления +8 сильно отличается от свойств типичных металлов: тетраоксид OsO4 проявляет свойства кислотного оксида, является летучим и крайне токсичным веществом.
На формирование его параметров влияют электронное строение (5d6 6s2), положение в семействе платиновых металлов и значение электроотрицательности 2,2 по шкале Полинга.
Содержание страницы
- 1. Почему +4 и +8 — ключевые степени окисления у осмия
- 2. Степень окисления осмия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему осмий может как отдавать электроны (+8), так и принимать (-4)?
- 4. 4 способа определить степень окисления осмия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления осмия
- 6. Шпаргалка для осмия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +4 и +8 — ключевые степени окисления у осмия
Причина стабильности этих состояний заключается в эффективном перекрывании 5d-орбиталей с орбиталями лигандов, что приводит к формированию высокосимметричных и энергетически выгодных структур.
- В простом веществе (Os⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d6 6s2. - В высшем оксиде (Os+8): Металл отдает все 8 валентных электронов. Конфигурация:
[Xe] 4f14.

Рис. 2. Процесс окисления осмия: от плотного металлического состояния до катионов различного заряда вплоть до рекордного значения +8.
Степень окисления осмия в соединениях
В зависимости от агрессивности среды, осмий в соединениях проявляет степень окисления, которая определяет его токсичность, цвет и каталитическую пользу:
- Тетраоксид осмия (OsO4): Os +8, O -2.
- Диоксид осмия (OsO2): Os +4, O -2.
- Гексафторид осмия (OsF6): Os +6, F -1.
- Хлорид осмия(III) (OsCl3): Os +3.
- Пентафторид осмия (OsF5): Os +5.
- Тетракарбонилосмат натрия (Na2[Os(CO)4]): Os -2.
Высшая степень окисления
Высшая степень окисления Os равна +8. Это максимально возможный предел для элементов в земных условиях (наряду с Ru, Ir и Xe).
Низшая степень окисления
Для осмия зафиксирована степень окисления -4 в некоторых редких кластерных соединениях, однако атом осмия имеет степень окисления 0 в виде самого плотного в мире металла — это стандарт для чистого вещества.
Промежуточные степени окисления
Степень окисления осмия в веществах часто принимает значения +2, +3, +5 и +6.
Они менее характерны для водных растворов, но широко представлены в химии комплексных соединений и галогенидов.
Важно: Способность осмия достигать степени окисления осмия формула соединения OsO4 (+8) делает его незаменимым реактивом в органической химии для селективного окисления двойных связей.
Почему осмий может как отдавать электроны (+8), так и принимать (-4)?
Знак заряда и его величина определяются гибкостью d-оболочки и природой партнеров по реакции:
- Положительная СО (+): Характерна при связи с фтором или кислородом, которые «вытягивают» электроны из атома металла.
- Нулевая СО (0): Свойственна для самого твердого и тяжелого представителя платиноидов.
- Отрицательная СО (-): Проявляется в присутствии лигандов, способных эффективно распределять избыточный отрицательный заряд.
4 способа определить степень окисления осмия
По таблице Менделеева
- Семейство: d-элемент (платиновый металл).
- Валентные электроны: 8 (два на 6s-подуровне и шесть на 5d-подуровне).
- Атомная масса осмия: 190,2 а.е.м.
По валентности (Число связей)
Учитывая сложность элемента, валентность осмия может достигать VIII в оксидах и VI в галогенидах.
- В тетраоксиде (OsO4): Осмий образует связи, эквивалентные валентности VIII, СО — +8.
- В диоксиде (OsO2): Металл проявляет валентность IV, СО — +4.
По электронной конфигурации
- Электронная формула осмия: [Xe] 4f14 5d6 6s2.
- Атому осмия степени окисления +8 достичь реально, так как сумма внешних электронов (6+2) равна восьми.
Для анализа распределения электронов по орбиталям используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для OsF6 (фторид осмия VI):
Сумма СО равна 0. Фтор всегда -1. Обозначим Os как x.
x + 6 · (-1) = 0 ⇒ x = +6
Примеры степеней окисления осмия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +8 | Высшая (рекордная). Уникальна для оксидов и фторидов. | OsO4, OsO3F2 |
| +4 | Наиболее устойчивая. Типична для большинства твердых соединений. | OsO2, OsCl4, K2[OsCl6] |
| +2, +3, +6 | Разнообразные. Проявляются в галогенидах и координационных комплексах. | OsCl3, OsF6, OsI2 |
| 0 | Металл. Состояние сверхплотного химического элемента. | Os (металл) |
Шпаргалка для осмия
- +4 и +8 — дуэт наиболее химически значимых состояний.
- Рекордсмен — один из четырех элементов, способных достигать максимальной СО +8.
- Окислитель — тетраоксид осмия (+8) является мощнейшим окислителем в органическом синтезе.
Пример решения задачи:
▶️ Дано:
Соединение: K2[OsCl6] (гексахлоросмат калия).
⌕ Найти:
Определите СО осмия.
✨ Решение:
Калий (K) равен +1, хлор (Cl) равен -1. Уравнение: 2·(+1) + x + 6·(-1) = 0 → 2 + x — 6 = 0 → x = +4.
✅ Ответ:
Os(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: OsO4 крайне токсичен и летуч, требует строгих мер безопасности.
5 — неверно: в специальных комплексах осмий может принимать СО до -4.
Часто задаваемые вопросы
В большинстве твердых соединений наиболее устойчивым считается состояние +4.
В обычных условиях максимум — +8. Сообщения о СО +9 для иридия существуют, но для осмия пределом считается восьмерка.
Появляются отрицательные степени окисления (от -1 до -4) по трем основным причинам:
1. Заполнение d-оболочки: Ему не хватает электронов до полностью заполненного, стабильного состояния «магического» числа электронов (правило 18 электронов).
2. Сильные доноры электронов (Лиганды): В присутствии специфических групп, таких как карбонил (CO), лиганды «накачивают» осмий избыточными электронами. Чтобы стабилизировать этот заряд, металл уходит в «минус».
3. Размер и положение: Осмий — это тяжелый 5d-элемент. Его электронные орбитали очень объемные и гибкие, что позволяет ему удерживать на себе отрицательный заряд гораздо лучше, чем легким металлам.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.