Теория:
Степень окисления иридия (Ir) охватывает уникальный для таблицы Менделеева диапазон от -3 до +9.
Тем не менее наиболее устойчивыми и часто встречающимися значениями являются +3 и +4.
Традиционно выделяют состояние 0, характерное для чистого химического элемента в виде сверхплотного благородного металла.
Например для наиболее стабильной СО +4: в таком соединении, как IrO2 (диоксид иридия), заряд центрального атома металла равен +4.
Для сравнения, СО +3: широко представлена в комплексных солях, например K3[IrCl6] (гексахлороиридат III калия).
- Почему +3 и +4? Иридий — это 5d-элемент 9-й группы. Потеря трех или четырех электронов позволяет сформировать наиболее энергетически выгодные конфигурации в условиях земной химии.
- Почему он так инертен? Высокая энергия связи между атомами в кристаллической решетке и значительная плотность электронного облака делают иридий самым коррозионностойким металлом.
- Рекордная СО +9: В экстремальных условиях синтезирован катион [IrO4]⁺, где иридий проявляет максимально возможную степень окисления среди всех известных элементов.
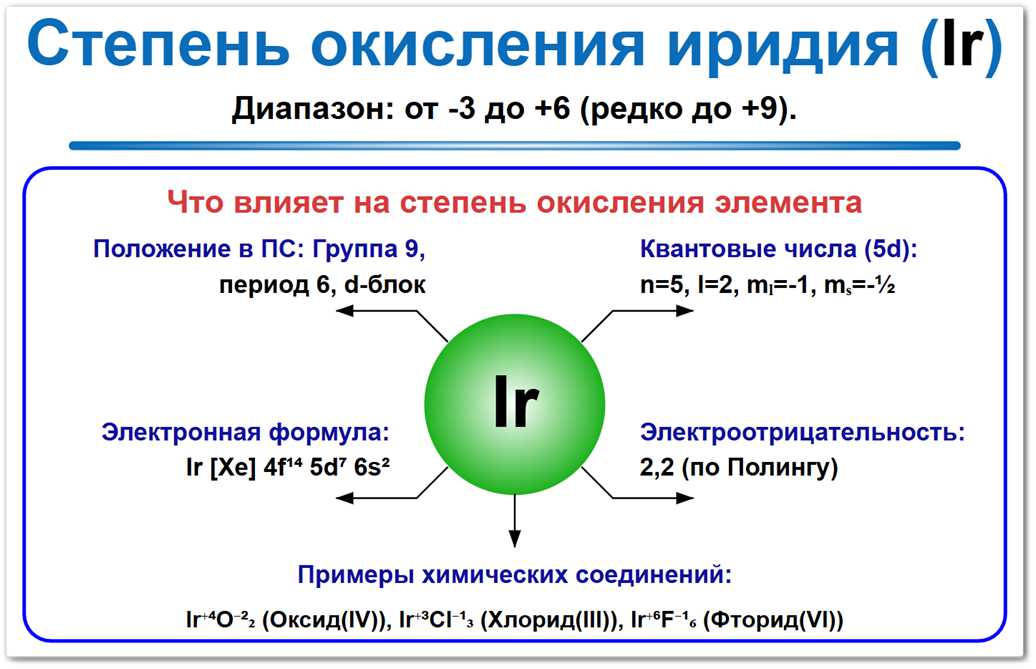
Рис. 1. Разнообразие валентных состояний иридия: от 0 до рекорда +9.
Наиболее устойчивые формы — +3 и +4, определяющие химию большинства его катализаторов и сплавов.
Обратите внимание, что химия иридия тесно связана с его способностью образовывать прочные координационные связи.
Благодаря этому он является незаменимым компонентом в каталитических процессах и свечах зажигания премиального сегмента.
На формирование его уникальных качеств влияют электронная структура (5d7 6s2), эффект лантаноидного сжатия и высокий показатель электроотрицательности 2,2 по шкале Полинга.
Содержание страницы
- 1. Почему +3 и +4 — самые стабильные степени окисления у иридия
- 2. Степень окисления иридия в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему иридий может как отдавать, так и принимать электроны?
- 4. 4 способа определить степень окисления иридия
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления иридия
- 6. Шпаргалка для иридия
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +3 и +4 — самые стабильные степени окисления у иридия
Причина устойчивости этих фаз заключается в оптимальном балансе между энергией ионизации и прочностью образуемых химических связей с лигандами.
- В простом веществе (Ir⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d7 6s2. - В ионе (Ir+4): Иридий теряет 4 электрона. Конфигурация:
[Xe] 4f14 5d5.

Рис. 2. Механизм трансформации иридия: переход от металлического состояния к стабильным катионам за счет изменения числа электронов на внешних орбиталях.
Степень окисления иридия в соединениях
В зависимости от типа химической связи, иридий в соединениях проявляет степень окисления, которая варьируется в очень широких пределах:
- Диоксид иридия (IrO2): Ir +4, O -2.
- Хлорид иридия(III) (IrCl3): Ir +3, Cl -1.
- Гексафторид иридия (IrF6): Ir +6, F -1.
- Тетракарбонилиридат натрия (Na[Ir(CO)4]): Ir -1.
- Оксид иридия(VIII) (IrO4): Ir +8.
Высшая степень окисления
Высшая степень окисления Ir официально зафиксирована на отметке +9 (в катионе [IrO4]⁺). Это абсолютный максимум во всей периодической системе.
Низшая степень окисления
В специфических комплексах для иридия характерна степень окисления -3, при этом стандартный атом иридия имеет степень окисления 0 в твердом металлическом виде.
Промежуточные степени окисления
Степень окисления иридия в веществах может принимать значения +1, +2, +5 и +6.
Эти формы встречаются реже и часто требуют особых условий стабилизации (например, использование фтора или сильных комплексных агентов).
Важно: Иридий — единственный элемент, для которого доказано существование СО +9, что делает его степень окисления иридия формула соединения предметом передовых исследований в квантовой химии.
Почему иридий может как отдавать, так и принимать электроны?
Знак и величина заряда зависят от положения металла в платиновой группе и высокой подвижности электронов на 5d-подуровне:
- Положительная СО (+): Основной тип связи, где иридий выступает типичным металлом-донором.
- Нулевая СО (0): Проявляется в инертных слитках, не реагирующих даже с царской водкой при обычных температурах.
- Отрицательная СО (-): Возможна благодаря высокой электроотрицательности иридия, позволяющей ему удерживать избыточную электронную плотность в присутствии активных лигандов.
4 способа определить степень окисления иридия
По таблице Менделеева
- Семейство: d-элемент (платиновая группа).
- Валентные электроны: 9 (7 на 5d и 2 на 6s-подуровне).
- Атомная масса иридия: 192,2 а.е.м.
По валентности (Число связей)
Наиболее часто валентность иридия составляет IV или III, хотя может достигать и более высоких значений.
- В диоксиде (IrO2): Иридий образует связи, соответствующие валентности IV, СО — +4.
- В хлориде (IrCl3): Металл проявляет валентность III, СО — +3.
По электронной конфигурации
- Электронная формула иридия: [Xe] 4f14 5d7 6s2.
- Атому иридия степени окисления +3 и +4 энергетически наиболее доступны из-за особенностей заполнения d-орбиталей.
Для детального разбора распределения электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для IrF6 (гексафторид иридия):
Сумма СО всех атомов равна 0. Фтор — это всегда -1. Обозначим иридий через x.
x + 6 · (-1) = 0 ⇒ x = +6
Примеры степеней окисления иридия
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4, +3 | Наиболее устойчивые. Основная форма существования иридия в природе и химии. | IrO2, IrCl3, K2IrCl6 |
| +6, +8, +9 | Высшие. Крайне агрессивные и нестабильные формы, рекордные для химии. | IrF6, IrO4, [IrO4]⁺ |
| -3…-1 | Низшие. Характерны для металлоорганических комплексов и кластеров. | [Ir(CO)3]³⁻, Ir(CO)4⁻ |
| 0 | Металл. Состояние чистого самородного иридия. | Ir (слиток) |
Шпаргалка для иридия
- +4 и +3 — ключевые состояния, доминирующие в растворах и оксидах.
- Мировой рекорд — иридий обладает самой высокой степенью окисления (+9) среди всех элементов.
- Инертность — благодаря стабильности своих состояний иридий почти не подвержен действию кислот.
Пример решения задачи:
▶️ Дано:
Соединение: IrCl3 (хлорид иридия III).
⌕ Найти:
Определите СО иридия.
✨ Решение:
Хлор (Cl) как галоген здесь равен -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
Ir(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: иридий является переходным d-металлом, и состояние +1 для него гораздо менее стабильно, чем +3 или +4.
Часто задаваемые вопросы
Наиболее типичные и устойчивые формы — это +3 и +4.
Да, именно иридий удерживает рекорд со значением +9, опережая осмий (+8).
Поэтому эти значения: -3, -1, 0, +1, +2, +3, +4, +5, +6, +7, +8, +9.
Да, в высокоспециализированных карбонильных комплексах иридий способен принимать такую необычную форму.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.