Перекись водорода (пероксид водорода) это бесцветная сиропообразную жидкость плотностью 1,45 г/см3, затвердевающую при —0,48 °С.
Это очень непрочное вещество, способное разлагаться со взрывом на воду и кислород, причем выделяется большое количество теплоты:
2Н2О2 (ж) = 2Н2О (ж) + О2 + 197,5 кДж
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго.
Пергидроль — раствор, который поступает в продажу, — содержит 30% Н2О2.
В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки.
Содержание страницы
Что такое перекись водорода, строение молекулы
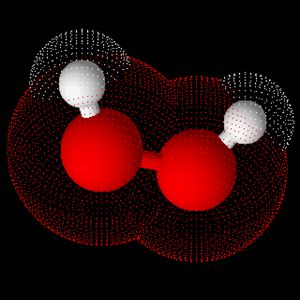
Современной физико- химическими методами установлено, что оба атома кислорода в перекиси водорода H2O2 связаны непосредственно друг с другом неполярной ковалентной связью.
Связи же между атомами водорода и кислорода полярны. Поэтому молекула H2O2 также полярна.
Между молекулами перекиси водорода возникает водородная связь, что приводит к их ассоциации с энергией связи O — O , равной 210 кДж ( 50,48 ккал ).
Что значительно меньше энергии связи H — O ( 470 кДж , или 112,4 ккал ).
Перекись водорода имеет формулу Н2О2.
Физические свойства перекиси водорода
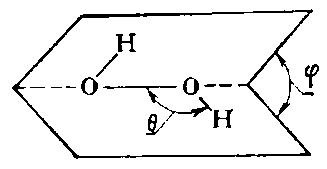
Рис. Схема строения молекулы Н2О2.
Чистая H2O2 — вязкая бесцветная жидкость с плотностью 1440 кг/ м³ и температурой плавления и кипения — 0,46 и 151,4°C.
В пероксиде водорода атомы водорода ковалентно связаны с атомами кислорода, между которыми также осуществляется простая связь.
Строение пероксида водорода можно выразить следующей структурной формулой:
Н—О—О—Н.
Молекулы Н2О2 обладают значительной полярностью (μ = 2,13 D), что является следствием их пространственной структуры (рис).
В молекуле пероксида водорода связи между атомами водорода и кислорода полярны (вследствие смешения общих электронов в сторону кислорода).
Поэтому в водном растворе под влиянием полярных молекул воды пероксид водорода может отщеплять ионы водорода, т. е. он обладает кислотными свойствами.
Химические свойства
Пероксид водорода— очень слабая двухосновная кислота (К1 = 2,6 • 10-12); в водном растворе она распадается, хотя и в незначительной степени, на ионы:
Н2О2 ⇄ Н+ + НО2—
Диссоциация по второй ступени
НО2— ⇄ Н+ + О22—
практически не протекает.
Она подавляется присутствием воды — вещества, диссоциирующего с образованием ионов водорода в большей степени, чем пероксид водорода.
Однако при связывании ионов водорода (например, при введении в раствор щелочи) диссоциация по второй ступени происходит.
В отличие от воды , перекись водорода — непрочное соединение. Она разлагается даже при комнатной температуре и очень легко при освещении или соприкосновении с некоторыми катализаторами ( MnO2 , PbO2 и другие ).
Происходит следующая реакция :
H2O2 = H2O + O
В разбавленном водном растворе перекись водорода значительно устойчивее . Малая устойчивость молекул H2O2 обусловливается непрочностью связи O — O . Перекись водорода смешивается с водой в любых соотношениях. Хранят её в посуде из тёмного стекла и прохладном месте .
При действии на кожу концентрированных растворов перекиси водорода образуются ожоги , причем обожженное место белеет .
Окислительная способность перекиси также обусловливается непрочность связи O — O. Например , йод — крахмальная бумага , содержащая KI и крахмал , при смачивании H2O2 синеет в присутствии выделяемого йода :
2KI + H2O2 = I2 + 2KOH
Таким образом перекись водорода является окислителем по отношению к I . Перекись может выступать и как восстановитель , но только при взаимодействии с сильными окислителями :
Cl2 + H2O2 = 2HCl + O2
Перекись обладает слабыми кислотными свойствами. Это подтверждается её взаимодействием со щелочью :
Ba( OH ) + H2O2 = 2H2O + BaO2 (перекись бария)
Соединение BaO2 — соль перекиси водорода , а не окись бария ( IV ) .
Сопоставим аналогичное по составу кислородные соединения SnO2 и BaО2 , они различаются своим отношением к кислотам , которые из солей перекиси водорода вытесняют перекись водорода :
BaO2 + H2SO4 = BaSO4 + H2O2
SnO2 + 2H2SO4 = Sn(SO4)2 + 2H2O
Разложение пероксида водорода ускоряется катализаторами.
Если, например, в раствор пероксида водорода бросить немного диоксида марганца МnО2, то происходит бурная реакция и выделяется кислород.
К катализаторам, способствующим разложению пероксида водорода, принадлежат медь, железо, марганец, а также ионы этих металлов. Уже следы этих металлов могут вызвать распад Н2О2.
Получение перекиси водорода
Перекись водорода получают электролизом растворов серной кислоты. Концентрированный водный раствор H2O2 фракционированной перегонкой под вакуумом ( вод испаряется легче чем H2O2 ).
Так же перекись можно получить из перекиси бария BaO2 действием на неё разбавленной серной кислоты или углекислым газом под давлением :
BaO2 + CO2 + H2O = BaCO3 + H2O2
Пероксид водорода образуется в качестве промежуточного продукта при горении водорода, но ввиду высокой температуры водородного пламени тотчас же разлагается на воду и кислород.
Однако если направить водородное пламя на кусок льда, то в образующейся воде можно обнаружить следы пероксида водорода.
Пероксид водорода получается также при действии атомарного водорода на кислород.
В промышленности пероксид водорода получают в основном электрохимическими методами, например анодным окислением растворов серной кислоты.
Или гидросульфата аммония с последующим гидролизом образующейся при этом пероксодвусерной кислоты H2S2O8. Происходящие при этом процессы можно изобразить схемой:
2H2SO4 = H2S2O8 + 2Н+ + 2е—
H2S2O8 + 2Н2О = 2H2SO4 + Н2О2
Применение перекиси водорода
Перекись водорода широко используют в качестве окислителя , например, для отбеливания тканей и других материалов.
Разрушая красящие вещества , она почти не затрагивает отбеливаемый материал.
Концентрированная 85 — 95% H2O2 в смеси с некоторыми горючими материалами используют для получения взрывчатых соединений.
Как окислитель чистая перекись применяют в ракетной и реактивной технике , 3 % раствор используют в медицине как дезинфицирующее средство для промывания ран , полоскания горла и так далее .
Применение пероксида водорода связано с его окислительной способностью и с безвредностью продукта его восстановления (Н2О).
Его используют для отбелки тканей и мехов, применяют в медицине (3% раствор — дезинфицирующее средство), в пищевой пром. промышленности (при консервировании пищевых продуктов), в сельском хозяйстве для протравливания семян.
А также в производстве ряда органических соединений, полимеров, пористых материалов. Как сильный окислитель пероксид водорода используется в ракетной технике.
Пероксид водорода применяют также для обновления старых картин, написанных масляными красками и потемневших от времени вследствие превращения свинцовых белил в черный сульфид свинца под действием содержащихся в воздухе следов сероводорода.
При промывании таких картин пероксидом водорода сульфид свинца окисляется в белый сульфат свинца:
PbS + 4Н2О2 = PbSO4 + 4Н2О
Соли пероксида водорода
С некоторыми основаниями пероксид водорода реагирует непосредственно, образуя соли.
Так, при действии пероксида водорода на водный раствор гидроксида бария выпадает осадок бариевой соли пероксида водорода:
Ва(ОН)2 + Н2О2 = ВаО2↓ + 2Н2О
Соли пероксида водорода называются пероксидами или перекисями.
Они состоят из положительно заряженных ионов металла и отрицательно заряженных иоиов О22— , электронное строение которых можно изобразить схемой:
Как окислитель
Степень окисленности кислорода в пероксиде водорода равна —1, т. е. имеет промежуточное значение между степенью окисленности кислорода в воде (—2) и в молекулярном кислороде (0).
Поэтому пероксид водорода обладает свойствами как окислителя, так и восстановителя, т. е. проявляет окислительно-восстановительную двойственность.
Все же для него более характерны окислительные свойства, так как стандартный потенциал электрохимической системы
Н2О2 + 2Н+ + 2е— = 2Н2О
в которой Н2О2 выступает как окислитель, равен 1,776 В, в то время как стандартный потенциал электрохимической системы:
О2 + 2Н+ + 2е— = Н2О2
в которой пероксид водорода является восстановителем, равен 0,682 В.
Иначе говоря, пероксид водорода может окислять вещества, φ° которых не превышает 1,776 В, а восстанавливать только те, φ° которых больше 0,682 В.
В качестве примеров реакций, в которых Н2О2 служит окислителем, можно привести окисление нитрита калия:
KNO2 + Н2О2 = KNO3 + Н2О
и выделение иода из иодида калия:
2KI + Н2О2 = I2 + 2КОН
Как восстановитель
Как пример восстановительной способности пероксида водорода укажем на реакции взаимодействия Н2О2 с оксидом серебра(I)
Ag2O + Н2О2 = 2Ag + Н2О + О2
а также с раствором перманганата калия в кислой среде:
2КМnО4 + 5Н2О2 + 3H2SO4 = 2MnSO4 + 5О2 + K2SO4 + 8Н2О
Если сложить уравнения, отвечающие восстановлению пероксида водорода и его окислению, то получится уравнение самоокисления-самовосстановления пероксида водорода:
(Н2О2 + 2Н+ + 2е— = 2Н2О) + (Н2О2 = О2 + 2Н+ + 2е—) → (2Н2О2 = 2Н2О + О2)
Это — уравнение процесса разложения пероксида водорода.
Вопросы и ответы?
Что будет если выпить перекись водорода?
Пить перекись водорода категорически запрещено, так как она является сильным окислителем, то есть даже 3% раствор может привести к ожогам ЖКТ.
Для чего можно применять перекись водорода?
Перекись водорода — это антисептическое средство из группы антиоксидантов. При контакте перекиси водорода с поврежденной кожей или слизистыми оболочками высвобождается активный кислород.
При этом происходит механическое очищение и инактивация органических веществ.
Что убивает перекись водорода?
Перекись водорода убивает грибки, бактерии, вирусы и споры плесени.
Статья на тему перекись водорода

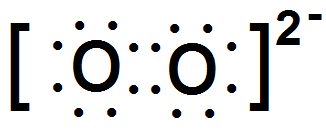
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.