Проверка выполнения заданий и ответов на вопросы к гл. I
1. 16; 61; 14; 42.
2. Различие в атомном весе разных изотопов одного и того же элемента объясняется разным числом нейтронов в ядре.
3—4. Ответы на эти вопросы вы найдете; прочитав текст на стр. 12.
5. Вычитая из атомного веса число нейтронов» мы получим число протонов 24—12 = 12. Число протонов равно величине заряда ядра. Заряд ядра соответствует порядковому номеру элемента. Элемент № 12 — магний,
6. Ответ на этот вопрос содержится в тексте на стр. 13.
7. s-Оболочка — это электронная оболочка сферической формы, состоящая из s-орбитали. На одной и той же s-оболочке может находиться не более 2 электронов.
8. Да. можно. s-оболочка может содержать только одну s-орбиталь, на которой могут размещаться 1 или 2 электрона.
9. р-Оболочка содержит 3 взаимноперпендикулярных р-орбитали гантелевидной формы. На р-оболочке может располагаться не более 6 электронов. 11—12.Внимательно прочтите текст на стр. 15—16. Там вы найдете ответы на эти вопросы. 13. К, L, М; N; О; Р; Q.
14. Знать значение главного квантового числа необходимо для того, чтобы определить, о каком энергетическом уровне говорится и сколько на нем может размещаться электронов.
15. 2n2, где n — главное квантовое число, численно равное порядковому номеру электронного слоя.
17—18. Ответы на эти вопросы найдите в тексте на стр. 17.
19. Наиболее Энергетически выгодна сферическая s-оболочка.
20. Конфигурация уровней К и L такая же. как у кремния (напишите самостоятельно). Конфигурация уровня М3s23p3;
21. Электронная конфигурация атома, натрия Na 1s22s22p63s1
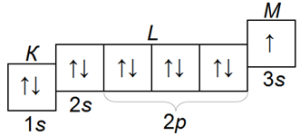
У натрия в процессе завершения 3s-оболочка, следовательно, он относится к s-элементам.
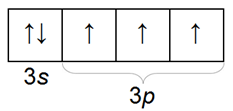
22. Электронная конфигурация атома кремния Si 1s22s22p63s23p2. Распределение электронов по орбиталям изображено на странице, 3р-электроны размещены на двух орбиталях, а не на одной, так как это энергетически выгоднее.
23. Sc, Ti, V, Cr, Mn, Fe, Co, Ni.
24. Приведем конфигурацию цинка Zn (уровни M и N) 3s23p63d104s2.
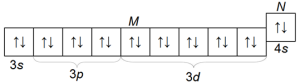
Электронные конфигурации остальных элементов изобразите самостоятельно.
25. Мы изобразим конфигурации N и O-слоев иттрия Y 4s24p64d15s2
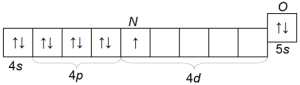
кадмия Cd 4s24p64d105s2
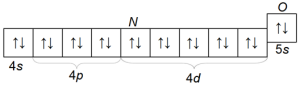
ксенона Xe 4s24p64d105s25p6
Остальные изобразите самостоятельно.
26. С возрастанием порядкового номера увеличивается число электронов во внешних электронных слоях. В связи с этим происходит уплотнение на орбиталях, «сжатие» электронных оболочек, уменьшается радиус атома, усиливается электроотрицательность. Все это ведет к усилению неметаллических свойств. При завершении внешнего электронного слоя до октета образуются атомы инертных элементов.
27. Чем больше радиус атома, тем ярче выражены металлические свойства.
28. Инертные элементы имеют завершенный «октет» электронов на внешнем слое.
29. Периодическая повторяемость свойств объясняется периодической повторяемостью электронных конфигураций внешнего и предвнешнего слоев.
30. В группах с возрастанием зарядов ядер увеличиваются атомные радиусы, электроотрицательность уменьшается, поэтому металлические свойства усиливаются.
31. У титана более ярко выражены металлические свойства, так как радиус его атома больше, чем у хрома.
32. Фосфор имеет меньший атомный радиус, большую электроотрицательность, у него неметаллические свойства выражены ярче, чем у висмута.
33. Сначала изобразите электронные конфигурации атомов хрома и селена (сделайте это самостоятельно). Хром — элемент побочной подгруппы — принадлежит к семейству d-элементов. а селен — к р-элементам. Этим обусловлено различие в свойствах.
34. Кальций имеет незастроенную d-оболочку предвнешнего слоя М и его 45-электроны в атоме удерживаются значительно слабее, чем у цинка, имеющего завершенный до 18е— предвнешний слой.
35. Атом хлора имеет семиэлектронный внешний слой :
При образовании двухатомной молекулы между атомами хлора образуется одна общая электронная пара
Образование молекулы кислорода объясните самостоятельно.
36. В молекуле H2S образуется ковалентная связь между атомом серы: и два атома Н· с сильным смещением электронных пар к более электроотрицательному атому серы. Образуется диполь
Молекула НВr образуется по такому же типу, что и НСl. Изобразите схему образования НВr самостоятельно.
37. Ионная связь между атомами К и Br возникает при передаче электрона от атома калия к атому брома
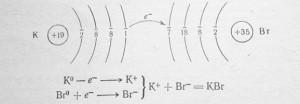
Ионная связь между атомами натрия Na и серы S в Na2S

Образование нитрида магния Mg3N2 объясните самостоятельно.
38. Ионные: ZnCl2. CaS; полярные: НВr, Н2О, СО, РН3; неполярные: SiH4, ССl4.
Схемы строения этих молекул изобразите самостоятельно.
39. Вода имеет молекулярную кристаллическую решетку, которая разрушается гораздо легче, чем атомная решетка углерода.
40. Низкие температуры плавления характерны для веществ с молекулярными кристаллическими решетками.
41. Ответ на вопрос найдите в тексте параграфа.
42. Nb — 5, Ga — 3, Тс — 7.
43. Sn-4, Sb —5, Tl — 3
44. CdO, Ga2O3,HfO2.
46. N2O5, CO2, Li2O.
46. Основные окислы: СаО — окись кальция; FeO — окись железа (II); MnO — окись марганца (II); CuO — окись меди (II); Na2O — окись натрия, Fe2O3 — окись железа (III) Кислотные окислы: SiO2—окись кремния (IV);СO2-окись углерода (IV); Р2О5 — окись фосфора (V); SO3— окись серы (VI); V2O5 — окись ванадия (V); ТiO2 — окись титана (IV). Амфотерные окислы: РbО —окись свинца (II).
47. 22 г СO2.
48. 0,5 г-мол CuO.
49. 392 г H2SО4.
50. 5,6 л О2.
O2 HCl
51. Pb → PbO → PbCl2
O2 NaOH
Pb → PbO → Na2PbO2
Полные уравнения реакций и уравнения в ионной форме напишите самостоятельно.
52. a) Cu2О; b) SiО2. Остальные найдите самостоятельно.
53. Окись бария вступит в реакцию с водой, азотной и фосфорной кислотами, двуокисью серы. Уравнения напишите самостоятельно.
54. Сначала следует определить, к какому классу относится вещество, которое требуется получить, затем искать план решения.
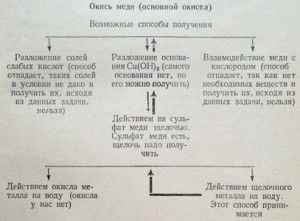
Теперь можно жирными стрелками показать путь получения окиси меди.
55. SrO, In2О3.
Вступают в реакцию с серной кислотой:
HgSO4 + SrO = SrSO4 + H2O
ln2O3 + 3H2SO4 = In2(SO4) + 3H2O
Оба окисла — основного характера, амфотерных свойств SrO не проявляет, а In2O3, проявляет в значительной степени, поэтому с NaOH реагирует.
56. RbОН, Ва(ОН)2, La(OH)3
57. RbOH + HNO3 =RhNO3 + Н2O
Ва(ОН)2 + 2НСl = BaCl2 + 2H2O
68. Зная, что селен располагается в конце IV периода, мы можем заключить, что это окисел кислотный. Ему отвечает гидроокись, представляющая собой кислоту, формулу которой несложно найти либо по аналогии с серой, либо мысленно прибавив Н2O к SeO3: H2SeO4.
SeO3 + Са(ОН)2 = CaSeO4 + Н2O
SeO3 + Na2O = Na2SeO4
59. H2SeO4 + 2RbOH = Rb2SeO4 + 2H2O
H2SeO4 + K2O = K2SeO4 + H2O
H2SeO4 + Ba(OH)2 = BaSeO4 + 2H2O
H2SeO4 + CaO = CaSeO4 + H2O.
60. H2TeO4; HClO4; для германия и хрома найдите самостоятельно
61. Ответьте на вопрос самостоятельно.
62 Si — 4; Р—3. Остальное определите самостоятельно.
63AsH3, НВr. Остальное — самостоятельно.
Учтите, что у элементов IV и V групп водород в формуле ста-вится на второе место, а у элементов VI и VII групп — на первое. Если вы допустили ошибку в написании, исправьте ee.
64. Ответьте на вопрос самостоятельно с использованием периодической системы элементов.
65а)SnCl4; б) InBr3;e) CdS.
Остальное выполните самостоятельно.
66. Са(МnO4)2 — марганцовокислый кальций (перманганат кальция) формулу мышьяковокислого рубидия напишите самостоятельно.
67 На этот вопрос дайте ответ самостоятельно.


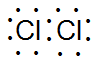
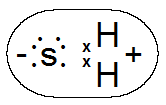
Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.