Дисперсионная система это гетерогенная система, которая состоит из одного или двух веществ в виде частиц.
Которые практически не смешиваются и не реагируют друг с другом химически.
Примером может служить окружающий нас воздух в котором растворены кислород, азот, углекислый газ и другие.
Эти системы можно разделить на три: грубодисперсные системы, коллоидные растворы, истинные растворы.

Содержание страницы
- 1. Что такое дисперсные системы
- 1.1. Суспензия — эмульсия
- 1.2. Растворимое вещество и растворитель
- 1.3. Процесс растворения
- 1.4. Как растворяются вещества
- 1.5. Сольватно гидратная теория
- 1.6. Растворимость
- 1.7. Растворимость веществ при нагревании
- 1.8. Растворимость стекла в воде
- 1.9. Перенасыщенные растворы
- 1.10. Концентрация растворов
- 1.11. Быстрые ответы?
Что такое дисперсные системы
Если одно вещество мелко раздроблено и равномерно распределено в другом веществе, возникает дисперсная система.
Раздробленное вещество называется дисперсной фазой, а вещество, в котором распределена дисперсная фаза, дисперсионной средой.
Дисперсные системы могут быть различными по агрегатному состоянию.
Воздух, например, является типичной газообразной дисперсной системой, состоящей из газообразного кислорода, азота, двуокиси углерода и др.
Сплавы металлов — типичные твердые дисперсные системы. Жидкие дисперсные системы образуются в жидкой дисперсионной среде.
Мы будем заниматься в основном жидкими дисперсными системами. Дисперсионной средой в таких системах могут быть вода, спирт, керосин, бензол и другие жидкости.
Дисперсной фазой могут являться как твердые вещества, так и жидкости и газы.
Дисперсные системы можно разделить на три группы:
1) Грубодисперсные системы (взвеси).
2) Коллоидные растворы.
3) Истинные растворы.
Это зависит от размеров частиц дисперсной фазы. Если их размер превышает 100 ммк, образуются грубодисперсные системы — суспензии или эмульсии.
Суспензия — эмульсия
Суспензии получаются, если дисперсная фаза твердая, а эмульсии — если она жидкая.
Например, если взболтать в воде глину или сильно измельченный мел, то получается мутная смесь, которая очень медленно отстаивается. Это и есть суспензия.
Примером эмульсии может служить молоко, где дисперсной фазой являются капельки жира.
Следует заметить, что образование эмульсии имеет определенное физиологическое значение, так как жир в виде эмульсии легче усваивается организмом.
Этим объясняется эмульгирующая функция желчи, выделяемой печенью.
Грубодисперсные системы не пропускают лучи света, частицы их достаточно крупны, их можно увидеть в микроскоп. Суспензии можно фильтровать через бумажный фильтр.
Как суспензии, так и эмульсии обычно более или менее быстро расслаиваются при хранении.
В отличие от них коллоидные растворы значительно более устойчивы. В них величина частиц дисперсной фазы колеблется в пределах от 1 до 100 ммк.
Наиболее устойчивы среди дисперсных систем так называемые истинные, или молекулярные, растворы, в которых величина частиц дисперсной фазы не превышает 1 ммк.
Как правило, в таких растворах дисперсная фаза раздроблена до молекул или до ионов.
➡️ 1. Для получения некоторых лаков приготовляют дисперсную систему из красителя и ацетона. Что является при этом дисперсной фазой и что дисперсионной средой?
2. В чем отличие взвесей от коллоидных растворов и истинных растворов? (См. Ответ)
Растворимое вещество и растворитель
Обязательными компонентами любого раствора являются растворитель и растворенное вещество.
Растворителем обычно называют компонент, агрегатное состояние которого такое же, как у раствора в целом.
В практике чаще пользуются растворами, в которых растворителя гораздо больше, чем растворенного вещества.
Растворенные вещества могут быть взяты в любом агрегатном состоянии. Кроме того, в одном растворе может быть растворено несколько веществ.
Типичным примером такого раствора служит морская вода. В нашем курсе мы будем рассматривать только такие растворы, где растворителем является вода.
Процесс растворения
Если взять, например, поваренную соль или сахар, или марганцовокислый калий и поместить их в воду, то мы заметим, как количество твердой соли или другого вещества постепенно уменьшается — идет растворение.
При этом вода, в которой растворилось вещество, изменяет свои свойства она приобретает вкус, окраску, изменяются ее температура кипения замерзания, удельный вес, электропроводность и т. д.
Изменяют свойства и растворяемые вещества. Они уже не являются твердыми. Сухая поваренная соль, например, не проводит электрический той, вода тоже не проводит ток, а водный раствор поваренной соли электро-проводен.
При растворении очень часто наблюдается выделение или поглощение тепла. Причиной этого являются различные физические и химические процессы, происходящие при растворении.
Примером может служить нитрат аммония и гидроксид натрия.
При растворении в воде нитрата аммония раствор сильно охлаждается, а гидроксид натрия нагревается.
Однако если выпарить из раствора воду, то можно опять получить поваренную соль, причем в том же количестве, что и до растворения.
Возникает вопрос можно ли рассматривать растворы как механические смеси? Но в механических смесях каждый компонент сохраняет свои свойства, а в растворах свойства компонентов меняются.
Исходя из этого, а также из того, что в растворе могут происходить химические реакции, Д. И. Менделеев предложил рассматривать растворы:
«…как жидкие, непрочные, определенные химические соединения в состоянии диссоциации».
Вместе с тем растворы нельзя считать химическими соединениями в полном смысле этого слова, так как раствор одного и того же вещества может иметь разный количественный состав, а у химического соединения состав постоянный.
Другими словами, количество растворенного вещества и растворителя в растворе может быть различным.
Таким образом, растворами можно назвать физико-химические дисперсные системы, состоящие из двух или нескольких веществ и их непрочных химических соединений.
➡️ 3. Какой из компонентов раствора следует считать растворителем?
4. Можно ли считать растворы механическими смесями? Почему?
5. Можно ли считать растворы химическими соединениями? Почему? (См. Ответ)
Как растворяются вещества
При растворении частицы растворяемого вещества со всех сторон окружаются молекулами растворителя.
Между молекулами растворяемого вещества и растворителя начинают активно действовать силы межмолекулярного притяжения, которые, в конце концов, преодолевают силы сцепления между молекулами растворяемого вещества и отрывают их друг от друга.
При этом молекулы растворяемого вещества вследствие диффузии постепенно равномерно распределяются по всему объему раствора.
Такова сущность процесса растворения в простейшем случае, если бы между растворителем и растворенным веществом не происходило химических процессов.
При растворении твердых веществ разрушение кристаллической решетки растворяемого вещества и распределение его молекул в большом объеме всегда сопровождается поглощением тепла и влечет за собой охлаждение раствора.
Если, например, поместить в стакан с водой кристаллы аммиачной селитры NH4NО3 и поставить стакан на кусочек влажного картона, то картон примерзнет к стакану, так как температура раствора падает ниже 0°.
➡️6. Объясните, в чем сущность процесса растворения.
7. Почему процесс растворения является эндотермическим процессом? (См. Ответ)
Сольватно гидратная теория
При растворении в воде серной кислоты или щелочи раствор очень сильно разогревается и может даже закипеть.
Выделение тепла нельзя объяснить, если рассматривать растворение как простое смешивание.
Объяснение этому явлению дает гидратная теория растворов Д. И. Менделеева.
Как уже говорилось, Д. И. Менделеев рассматривал процесс растворения как сложное взаимодействие растворителя и растворенного вещества.
Изучая свойства водных растворов серной кислоты, спирта и ряда других веществ, Д. И. Менделеев пришел к выводу.
Что растворы представляют собой системы, состоящие не только из растворителя и растворенного вещества, но и из продуктов их взаимодействия — гидратных соединений различного состава — гидратов.
Объясняя это явление, Д. И. Менделеев предположил, что в растворе между молекулами растворяемого вещества и растворителя возникают силы межмолекулярного притяжения.
В результате чего происходит, как было указано выше, растворение и молекулы растворенного вещества оказываются окруженными оболочкой из молекул растворителя.
Такая оболочка называется сольватной. Если растворителем является вода, то оболочка называется гидратной.
Гидратная оболочка иногда настолько прочно удерживается молекулой растворенного вещества, что не разрушается даже при выпаривании раствора, а образует химические соединения — кристаллогидраты, например CuSО4 · 5H2О.
Процессу образования гидратов — химический процесс, сопровождающийся выделением тепла.
В уже упомянутом примере с аммиачной селитрой также происходит процесс гидратации, но эндотермические процессы преобладают.
➡️8. Чем отличаются тепловые явления, происходящие при растворении серной кислоты, от тепловых явлений при растворении аммиачной селитры?
9. Как объясняет явления, названные в предыдущем вопросе, гидратная теория растворов Д. И. Менделеева? (См. Ответ)
Растворимость
Большинство твердых веществ не может растворяться в каком-то определенном объеме воды в неограниченном количестве.
Всякий раз мы замечаем, что при растворе- нии наступает такой момент, когда вещество перестает растворяться, добавленный избыток его выпадает из раствора в виде осадка.
Такой раствор, в котором при данных условиях взятое вещество больше не растворяется, называется насыщенным раствором.
Количество растворенного вещества, Необходимое для образования насыщенного раствора, при одних и тех же условиях у разных веществ различно.
Например, в 100 г воды при 0° может раствориться не больше 15 г нитрата калия или не больше 30 г нашатыря, или не больше 15 г медного купороса, при 20° — 33 г нитрата калия, 37 г нашатыря, 20 г медного купороса и т. д.
Количество вещества (в граммах), образующее при данных условиях насыщенный раствор в 100 г растворителя (воды), называется коэффициентом растворимости.
Растворимость — одна из количественных характеристик вещества. С изменением температуры или давления растворимость меняется.
Зависимость растворимости некоторых твердых веществ от температуры представлена на рис. 13.
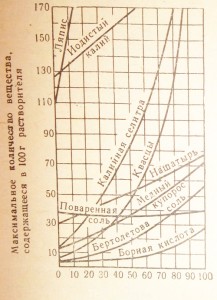
10. Пользуясь кривой, приведенной на рис. 13, определите растворимость нашатыря при 50°, бертолетовой соли при 90°, медного купороса при 85°.
11. Рассчитайте растворимость квасцов при 50°, если из 75 г раствора, насыщенного при этой температуре, можно выделить 25 г соли.
Растворимость веществ при нагревании
Как правило, с повышением температуры растворимость твердых веществ резко возрастает.
Например, растворимость нитрата калия при 0° составляет 10 г в 100 г воды, при 45°—75 г, при 60°— 110 г, а при 80° — 130 г. Но есть и исключения.
Рис. 13. График зависимости растворимости некоторых твердых веществ от температуры.
Так, растворимость сульфата натрия до 32° возрастает, а затем слегка понижается. Аналогично ведет себя весьма плохо растворимый сульфат кальция.
Многие жидкости, как правило, смешиваются с водой в любых соотношениях уже при обычных условиях.
| Зависимость растворимости в воде некоторых газов от температуры. Таблица 3 | ||
| Газ | Растворимость (объем газа в одном объеме воды) | |
| 0° | 20° | |
|
Кислород Азот Двуокись углерода Аммиак |
0,0492 0,0235 0,0215 1,713 1200 |
0,0310 0,0154 0,0182 0,878 700 |
К ним относятся сильные минеральные кислоты, спирт. Однако имеется большое количество жидкостей, нерастворимых в воде: анилин, бензол, масла и т.д.
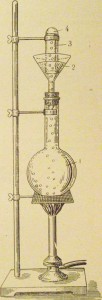
Растворимость газов в воде в противоположность растворимости твердых веществ понижается с ростом температуры (таблице). Это можно наблюдать на опыте (рис. 14).
В колбу 1 наливают доверху воду и вставляют пробку с воронкой 2, в которой также имеется немного воды В воронку опрокинута заполненная холодной водой пробирка 3, которая прикрывает Отверстие воронки.
При нагревании воды растворимость в ней воздуха понижается и избыток его в виде пузырьков собирается в пробирке.
Растворимость газов в зависимости от температуры приведена в табл. 3.
Следует отметить, что растворимость большинства газов в воде вообще гораздо ниже, чем растворимость твердых веществ.
Исключение составляют газы, вступающие с водой в химические реакции: аммиак, двуокись углерода, двуокись серы, хлористый водород и др. Растворимость газов тем больше чем выше давление.
На этом свойстве газов основано применение двуокиси углерода для изготовления шипучих напитков. При высоком давлений воду насыщаю двуокисью углерода.
В дальнейшем при откупориваний бутылки давление резко понижается и избыток газа выходит в виде пузырьков и вспенивает воду.
Рис. 14. Прибор для наблюдения уменьшения растворимости воздуха с повышением температуры
1 — колба с водой; 2 — воронка с водой; 3 — пробирка с водой для собирания воздуха, выделяющегося из воды при нагревания; 4 — пузырек воздуха.
Растворимость твердых веществ зависит также от природы самого вещества.
Среди веществ различают вещества, хорошо растворимые в воде (NaCl, KNO3, NaOH, КОН, FeSO4, FeCl3, MgCl2, KI), малорастворимые (CaSO4) и практически нерастворимые (BaSО4, AgCl, AgI, AgBr, CaCO3).
Это показано в таблице растворимости кислот, оснований и солей в воде.
Растворимость стекла в воде
Всякое вещество хотя в самой малой степени, но растворимо.
Например , если взять кусок стекла и поместить в воду, то растворение его обнаружить не удается, но мелкая стеклянная пыль заметно растворима.
Если ее смешать с водой, то с помощью фенолфталеина можно обнаружить в растворе щелочь, так как в состав стекла входят соединения щелочных металлов.
Растворимость сульфата бария, хлорида серебра при обычных условиях еще меньше, но все-таки и они в какой-то степени растворимы.
➡️12. Как влияет давление на растворимость газов в воде?
13. Какие причины могут оказывать влияние на растворимость твердых веществ и газов в воде?(См. Ответ)
Перенасыщенные растворы
Некоторые твердые вещества в отдельных случаях могут образовать перенасыщенные, или пересыщенные растворы, в которых растворенного вещества содержится больше, чем достаточно при данных условиях для насыщения.
Получить такие растворы можно при очень медленном, осторожном охлаждении горячего концентрированного раствора.
В какой-то момент температура раствора станет такой, при которой он в соответствии с растворимостью вещества становится насыщенным, а избыток вещества должен выпасть в осадок в виде кристаллов.
Этого может не произойти, если отсутствуют так называемые центры кристаллизации. В этом случае в растворе вещества удерживается больше, чем требуется для насыщения, и раствор является пересыщенным.
Пересыщенный раствор — весьма нестойкая система: от легкого толчка или попадания очень малого инородного тела (например, пылинки), которое может послужить центром кристаллизации.
Из него мгновенно выпадает в осадок избыток растворенного вещества, а раствор становится насыщенным — переходит в устойчивое состояние.
➡️14. В чем отличие пересыщенного раствора от насыщенного?
15. При каких условиях может образовываться пересыщенный раствор? (См. Ответ)
Концентрация растворов
Зная растворимость вещества, можно достаточно точно определить количественный состав насыщенного в данных условиях раствора этого вещества.
Если речь идет о ненасыщенном растворе, то эта точность сразу исчезает.
Такой раствор может содержать любые количества растворенного вещества, но только меньшие, чем требуется для насыщения раствора.
Столь же неточными являются понятия «концентрированный» и «разбавленный» растворы, которые тем не менее имеют широкое хождение в лабораторной практике.
Для точного определения количественного состава раствора вводится понятие концентрации раствора.
Концентрация раствора показывает, какое количество растворенного вещества содержится в определенном весовом или объемном количестве раствора.
Концентрация является одной из важнейших характеристик раствора.
Существует несколько способов выражения концентрации растворов. Иногда, особенно в случае кислот, мы встречаем на этикетках обозначения 1 : 2, 1 : 6, 1 : 10 или 1 ; 22.
Это значит, что поступившая в лабораторию концентрированная кислота была смешана с водой в соответствующей пропорции: на 1 объем кислоты было взято 2, б, 10 или 12 объемов воды.
Здесь уже есть какое-то количественное указание, однако и оно не является достаточно точным.
Более точно выражать концентрацию в процентах, в молях на литр и в грамм-эквивалентах на литр.
Первая называется процентной, вторая — молярной, а третья — нормальной концентрацией.
Процентная концентрация представляет собой весовую, а молярная и нормальная — объемные концентрации. Концентрация условно обозначается буквой С.
➡️16. Перечислите и запишите в тетрадь способы выражении концентрации растворов.
17. Какими путями ненасыщенный раствор можно сделать насыщенным? (См. Ответ)
Быстрые ответы?
Образования из фаз (тел), которые практически не смешиваются и не реагируют друг с другом химически.
В типичном случае двухфазной системы первое из веществ (дисперсная фаза) мелко распределено во втором (дисперсионная среда).
Классифицируют по агрегатному состоянию образующих систему фаз. В зависимости от размера частиц дисперсные системы подразделяют на грубодисперсные (взвеси).
Состоящие из частиц размером свыше 1000 нм, и тонкодисперсные (коллоидные системы, коллоиды) с размерами частиц от 1 до 1000
По степени раздробленности (дисперсности) системы делятся на следующие классы:
1) Грубодисперсные, размер частиц в которых более 10-5 м.
2) Тонкодисперсные (микрогетерогенные) с размером частиц от 10-5 до 10-7 м.
3) Коллоидно-дисперсные (ультрамикро-гетерогенные) с частицами размером от 10-7 до 10-9м.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.