Уран это химический элемент с порядковым номером 92 и обозначением U. Это металл из группы актиноидов периодической системы имеет цвет серебристо-серый.
Атом урана содержит 92 протона и 92 электрона, в том числе 6 валентных электронов. Уран обладает радиоактивными свойствами, в основном испуская альфа-частицы.
Период полураспада урана может варьироваться от 159 200 до 4,5 миллиардов лет в зависимости от изотопа, что делает его полезным для определения возраста земли.
Наиболее распространенными природными изотопами урана являются уран-238 (содержащий 146 нейтронов) и уран-235 (содержащий 143 нейтрона).
Уран обладает самым высоким атомным весом среди всех естественных элементов. Его плотность превышает плотность свинца на 70%, но немного ниже, чем у золота или вольфрама.
Встречается уран в виде низких концентраций в почвах, горных породах и воде, и его добывают коммерчески из уранин содержащих минералов, таких как уранинит.
Содержание страницы
Что такое уран
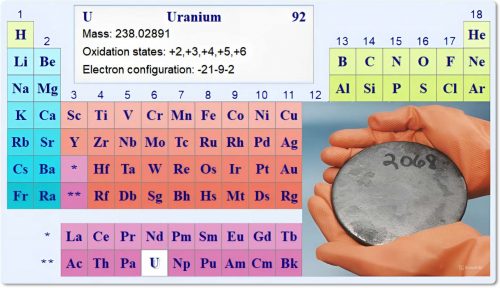
(Uranium; от назв. планеты Уран), U — радиоактивный химический элемент 3 группы ( устаревшая классификация: III В группы) периодической системы элементов.
Атомный номер 92, Атомная масса 238,029; относится к актиноидам.
Серебристо-белый блестящий металл. В соединениях проявляет степени окисления от +2 до +6, наиболее характерны +4 и +6.
Изотопы
Природный Уран состоит из изотопов 238U (99,282%), 235U (0,712%) и 234U (0,006%). Среди искусственных изотопов практическое значение имеет изотоп 233U.
В виде окисла UО2 открыл (1789) нем. химик М.-Г. Клапрот.
История
Металлический уран получил (1841) франц. химик Э.М. Пелиго. С 40-х гг. 20 в. У. приобрел значение как источник ядерной энергии, выделяющейся в процессе деления его атомов при захвате нейтронов; этим св-вом обладают изотопы 235U и 233U .
Изотоп 238U при захвате нейтронов превращается в плутоний (239Рu), к-рый также является ядерным горючим. Содержание урана в земной коре 0,3—0,0004%.
Нахождение в природе
Главным его минералом является разновидность уранита — настуран (урановая смолка) (40—76% U).
В малых количествах уран содержится в гранитах (0,0004%), в почвах (0,0001 — 0,00004%) и водах ( ~10-8%).
Физические свойства
Известны три его аллотропические модификации:
- Альфа-уран с ромбической кристаллической решеткой и с периодами а = 2,8541 А, b = 5,8692 А и с = 4,9563 А (т-ра 25° С), к-рый переходит при т-ре 667,7° С в бета-уран.
- Бета-уран с тетрагональной кристаллической решеткой и с периодами а = 10,759 А и с = 5,656 A (т-ра 720° С).
- Выше т-ры 774,8° С устойчив гамма-уран с объемноцентрированной кубической, решеткой и с периодом а = 3,524 А (т-ра 805° С).
Плотность альфа-урана при комнатной т-ре 19,05 г/см3; tпл 1132° С; tкип 3820° С (давление 1 ат).
Теплоты превращений альфа ⇄ бета, бета ⇄ гамма, плавления и испарения уран соответственно ~ 0,70; 1,15; 4,75 и 107—117 ккал/моль. Теплоемкость с = 6,4 кал/моль (т-ра 25° С).
Средний коэфф. термического расширения альфа-урана по осям a, b и с в интервале т-р 20—500° С соответственно 32,9; — 6,3 и 27,6 • 10-6 град-1.
Коэффициент теплопроводности урана при комнатной т-ре ~ 0,06 кал/см • сек • град и увеличивается с ростом т-ры.
Электрическое сопротивление альфа-урана зависит от кристаллографического направления; усредненная его величина уран поликристаллического образца высокой чистоты ~ 30 мком х см при комнатной т-ре и увеличивается до ~ 54 мком х см при т-ре 600° С.
У альфа-урана наблюдается также анизотропия модуля Юнга. У поликристаллического альфа-урана модуль Юнга 2,09 х 10 4 кгс/мм2; модуль сдвига 0,85 х 10 4 кгс/мм2; коэфф. Пуассона 0,23.
Твердость альфа-урана при комнатной т-ре HV = 200, но снижается до 12 при т-ре 600° С.
При переходе из альфа- в бета-уран твердость увеличивается от ~ 10 до ~ 30. Предел прочности на растяжение отожженного альфа-урана (0,02% С) при т-ре 20° С составляет ~ 42 кгс/мм2, увеличивается до 49 кгс/мм2 при т-ре 100 9 С и затем почти линейно снижается до ~ 11 кгс/мм2 с повышением т-ры до 600° С.
При т-ре 20° С предел текучести, относительное удлинение и относительное сужение соответственно 26 кгс/мм2, 8 и 11%, а при т-ре 600° С — 9 кгс/мм2, 26 и 65%.
Увеличение содержания углерода от 0,01 до 0,20% повышает пределы прочности и текучести σ 0,2 соответственно от 37 и 24 до 52 и 32 кгс/мм2.
Все механические характеристики уран существенно зависят от наличия примесей и предварительной обработки.
Ползучесть урана особенно зависит от циклических изменений т-ры, что связано с дополнительными термическими напряжениями, возникающими из-за большой разницы коэфф. термического расширения по различным кристаллографическим направлениям альфа-урана.
Ударная вязкость альфа-урана (0,03% С), невысокая при т-рах 20 и 100° С (соответственно 1,4 и 2,3 кгс-м/см2), увеличивается почти линейно до 11,7 кгс-м/см2 при т-ре 500° С.
Характерной особенностью является удлинение прутков поликристаллического альфа-урана с текстурой [010] вдоль оси под влиянием повторяющихся нагревов и охлаждений.
При делении атомов урана образуются ксенон и криптон, нерастворимые в уране, что приводит к распуханию металла (весьма нежелательному для ядерного горючего).
Химические свойства
Даже при комнатной т-ре уран окисляется в сухом воздухе с образованием тонкой окисной пленки, при нагреве до т-ры 200° С образуется окалина двуокиси UО2, при т-ре 200—400° С — U3О8, при более высокой т-ре —UО3 (точнее — твердые растворы на основе этих окислов).
Скорость окисления мала при т-ре 50° С и очень велика при т-ре 300° С. С азотом уран медленно взаимодействует ниже т-ры 400° С, но достаточно быстро при т-ре 750 — 800° С.
Взаимодействие с водородом протекает уже при комнатной т-ре с образованием гидрида UH3.
В воде при т-ре до 70° С на уране образуется пленка двуокиси, оказывающая защитное действие; при т-ре 100° С взаимодействие существенно ускоряется.
В соединениях уран проявляет степень окисления: +3, +4, +5, +6.
Получение
Для получения U, его руды обогащают мокрым химическим способом, выщелачивая серной к-той в присутствии окислителя — двуокиси марганца.
Из сернокислого раствора урана экстрагируют органическими растворителями или выделяют фенольными смолами.
Полученный концентрат растворяют в азотной к-те. Образующийся при этом нитрат уранила UО2 (NО3)2 извлекают, например бутилфосфатом и после освобождения от последнего разлагают соединения У. при т-ре 500—700° С.
Полученные окислы U3О8 и UО3 высокой чистоты восстанавливают водородом при т-ре 600—800° С до двуокиси UО2.
Металлический уран получают металлотермическим восстановлением (кальцием или магнием) двуокиси UО2 либо тетрафторида урана UF4, предварительно получаемого из двуокиси действием безводного фтористого водорода при т-ре 500° С.
Последний метод более распространен, позволяет получать слитки высокой чистоты (0,0045% Fe, 0,001% Si, 0,003% С) и массой более тонны.
Металлический металл получают также электролизом в соляных ваннах, содержащих UF4, при т-ре 800— 1200° С.
Черновой уран обычно подвергают рафинирующей плавке (т-ра 1450—1600° С) в графитовых тиглях, в высокочастотных вакуумных печах с разливкой в графитовые изложницы.
Малые опытные образцы деформируют ковкой в альфа-состоянии, ее же применяют, наряду с прессованием в альфа- или гамма-состоянии, для деформирования крупных слитков.
Холодная прокатка повышает прочностные характеристики урана, твердость при обжатии на 40%, увеличивает HV от 235 до 325.
Снятие наклепа наступает в основном при т-ре 350—450° С в металле технической чистоты и сопровождается в этих условиях рекристаллизацией; вторичная, собирательная рекристаллизация развивается при т-ре 600—650° С.
Охлаждение урана в воде или масле из бета- или гамма-состояния не подавляет образования альфа-фазы, но измельчает зерно альфа-урана, особенно при наличии примесей.
Применение
Металлический U, сплавы на его основе и двуокись используют в качестве ядерного горючего.
Обогащенный в создании атомного оружия, а также водородных бомб, в военном деле необогащенный в виде снарядов.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.