Плутоний — химический элемент с обозначением Pu и порядковым номером 94. он представляет собой металлический элемент серебристо-серого оттенка, который при воздействии атмосферного воздуха потускнеет, образуя оксидированное покрытие.
У плутония существует шесть различных аллотропов и четыре степени окисления, он способен взаимодействовать с углеродом, галогенами, азотом, кремнием и водородом, образуя соответствующие оксиды и гидриды при наличии влажного воздуха.
Что приводит к увеличению объема образца на 70% и образованию пирофорного порошка.
Плутоний является радиоактивным элементом, который может накапливаться в костях, делая его использование опасным.
Содержание страницы
Что такое плутоний
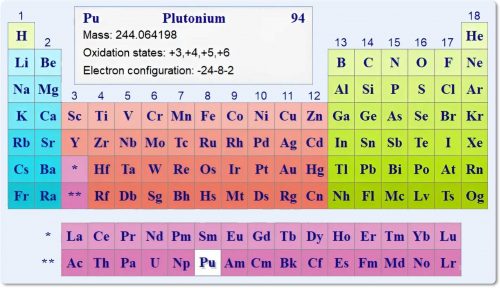
Это — искусственно полученный радиоактивный химический элемент 3-й группы 7-го периода Рu (Plutonium; от назв. планеты Плутон).
Атомный номер 94; атомная масса 244,0642, относится к актиноидам. Металл серебристо-белого цвета.
В соединениях проявляет степени окисления от + 3 до + 7, наиболее характерна степень окисления + 4.
Физические свойства
В интервале т-р от комнатной до т-ры плавления существует в виде полиморфных модификаций:
- Альфа.
- Бета.
- Гамма.
- Дельта.
- Эта и эпсилон.
Из них низкотемпературная альфа-модификация с простой моноклинной решеткой устойчива ниже т-ры 122° С.
Наиболее высокотемпературная эпсилон-модификация с кубической объемноцентрированной решеткой — выше т-ры 476° С.
Плотность альфа-плутония (т-ра 20° С) 19,8 г/см3; tпл 639,5° С; tкип 3235° С; удельная теплоемкость 0,032 кал/г • град (в интервале т-р 0—100° С).
В соединениях плутоний проявляет степень окисления: +3, +4, +5, +6, +7, а также 2 и сам химический элемент 0.
Изотопы
Плутоний в виде изотопа 238Рu впервые получили (1940) амер. ученые Г. Сиборг, Э. Макмиллан, Дж. Кеннеди и А. Валем, облучая уран ядрами тяжелого водорода — дейтронами.
Идентифицировано около 15 изотопов плутония с массовыми числами от 232 до 246. Период полураспада практически важного долгоживущего изотопа 239Pu составляет 24 360 лет.
В ничтожных количествах он обнаружен в урановых рудах.
Интересный факт о Плутонии: Он может светиться и «гореть» на воздухе, но не так, как обычное пламя.
Соединения плутония
При нагревании на воздухе плутоний быстро окисляется. В тонко-измельченном состоянии пирофорен.
Образует соединения с галогенами, кислородом, водородом, углеродом, азотом, серой, фосфором и др. неметаллами; со многими металлами — интерметаллические соединения.
Сероводородом плутония из водных растворов не осаждается. Его сульфид получают нагреванием двуокиси с газообразным сероводородом.
При прокаливании соединений плутония на воздухе образуется двуокись PuО2 — желто-коричневый кристаллический порошок.
Применение
В водных растворах соединения плутоний дают характерно окрашенные ионы: Рu3+ — синий, Рu4+ — от желтого до коричневого, PuO⁺2 — красно-фиолетовый, PuО⁺2² — розово-коричневый.
Более электроположительные, чем плутоний, металлы (например, барий, кальций) восстанавливают галогениды плутония до металла.
Наибольшее практическое значение имеет изотоп 239Рu.
В промышленности его получают в больших количествах в урановых ядерных реакторах.
Он имеет большое сечение деления на медленных нейтронах, поэтому его используют в качестве делящегося материала.
Плутоний очень токсичен, при попадании внутрь организма накапливается главным образом в костях.
Литература
Актиниды. Пер. с англ. Сиборг Г.
Часто задаваемые вопросы
Основное применение в ядерном оружии, ядерном горючем, источниках нейтронов.
Пороговых детекторах для определения спектра нейтронов и в производстве высших изотопов плутония и трансплутониевых элементов.
В ядерных реакторах в результате серии ядерных реакций, в основе которых лежит захват нейтрона и бета-распады.
Под воздействием нейтронов в ядерном реакторе, Уран-238 последовательно превращается в Уран-239, затем в Нептуний-239 и, наконец, в стабильный 239Рu.
Смертельная опасность: Это крайне радиоактивный и токсичный элемент.
Не прикасайтесь, отойдите на безопасное расстояние, предупредите окружающих.
Немедленно сообщите в соответствующие органы (полиция, пожарные).

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.