U уран (Uranium; от назв. планеты Уран) — химический элемент 3-й группы, с порядковым номером 92 в периодической системе.
Атомный номер 92, атомная масса 238,029. Находится в седьмом периоде. Температура плавления: 1132.4 °C, температура кипения 4131 °C. Плотность: 18.97 г/см3.
Содержание страницы
Электронная формула
Полная электронная формула атома урана в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 5f3 6s2 6p6 6d1 7s2
Сокращенная электронная конфигурация U:
[Rn] 5f3 6d1 7s2
Электронная формула атома урана в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f3 6d1
Порядок заполнения орбиталей электронами в атоме U является исключением из правила Клечковского.
Электронно-графическая схема урана (U)
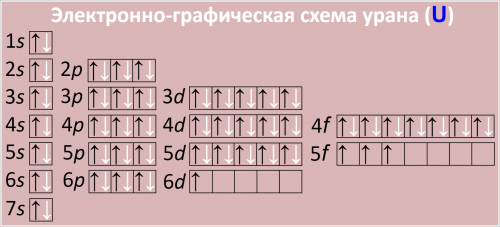
Рис. Схема распределения электронов по атомным орбиталям в атоме урана.
Энергетические уровни
Распределение электронов по орбиталям в атоме урана:
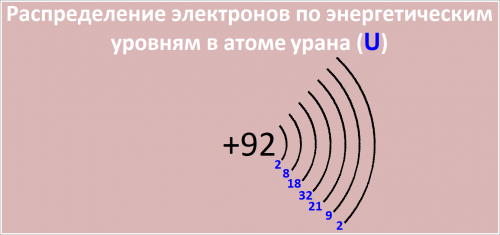
92 U )2 )8 )18 )32 )21 )9 )2
Распределение электронов по энергетическим уровням в атоме U:
- -й уровень (K): 2
- -й уровень (L): 8
- -й уровень (M): 18
- -й уровень (N): 32
- -й уровень (O): 21
- -й уровень (P): 9
- -й уровень (Q): 2
В соединениях уран проявляет степень окисления: +3, +4, +5, +6.
Стабильные изотопы
| Изотоп | Протоны | Нейтроны | Атомная масса изотопа |
| 235U | 92 | 143 | ~235.0439299 |
| 238U | 92 | 146 | ~238.0507882 |
Природный уран состоит из изотопа: 238U (99,282%), 235U (0,712%) и 234U (0,006%).
Изотоп 234U является не первичным, а радиогенным, он входит в состав радиоактивного ряда 238U.
Среди искусственных изотопов практическое значение имеет изотоп 233U.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.