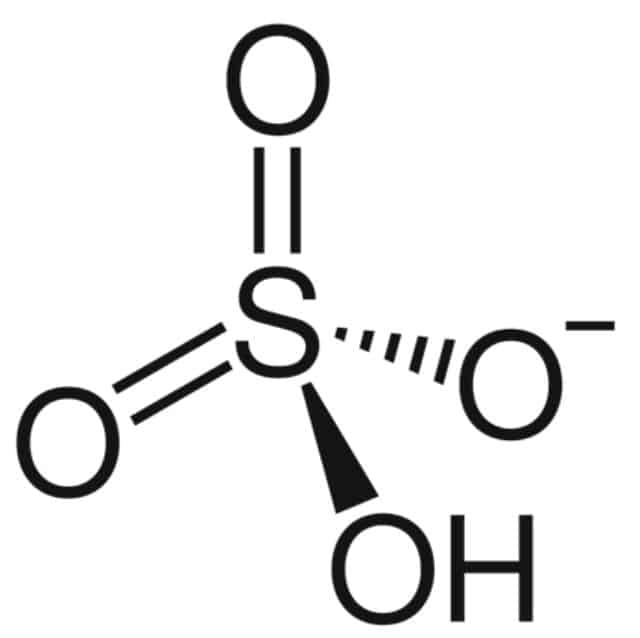
Сульфат водорода, также известный как бисульфат, является ионом со химической формулой HSO4—. Он образуется как компонент серной кислоты H2SO4.
Химические соединения, содержащие этот ион, известны как бисульфаты или сульфаты водорода. Примером такого соединения может служить бисульфат натрия.
Сульфаты водорода считаются кислыми и могут быть использованы как более мягкая форма кислоты по сравнению со своим исходным соединением, серной кислотой.
Фактически, они являются солями серной кислоты, в которых серная кислота депротонируется только один раз. В отличие от этого, в сульфат-ионе серная кислота депротонируется дважды.
Содержание страницы
Что такое сульфат водорода
Сульфат водорода, также известный как бисульфат, представляет собой анион с формулой HSO4 и образуется с химическим радикалом сульфатом (HSO4).
Когда сульфат водорода попадает в воду, он вступает в реакцию и образует серную кислоту, формула которой H2SO4.
Сульфат водорода является кислым по своей природе и используется как более слабая альтернатива серной кислоте.
Сульфат водорода вступает в реакцию с натрием с образованием бисульфата натрия (NaHSO4), который представляет собой чистое вещество.
Формула сульфата водорода показывает, что один атом водорода и один атом серы наряду с четырьмя атомами кислорода.
Физические свойства сульфата водорода
Молярная масса — 97,064 г/моль, Плотность — 1826,7 кг /м3. Температура плавления — 59 ºC. pH — 1. Цвет — Белый.
Химические свойства сульфата водорода
Сульфат водорода обладает высокой реакционной способностью с дистиллированной водой, образуя сульфат и ионы гидрония.
Его химическое уравнение приведено в виде:
HSO4— + H2O → H3O+ + SO42-
Он также может вступать в реакцию с нитрат-ионами с образованием сульфат-ионов и азотистой кислоты.
Химическое равенство приведено ниже:
HSO4— + NO2— → SO42- + HNO2
Сульфат водорода также может вступать в реакцию с водой (в качестве основания) и образовывать ионы гидрония.
Это происходит в соответствии с кислотно-основными реакциями Бренстеда-Лоури.
HSO4— +H2O ⇄ H3O+ +SO42-
Согласно Бренстеду-Лоури, кислотно-щелочная реакция фактически происходит, когда происходит перенос одного протона от одного иона или молекулы к другой.
В приведенном выше случае вода действует как основание, поскольку она реагирует с HSO4—, который является лучшим донором протонов.
Это происходит из-за амфотерной природы воды. Она может действовать как основание, так и кислота.
Использование сульфата водорода
Сульфат водорода используется на водоочистных сооружениях для удаления остаточного хлора. Сульфат водорода является основной альтернативой жидкому диоксиду серы.
Производство селитряного кека производится из натриевых солей сульфата водорода. Смолы, образующиеся из сульфата водорода, используются для успокоения кожи.
Сульфат водорода, также широко известный как бисульфат, является анионом. Формула сульфата водорода приведена в HSO4—. Сульфат водорода образуется с химическим радикалом сульфатом (HSO4).
Когда HSO4 подвергаются воздействию воды, они вступают в реакцию с образованием серной кислоты (H2SO4).
При сульфатном излучении сероводород обычно имеет кислую природу. Фактически, они используются как более слабая альтернатива серной кислоте.
Сульфат водорода вступает в реакцию с натрием с образованием бисульфата натрия (NaHSO4), который на самом деле является чистым веществом.
Он создает тетраэдрическую структуру с атомом серы в центре и четырьмя атомами кислорода, окружающими его. Он образует структуру, аналогичную структуре метана.
Сульфат с его химической формулой, SO42- на самом деле является оксоанионом серы. Путем депротонирования обеих ОН-групп в серной кислоте фактически можно получить сульфатный радикал.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.