Сульфат кальция, или гипс, является кристаллическим минералом, широко используемым в различных отраслях промышленности и строительства.
Этот неорганический соединение состоит из ионов кальция и сульфатных групп.
В природе сульфат кальция встречается в виде гипсового камня или ангидрита, а также может быть получен при различных технологических процессах.

Содержание страницы
Что такое сульфат кальция
Сульфат кальция представляет собой неорганическое соединение, известное своими гидратированными формами гипса.
Химическая формула сульфата кальция CaSO4.
Это очень полезное соединение как в безводной, так и в гидратированной форме. Его также называют дриеритом. Он плохо растворим в воде и вызывает постоянную жесткость воды.
Структура сульфата кальция
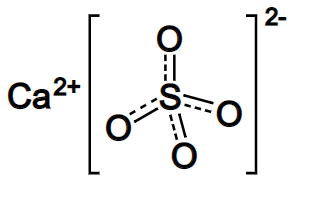
Сульфат кальция содержит по одному атому кальция и серы и четыре атома кислорода. Это ионное соединение, которое состоит из одного катиона кальция и одного сульфатаниона (многоатомного иона).
Ион кальция имеет валентность +2, в то время как многоатомный ион сульфата имеет валентность -2.
Таким образом, при соединении они образуют нейтральное соединение сульфат кальция (CaSO4).
Физические свойства
Безводный сульфат кальция при нормальных условиях бесцветные кристаллы, которые медленно присоединяют воду становясь гидратируясь до кристаллогидрата с 1/2 или 2 молекулами воды на 1 молекулу сульфата, соответственно CaSO4 · 0,5H2О и CaSO4 · 2H2О.
При повышенной температуре (свыше 1200 °C) может существовать в виде стабильной кубической модификации или двух метастабильных α- и β-гексагональных модификаций.
В воде растворим незначительно. Растворимость падает с повышением температуры: если при 20 °C она составляет 0,2036 г/100 г воды, то вблизи точки кипения воды (100 °C) снижается до 0,067 г сульфата на 100 г воды.
Растворённый в природной воде сульфат кальция является одним из факторов, определяющих жёсткость воды.
Получение
В лабораторных (домашних) условиях может быть получен действием серной кислоты H2SO4 на гидроксид кальция Ca(OH)2:
Ca(OH)2 + H2SO4 → CaSO4 + 2H2O
На оксид кальция:
CaO + H2SO4 → CaSO4 + H2O
Карбонат кальция:
CaCO3 + H2SO4 → CaSO4 + H2CO3
А также оксалата или ацетата кальция.
В производственных масштабах получают из природных минералов гипса, селенита или алебастра.
Образуется в результате окисления сульфида кальция при нагреве до 700—800 °C по реакции:
CaS + 2O2 = CaSO4.
Применение
Сельское хозяйство
Одним из главных применений сульфата кальция является его использование в сельском хозяйстве.
Сульфат кальция не только обогащает почву необходимыми питательными веществами, но и способствует укреплению корневой системы растений.
Благодаря этому, растения становятся более устойчивыми к стрессовым условиям, таким как засуха или неблагоприятная погода.
Кроме того, повышает качество урожая, увеличивая его урожайность и улучшая вкусовые характеристики продуктов.
Промышленность
В промышленности сульфат кальция также находит широкое применение. Он используется в составе строительных материалов, таких как гипсовая штукатурка, гипсовые панели и гипсокартонные плиты.
Благодаря особым свойствам сульфата кальция, эти материалы обладают высокой прочностью и устойчивостью к огню.
Кроме того, сульфат кальция также используется в производстве бумаги, пластика, косметических и фармацевтических препаратов.
Пищевая промышленность
Еще одной важной областью применения сульфата кальция является пищевая промышленность.
Он используется как пищевая добавка E516 и применяется в качестве стабилизатора, сгустителя и регулятора кислотности в различных продуктах, таких как молочные продукты, кондитерские изделия, мороженое и напитки.
Благодаря своим свойствам, сульфат кальция улучшает текстуру и долговечность этих продуктов, делая их более привлекательными для потребителей.
Фармацевтическая промышленность
Фармацевтическая промышленность также находит применение сульфата кальция. Он используется в производстве препаратов, предназначенных для омоложения и укрепления костей.
А также для лечения остеопороза и других заболеваний костей.
Благодаря своей способности усиливать костную ткань, сульфат кальция становится важным компонентом многих препаратов, направленных на поддержание здоровья костей.
Где еще применяют
1. Одним из наиболее распространенных и востребованных применений сульфата кальция является его использование в строительной отрасли.
2. Гипсовые плиты и панели широко используются для отделки стен и потолков в зданиях. Этот материал обладает такими преимуществами, как простота монтажа, огнеупорность и хорошая звукоизоляция.
3. Кроме того, гипс используется в производстве строительных смесей, таких как гипсовые штукатурки или шпатлевки, благодаря своим связывающим свойствам.
4. В промышленности сульфат кальция также находит широкое применение. Например, его используют для получения гипсовых изделий, таких как гипсокартонные листы или гипсовые блоки, которые также используются в строительстве.
5. Кроме того, используется в производстве текстиля, бумаги и пластмасс, где он служит в качестве наполнителя или стабилизатора.
6. В сельском хозяйстве сульфат кальция применяется как минеральное удобрение, поскольку кальций и сера являются необходимыми элементами для здорового роста растений.
7. Он способствует укреплению клеточных стенок, улучшает аэрацию почвы и повышает устойчивость культур к болезням.
8. Кроме всего этого, сульфат кальция находит применение в медицине. Он используется в процедурах гипсования для лечения переломов или деформаций костей, а также в стоматологии для создания моделей зубов или протезирования.
Часто задаваемые вопросы и ответы?
Это пищевая добавка, используемая как средство против слеживания, кондиционера и усилителя теста, средство для обработки муки, регулятор pH, загуститель и дрожжевой корм.
Состав сульфата кальция. Формула состава: CaSO4.
Используется для корневых и некорневых подкормок овощей, плодовых деревьев, декоративных культур.
