Теория:
Степень окисления свинца (Pb) в большинстве химических соединений принимает значения +2 и +4.
Это связано с особенностями электронной конфигурации атома и так называемым «эффектом инертной электронной пары», который становится всё более выраженным у тяжелых элементов 14-й группы.
Кроме того, существует показатель 0, характерный для свинца в виде простого вещества (тяжелый, мягкий синевато-серый металл).
Например для наиболее стабильной СО +2: в соединении PbO (оксид свинца II) или Pb(NO3)2 (нитрат свинца II) заряд катиона равен +2. Это состояние является энергетически наиболее выгодным.
Для сравнения, СО +4: встречается в таких веществах, как PbO2 (диоксид свинца) или PbCl4 (хлорид свинца IV). Соединения с этим зарядом являются сильными окислителями.
- Почему +2? Атом свинца отдает два 6p-электрона, при этом пара 6s-электронов остается на уровне. У тяжелых элементов эти s-электроны притянуты к ядру настолько сильно, что неохотно участвуют в реакциях.
- Почему +4 менее устойчива? Для достижения СО +4 необходимо задействовать ту самую инертную 6s-пару. Из-за высокой энергии ионизации такие соединения легко восстанавливаются до состояния +2.
- Синонимы и аналогичные термины: Окислительное число свинца, валентный уровень Pb, электрохимический заряд металла, степень электроположительности.
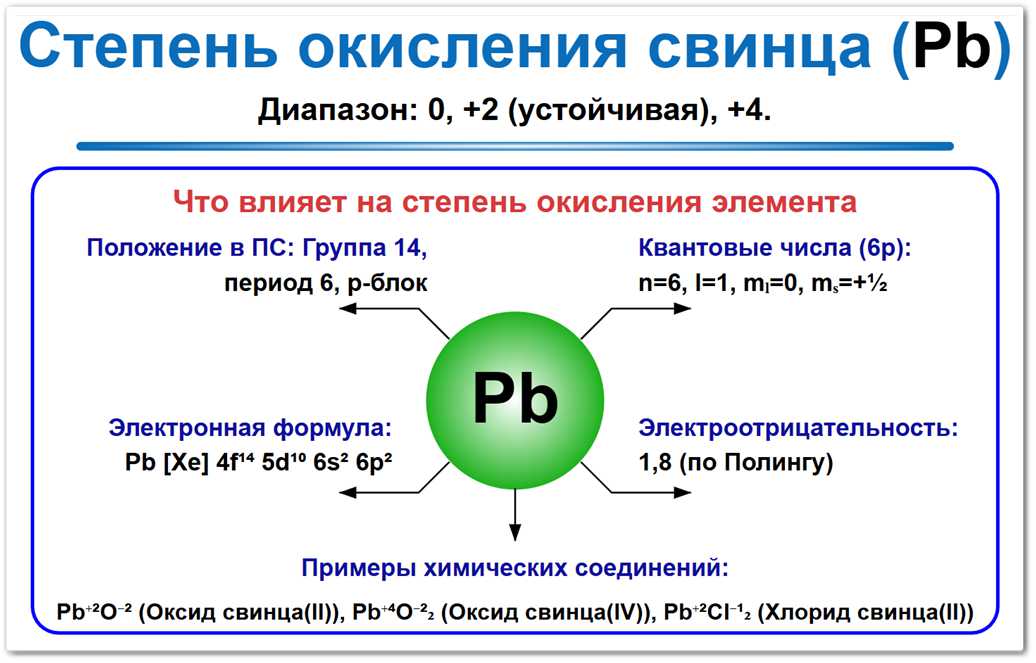
Рис. 1. Основные степени окисления свинца: 0, +2 и +4.
Состояние +2 доминирует в классической химии растворов, тогда как форма +4 чаще встречается в твердых оксидах или специфических органических соединениях.
Важно помнить, что свинец и все его производные высокотоксичны. Он обладает способностью накапливаться в костях и тканях, вызывая тяжелые отравления (сатурнизм).
На свойства этого элемента влияют электронное строение (4f14 5d10 6s2 6p2), релятивистское сжатие орбиталей и значение электроотрицательности 1,8 по Полингу.
Содержание страницы
- 1. Почему +2 — самая устойчивая степень окисления у свинца
- 2. Степень окисления свинца в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему свинец предпочитает заряды +2 и +4?
- 4. 4 способа определить степень окисления свинца
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления свинца
- 6. Шпаргалка для свинца
- 7. Свинец вне учебника: какие степени окисления существуют только в теории?
- 8. Пример решения задачи:
- 9. Проверка знаний
- 10. Часто задаваемые вопросы
Почему +2 — самая устойчивая степень окисления у свинца
Стабильность двухвалентного состояния объясняется тем, что 6s2-электроны ведут себя «пассивно», превращаясь в инертную пару.
- В простом веществе (Pb0): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d10 6s2 6p2. - В двухвалентном ионе (Pb+2): Металл теряет 2 электрона с p-подуровня. Конфигурация:
[Xe] 4f14 5d10 6s2.

Рис. 2. Схема формирования СО +2: удаление пары 6p-электронов и сохранение инертной 6s-пары.
Степень окисления свинца в соединениях
В зависимости от условий протекания реакции, свинец в соединениях проявляет степень окисления, которая меняет его свойства:
- Нитрат свинца(II) (Pb(NO3)2): Pb +2.
- Диоксид свинца (PbO2): Pb +4.
- Сульфид свинца (PbS / галенит): Pb +2.
- Тетраацетат свинца (Pb(CH3COO)4): Pb +4.
- Хлорид свинца(II) (PbCl2): Pb +2.
Высшая степень окисления
Высшая степень окисления Pb составляет +4. В этом состоянии он проявляет выраженные окислительные свойства, стремясь забрать электроны и вернуться в состояние +2.
Низшая степень окисления
Для элемента характерна степень окисления 0 в металлическом виде.
Отрицательные значения заряда в классических солях отсутствуют.
Промежуточные степени окисления
Степень окисления свинца в веществах иногда выглядит необычно. Яркий пример — сурик (Pb3O4).
Это смешанный оксид, который можно представить как 2PbO · PbO2.
В нем одновременно присутствует свинец в СО +2 и +4, что дает среднее формальное значение +2,66.
Важно: Из-за своей устойчивости в СО +2, свинец часто замещает кальций (Ca2+) в костных тканях человека, что является основной причиной его хронической токсичности.
Почему свинец предпочитает заряды +2 и +4?
Тип взаимодействия определяется его нахождением в 14-й (IVA) группе:
- Положительная СО (+): Свинец отдает валентные электроны. Переход в +4 требует очень жестких условий (сильных окислителей).
- Отсутствие отрицательных СО (-): Как типичный металл нижней части таблицы, он обладает низким сродством к электрону.
4 способа определить степень окисления свинца
По таблице Менделеева
- Семейство: p-элемент.
- Валентные электроны: 4 электрона (6s2 6p2).
- Атомная масса свинца: 207,2 а.е.м.
По валентности (Число связей)
Обычно валентность свинца составляет II или IV.
- В PbO: Свинец образует две связи с кислородом, СО — +2.
- В PbO2: Свинец образует четыре связи, СО — +4.
По электронной конфигурации
- Электронная формула свинца: [Xe] 4f14 5d10 6s2 6p2.
- Атому свинца степени окисления +2 достичь проще, так как пара p-электронов слабо связана с ядром по сравнению с s-парой.
По химическому соединению (Алгебраический расчет)
Пример для PbO2:
Суммарный заряд равен 0. Кислород равен -2. Обозначим свинец за x.
x + 2 · (-2) = 0 ⇒ x — 4 = 0 ⇒ x = +4
Примеры степеней окисления свинца
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +2 | Наиболее стабильная. Характерна для большинства солей и минералов. | PbO, PbCl2, PbSO4 |
| +4 | Окислительная. Проявляется в диоксиде и нестабильных галогенидах. | PbO2, PbF4, Pb(CH3COO)4 |
| 0 | Металл. Состояние чистого элемента, устойчивого к коррозии. | Pb (металлический свинец) |
Шпаргалка для свинца
- +2 — главная степень окисления, соли с этим зарядом часто малорастворимы.
- +4 — высокая степень окисления, делает свинец мощным реагентом для окисления.
- PbO2 — используется в свинцовых аккумуляторах именно благодаря СО +4.
Свинец вне учебника: какие степени окисления существуют только в теории?
Отрицательные степени (-1, -2, -4): В классической химии они не встречаются.
Однако в химии твердого тела существуют фазы Цинтля (сплавы с активными металлами, например, Na4Pb9), где свинец образует кластеры с формально отрицательным зарядом.
+1 и +3: Эти состояния крайне нестабильны. Они могут возникать как короткоживущие промежуточные продукты в окислительно-восстановительных процессах или в газовой фазе при экстремальных температурах.
Пример решения задачи:
▶️ Дано:
Соединение: PbS (сульфид свинца II).
⌕ Найти:
Определите СО свинца.
✨ Решение:
Сера (S) в бинарных соединениях с металлами проявляет СО -2. Для электронейтральности молекулы заряд свинца должен быть противоположным.
✅ Ответ:
Pb(+2).
Проверка знаний
Показать ответы
Правильные ответы: 1, 3, 4.
Разбор ошибок:
2 — неверно: для свинца намного стабильнее СО +2; соединения с СО +4 являются сильными окислителями.
Часто задаваемые вопросы
В химии — СО +2, в быту (металл) — СО 0.
Он является активной массой положительных пластин автомобильных аккумуляторов, где свинец переходит из СО +4 в СО +2 при разряде.
Потому, что это типичный металл с низкой электроотрицательностью.
Слабое удержание электронов: У свинца большой атомный радиус. Его внешние электроны находятся далеко от ядра и слабо им притягиваются, поэтому ему проще их отдать, чем забрать чужие.
Электроотрицательность: У свинца она составляет всего 1,8 (по Полингу). Для сравнения: у водорода — 2,2, у фтора — 4,0. Свинец просто не может «перетянуть» электрон у большинства других элементов.
Энергетика: Создание отрицательного иона свинца (Pb— или Pb4-) требует огромных затрат энергии, которые не компенсируются образованием химических связей.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.