Pb свинец (Plumbum) — химический элемент принадлежащий к 14-й группе, с порядковым номером 82 в периодической системе.
Находится в шестом периоде. Температура плавления: 327.5 °C, температура кипения 1749 °C. Плотность: 11.34 г/см3.
Содержание страницы
Электронная формула
Полная электронная формула атома свинца в порядке возрастания энергий орбиталей:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p2
Сокращенная электронная конфигурация Pb:
[Xe] 4f14 5d10 6s2 6p2
Электронная формула атома свинца в порядке следования уровней:
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 6s2 6p2
Электронно-графическая схема свинца (Pb)
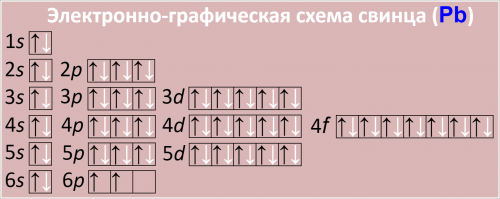
Рис. Схема распределения электронов по атомным орбиталям в атоме свинца.
Энергетические уровни
Распределение электронов по орбиталям в атоме свинца:
82 Pb )2 )8 )18 )32 )18 )4
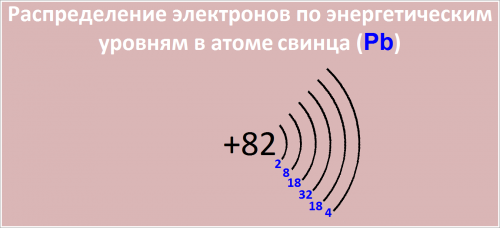
Распределение электронов по энергетическим уровням в атоме Pb:
- -й уровень (K): 2
- -й уровень (L): 8
- -й уровень (M): 18
- -й уровень (N): 32
- -й уровень (O): 18
- -й уровень (P): 4
Рис. Распределение электронов по энергетическим уровням в атоме свинца.
Валентные электроны свинца
Количество валентных электронов в атоме — 4.
Таблица квантовых чисел Pb (N — главное, L — орбитальное, M — магнитное, S — спин).
| Орбиталь | N | L | M | S |
| s | 6 | 0 | 0 | +1/2 |
| s | 6 | 0 | 0 | -1/2 |
| p | 6 | 1 | -1 | +1/2 |
| p | 6 | 1 | 0 | +1/2 |
В соединениях свинец проявляет степень окисления: -4, +2, +4.
Находится в одной группе с другими элементами, но валентность свинца является ключевым свойством, отличающим его от многих других элементов.
Стабильные изотопы
| Изотоп | Протоны | Нейтроны | Атомная масса изотопа |
| 204Pb | 82 | 122 | ~203.9730436 |
| 206Pb | 82 | 124 | ~205.9744653 |
| 207Pb | 82 | 125 | ~206.9758969 |
| 208Pb | 82 | 126 | ~207.9766521 |
Природный свинец состоит из стабильных изотопов: 204Рb (1,4%), 206Рb (25,2%), 207Рb (21,7%) и 208Рb (51,7%).
Есть также несколько радиоактивных изотопов 194Pb — 203Pb, 205Pb, 209Pb — 214Pb.
Из них наиболее долгоживущие — 202Pb и 205Pb (с периодами полураспада 52,5 тысяч и 17,3 млн лет.
Для более глубокого изучения его атомного строения, физических свойств и применения, мы рекомендуем ознакомиться с нашей главной статьей: свинец химический элемент.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.