Теория:
Степень окисления платины (Pt) в большинстве своих химических связей принимает значения +2 и +4.
Также существуют степени окисления +1, +3, +5 и +6, но они крайне нестабильны и существуют только в особых условиях.
Например, в составе некоторых комплексных соединений или при взаимодействии с сильными окислителями (фтором, кислородом при высоких температурах).
Кроме того, встречается и отрицательная степень окисления (например, −1 или −2) — она наблюдается в редких случаях, в составе определённых металлоорганических комплексов и интерметаллидов.
Где платина выступает в роли акцептора электронной плотности, такие соединения малоизучены и не распространены в обычной химической практике.
Выделяют также показатель 0, который относится к простому веществу в его естественном металлическом состоянии — то есть к элементарной платине (Pt) в виде металла, не вступившего в химическую связь.
Например для наиболее стабильной СО +4: в популярном лабораторном реактиве H2[PtCl6] (гексахлороплатиновая кислота) заряд центрального иона равен +4.
Для сопоставления, СО +2: часто встречается в таких веществах, как PtCl2 (хлорид платины II) или комплексных солях типа соли Пейроне.
- Почему +2 и +4? Платина — это 5d-элемент. Электронная конфигурация [Xe] 4f14 5d9 6s1 позволяет ей легко задействовать s-электрон и часть d-электронов для формирования прочных связей.
- Эффект стабильности: Для платины характерно образование плоскоквадратных комплексов в состоянии +2 и октаэдрических в состоянии +4, что энергетически очень выгодно.
- Почему редко выше +6? Хотя теоретически платина может отдавать больше электронов, высшие степени окисления (например, +6 в PtF6) требуют крайне агрессивных условий и очень сильных окислителей.
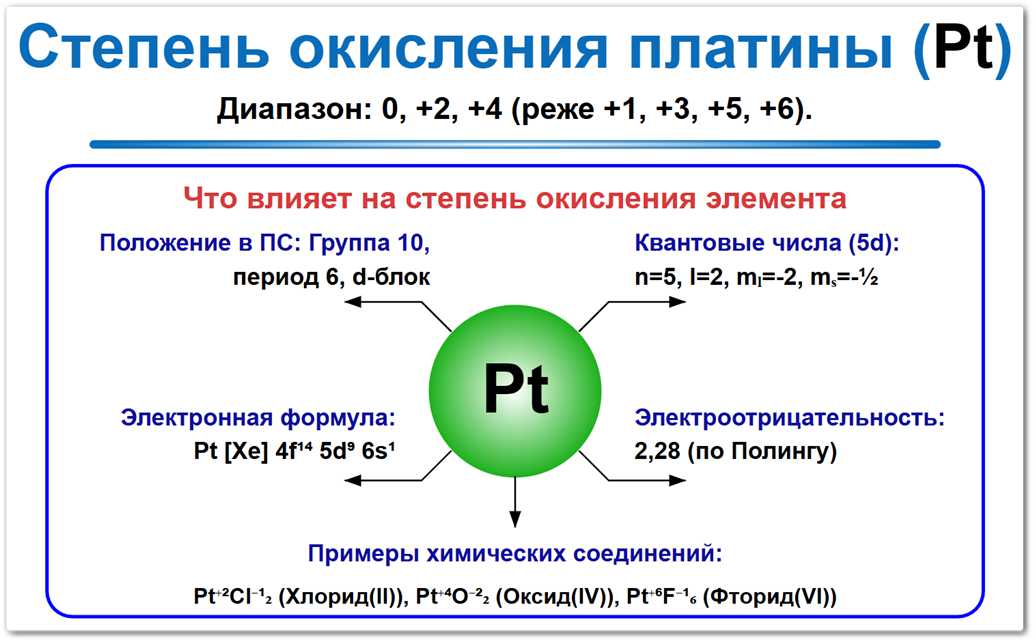
Рис. 1. Варианты степеней окисления платины: от 0 до +6.
Превалирующими формами являются +2 и +4, которые определяют свойства большинства катализаторов и лекарственных препаратов на основе этого металла.
Важно учитывать, что химия платины в различных валентных состояниях легла в основу создания противоопухолевых средств (например, цисплатина), где именно геометрия связей и заряд металла играют решающую роль.
На свойства элемента влияют электронное строение (5d9 6s1), эффект лантаноидного сжатия и достаточно высокое значение электроотрицательности — 2,28 по шкале Полинга.
Содержание страницы
- 1. Почему +2 и +4 — самые стабильные степени окисления у платины
- 2. Степень окисления платины в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему платина чаще отдает электроны (заряды +2, +4), а не принимает?
- 4. 4 способа определить степень окисления платины
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления платины
- 6. Шпаргалка для платины
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +2 и +4 — самые стабильные степени окисления у платины
Причина непоколебимости данных состояний кроется в формировании симметричных и прочных координационных сфер вокруг атома металла.
- В простом веществе (Pt⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d9 6s1. - В ионе (Pt+2): Платина лишается 2 электронов. Конфигурация:
[Xe] 4f14 5d8.

Рис. 2. Процесс окисления платины: путь от инертного металла до устойчивых катионов +2 и +4 за счет перестройки электронной оболочки.
Степень окисления платины в соединениях
В зависимости от агрессивности среды и природы лигандов, платина в соединениях проявляет степень окисления, которая меняет ее реакционную способность и цвет:
- Оксид платины(IV) (PtO2): Pt +4, O -2.
- Хлорид платины(II) (PtCl2): Pt +2, Cl -1.
- Гексафторид платины (PtF6): Pt +6.
- Тетрахлороплатинат(II) калия (K2[PtCl4]): Pt +2.
- Сульфид платины(IV) (PtS2): Pt +4.
Высшая степень окисления
Высшая степень окисления Pt составляет +6. Это состояние крайне нестабильно и проявляется лишь в единичных соединениях с фтором или в составе оксофторидов.
Низшая степень окисления
Для платины в комплексных соединениях возможна степень окисления 0 (например, в карбонилах), а сам металлический атом платины имеет степень окисления 0 в чистом слитке.
Промежуточные степени окисления
Степень окисления платины в веществах иногда принимает значения +1, +3 или +5. Однако такие формы являются переходными и стремятся перейти в более устойчивые +2 или +4.
Важно: Гексафторид платины (Pt+6) — настолько мощный окислитель, что именно с его помощью впервые удалось окислить благородный газ ксенон, что перевернуло представления о химии.
Почему платина чаще отдает электроны (заряды +2, +4), а не принимает?
Знак заряда обусловлен типично металлическим характером элемента и его положением в d-блоке:
- Положительная СО (+): Платина выступает донором, отдавая электроны более активным неметаллам.
- Нулевая СО (0): Характерна для тяжелого, блестящего и благородного металла, устойчивого к химии.
- Отрицательная СО (-): Чрезвычайно редка и зафиксирована только в особых интерметаллидах с активными металлами (например, платиниды щелочных металлов).
4 способа определить степень окисления платины
По таблице Менделеева
- Семейство: d-элемент (платиновые металлы).
- Валентные электроны: 10 (9 на 5d и 1 на 6s-подуровне).
- Атомная масса платины: 195,1 а.е.м.
По валентности (Число связей)
Как и у большинства металлов ее группы, валентность платины чаще всего равна IV или II.
- В диоксиде (PtO2): Платина образует четыре связи с кислородом, СО — +4.
- В хлориде (PtCl2): Металл проявляет валентность II, СО — +2.
По электронной конфигурации
- Электронная формула платины: [Xe] 4f14 5d9 6s1.
- Атому платины степени окисления +2 и +4 достичь проще всего, так как это приводит к образованию стабильных координационных структур.
Для просмотра распределения электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для K2PtCl6 (гексахлороплатинат IV калия):
Сумма СО равна 0. Калий всегда +1, хлор -1. Обозначим Pt как x.
2·(+1) + x + 6·(-1) = 0 ⇒ 2 + x — 6 = 0 ⇒ x = +4
Примеры степеней окисления платины
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +4 | Типичная. Наиболее устойчивая форма в кислых средах и солях. | PtO2, H2PtCl6, PtF4 |
| +2 | Постоянная. Характерна для хлоридов и множества комплексных соединений. | PtCl2, PtO, [Pt(NH3)2Cl2] |
| 0 | Металл. Благородное состояние самородного элемента. | Pt (металлическая) |
Шпаргалка для платины
- +4 и +2 — фундаментальные степени окисления, встречающиеся почти везде.
- Комплексообразователь — платина является чемпионом по созданию сложных координационных солей.
- Благородство — в СО 0 металл практически не реагирует с кислотами, кроме «царской водки».
Пример решения задачи:
▶️ Дано:
Соединение: PtF4 (фторид платины IV).
⌕ Найти:
Определите СО платины.
✨ Решение:
Фтор (F) как самый электроотрицательный элемент всегда -1. Уравнение: x + 4 · (-1) = 0 → x — 4 = 0 → x = +4.
✅ Ответ:
Pt(+4).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: в исключительных случаях, например во фториде PtF6, платина способна проявлять СО +6.
Часто задаваемые вопросы
Обе формы (+2 и +4) очень стабильны, выбор зависит от химического окружения.
Да, в крайне редких сплавах с активными металлами (платинидах) она может формально принимать отрицательные значения.
Это связано с высокой энергией ионизации и прочностью связи электронов с ядром, что делает ее «благородной».

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.