Теория:
Степень окисления золота (Au) в большинстве соединений принимает значение +3, однако для этого благородного металла также характерно устойчивое состояние +1.
Кроме того, выделяют показатель 0, который относится к чистому химическому элементу в виде самородного металла.
Но есть и другие -1, +2, +5, эти состояния встречаются крайне редко, соединения малоустойчивы и часто существуют только в специфических условиях.
Например для наиболее стабильной СО +3: в соединении AuCl3 (хлорид золота III) степень окисления металла равна +3.
Для сравнения, СО +1: встречается в таких веществах, как AuCl (хлорид золота I).
- Почему +3? Золото — это d-элемент. При образовании связей оно может отдавать один 6s-электрон и два 5d-электрона, что приводит к формированию устойчивой плоскоквадратной конфигурации комплексов.
- Почему +1 так часто встречается? У золота электронная конфигурация [Xe] 4f14 5d10 6s1. Отдача единственного внешнего s-электрона оставляет полностью заполненный 5d10 слой, что энергетически выгодно.
- Уникальность золота: Это один из немногих металлов, способных в специфических условиях (с цезием) принимать отрицательную степень окисления -1 (ауриды), ведя себя подобно галогенам.
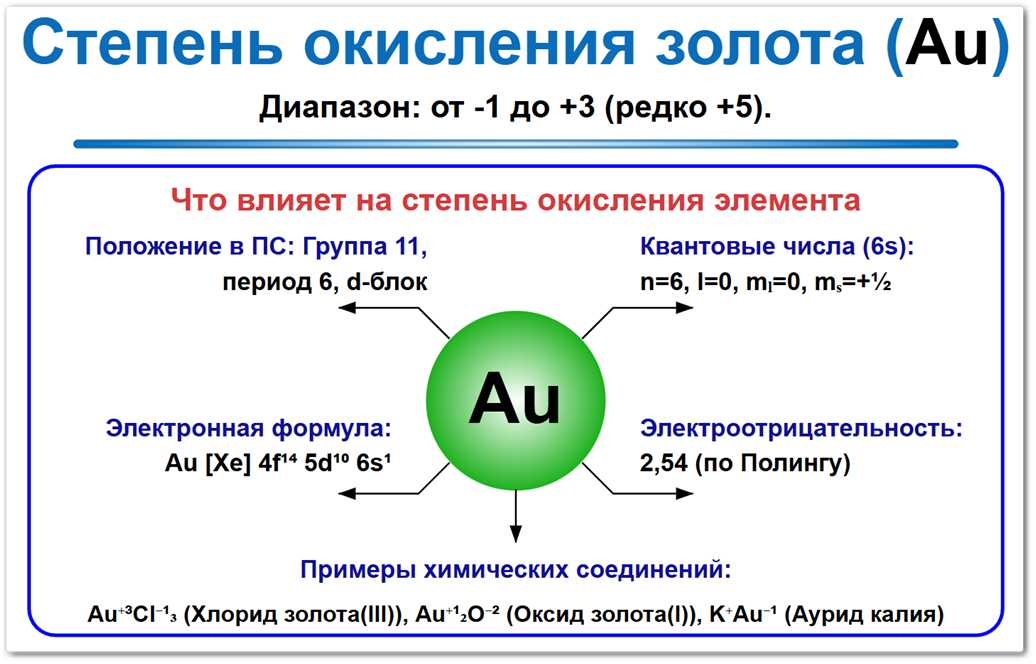
Рис. 1. Основные степени окисления золота: от 0 до +3.
Наиболее устойчивые формы — +3 (в комплексах) и +1, а состояние 0 соответствует металлическому золоту, обладающему исключительной химической стойкостью.
Обратите внимание, что химия золота в значительной степени определяется релятивистскими эффектами, которые сближают энергии 6s и 5d орбиталей.
Это объясняет и его характерный желтый цвет, и высокую электроотрицательность.
На формирование его параметров влияют электронное строение (5d10 6s1), положение в 11-й группе и значение электроотрицательности 2,4 по шкале Полинга (самое высокое среди металлов).
Содержание страницы
- 1. Почему +3 — самая стабильная степень окисления у золота в растворах
- 2. Степень окисления золота в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему золото — благородный металл (степени 0, +1, +3)?
- 4. 4 способа определить степень окисления золота
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления золота
- 6. Шпаргалка для золота
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему +3 — самая стабильная степень окисления у золота в растворах
Причина преобладания этого состояния заключается в высокой прочности образуемых комплексных соединений, где золото достигает стабильной координации.
- В простом веществе (Au⁰): Заряд равен 0. Конфигурация:
[Xe] 4f14 5d10 6s1. - В ионе (Au+1): Золото теряет s-электрон. Конфигурация:
[Xe] 4f14 5d10.

Рис. 2. Процесс окисления золота: от инертного металла до катионов +1 и +3 за счет взаимодействия с сильными окислителями (например, царской водкой).
Степень окисления золота в соединениях
В зависимости от реагентов, золото в соединениях проявляет степень окисления, которая определяет устойчивость и цвет вещества:
- Оксид золота(III) (Au2O3): Au +3, O -2.
- Хлорид золота(I) (AuCl): Au +1, Cl -1.
- Золотохлористоводородная кислота (H[AuCl4]): Au +3.
- Аурид цезия (CsAu): Au -1, Cs +1.
- Фторид золота(V) (AuF5): Au +5.
Высшая степень окисления
Высшая степень окисления Au в стабильных условиях равна +3, однако в присутствии фтора может достигать значения +5.
Низшая степень окисления
Для золота зафиксирована уникальная степень окисления -1, но чаще всего атом золота имеет заряд 0 в самородном состоянии.
Промежуточные степени окисления
Степень окисления золота в веществах редко принимает значения +2. Такие формы крайне неустойчивы и быстро превращаются в смесь состояний +1 и +3 (диспропорционируют).
Важно: Способность золота переходить в СО +3 под действием смеси кислот делает степень окисления золота формула соединения (например, в «царской водке») ключевой для процессов аффинажа и ювелирного дела.
Почему золото — благородный металл (степени 0, +1, +3)?
Поведение заряда продиктовано высокой инертностью и положением в ряду напряжений:
- Положительная СО (+): Требует воздействия мощных окислителей или комплексообразователей.
- Нулевая СО (0): Предпочтительное состояние, обеспечивающее сохранность золотых изделий тысячелетиями.
- Отрицательная СО (-): Проявляется только с самыми активными щелочными металлами из-за аномально высокой электроотрицательности золота.
4 способа определить степень окисления золота
По таблице Менделеева
- Семейство: d-элемент.
- Валентные электроны: 1 (на 6s-подуровне) и потенциально электроны 5d-подуровня.
- Атомная масса золота: 197 а.е.м.
По валентности (Число связей)
Типичная валентность золота составляет III или I.
- В оксиде (Au2O3): Золото образует связи, соответствующие валентности III, СО — +3.
- В цианиде (KAu(CN)2): Золото проявляет валентность I, СО — +1.
По электронной конфигурации
- Электронная формула золота: [Xe] 4f14 5d10 6s1.
- Атому золота степени окисления +1 достичь легче всего, но комплексы в СО +3 часто оказываются более прочными.
Для просмотра квантовомеханических характеристик используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для KAuCl4 (тетрахлороаурат III калия):
Сумма СО равна 0. Калий +1, Хлор -1. Золото — x.
(+1) + x + 4 · (-1) = 0 ⇒ x = +3
Примеры степеней окисления золота
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +3 | Типичная. Основная форма для комплексных кислот и солей. | AuCl3, HAuCl4, Au2O3 |
| +1 | Устойчивая. Характерна для простых галогенидов и цианистых комплексов. | AuCl, AuCN, K[Au(CN)2] |
| 0 | Металл. Стандартное состояние природного золота. | Au (самородок) |
Шпаргалка для золота
- +3 — самая распространенная СО в химии растворов.
- +1 — устойчивое состояние, важное для добычи золота (цианирование).
- Инертность — золото почти не окисляется кислородом даже при нагревании.
Пример решения задачи:
▶️ Дано:
Соединение: AuCl3 (хлорид золота III).
⌕ Найти:
Определите СО золота.
✨ Решение:
Хлор (Cl) как галоген равен -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
Au(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: золото может проявлять СО -1 в ауридах (например, CsAu), что является редким исключением для металлов.
Часто задаваемые вопросы
В металлическом виде — СО 0, в химических соединениях — чаще всего +3.
Это состояние крайне нестабильно и встречается только в очень редких комплексах, которые быстро распадаются.
Это связано с тем, что оно не склонно переходить из СО 0 в СО +1 или +3 при контакте с воздухом и влагой.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.