Теория:
Степень окисления ксенона в большинстве соединений принимает значения +2, +4, +6, +8, значительно реже встречаются состояния +1 (в метастабильных ионах).
Будучи благородным газом, ксенон также существует в состоянии с СО 0 (свободный газ). Отрицательные степени окисления для него нехарактерны и в обычных химических условиях не наблюдаются.
Например для высшей СО +8: в соединении XeO4 (тетраоксид ксенона) степень окисления элемента равна +8.
Это происходит потому, что ксенон находится в 18-й группе и при взаимодействии с таким мощным окислителем, как кислород, он способен задействовать все 8 электронов внешнего слоя (5s2 5p6), достигая максимально возможного заряда.
Для сравнения, нулевая СО 0: характерна для ксенона в свободном состоянии, как Xe (газ).
Здесь ситуация стабильна: ксенон имеет завершенную электронную оболочку и не вступает в реакции без воздействия экстремально активных реагентов (фтор, кислород), сохраняя нейтральный заряд.
Соединения ксенона в высших степенях окисления крайне нестабильны и являются сильнейшими окислителями. Например, тетраоксид ксенона склонен к взрывному разложению на свободный ксенон и кислород.
Промежуточные же степени окисления, такие как +2 или +4, являются более доступными в синтезе.
Обладая конфигурацией [Kr] 4d10 5s2 5p6, ксенон за счет распаривания электронов и перехода их на свободные 5d-орбитали может образовывать устойчивые при низких температурах фториды.
Именно поэтому химия ксенона началась с получения XeF2 и XeF4 — соединений, где он «выкладывается» лишь частично.
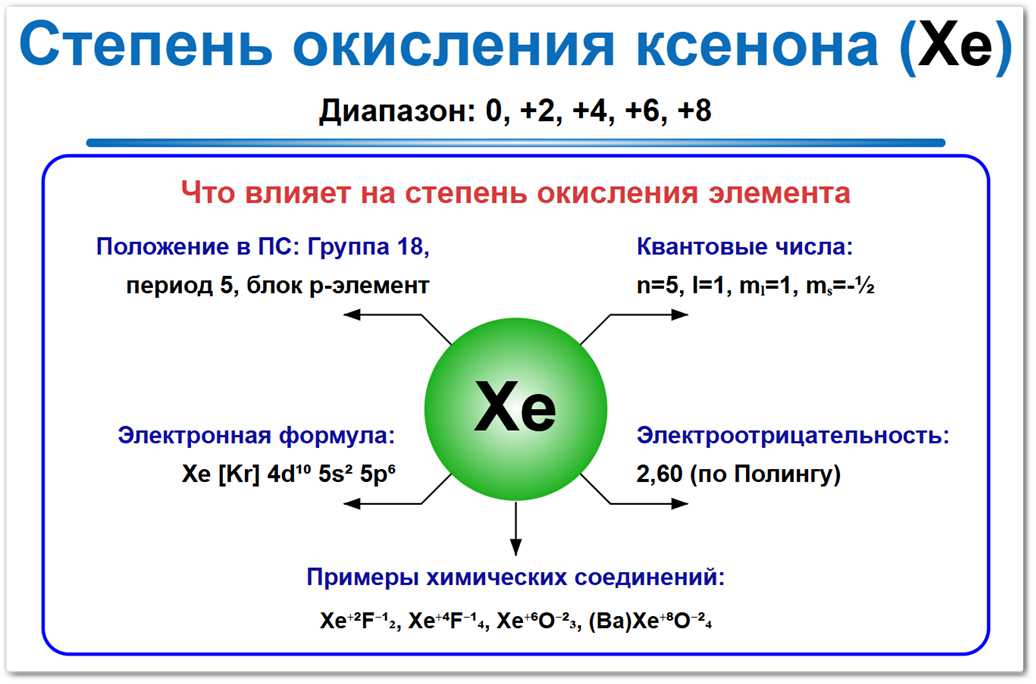
Рис. 1. Возможные степени окисления ксенона: от 0 до +8. Наиболее изученные формы — +2 (фторид), +4 (тетрафторид) и высшая форма +8, характерная для перксенатов.
Обратите внимание, что химия ксенона во многом схожа с химией криптона (Kr) и радона (Rn), однако ксенон образует гораздо более широкий спектр устойчивых соединений благодаря более низкому потенциалу ионизации.
На их формирование влияют электронное строение (5s2 5p6), положение в 18-й группе и значение электроотрицательности 2,6 по шкале Полинга.
Содержание страницы
- 1. Почему у ксенона стабильная степень окисления?
- 2. Степень окисления ксенона в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления ксенона
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления ксенона
- 6. Шпаргалка для ксенона
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у ксенона стабильная степень окисления?
Причина возможности существования положительных состояний ксенона заключается в том, что его валентные электроны находятся достаточно далеко от ядра, что позволяет сильным окислителям «распаривать» их и задействовать пустующие d-орбитали.
- В простом веществе (Xe⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 5p [↑↓][↑↓][↑↓]. - В ионе (Xe+8): Ксенон задействует все 8 валентных электронов. Конфигурация внешнего слоя пуста.

Рис. Высшая степень окисления +8 реализуется в жестких условиях, например, в составе перксенат-иона (XeO64-).
Степень окисления ксенона в соединениях
В зависимости от степени окисления, ксенон в соединениях проявляет свойства, делающие его уникальным объектом благородной химии:
- Тетраоксид ксенона (XeO4): Xe +8, O -2.
- Триоксид ксенона (XeO3): Xe +6, O -2.
- Тетрафторид ксенона (XeF4): Xe +4, F -1.
- Дифторид ксенона (XeF2): Xe +2, F -1.
- Перксенат натрия (Na4XeO6): Xe +8.
Высшая степень окисления
Высшая степень окисления ксенона равна +8. Это значение соответствует числу электронов на внешнем уровне (группа XVIII или VIIIА) и проявляется в солях перксеновой кислоты и летучем оксиде XeO4.
Низшая степень окисления
Для ксенона степень окисления равна 0 в свободном виде — это его наиболее стабильное и распространенное состояние в атмосфере Земли.
Промежуточные степени окисления
Степень окисления ксенона в веществах часто принимает значения +2, +4 и +6. Эти формы являются промежуточными ступенями окисления и широко используются в лабораторном синтезе как фторирующие агенты.
Важно: Состояние +2 во фториде (XeF2) — это наиболее термически стабильная форма химически связанного ксенона, где степень окисления ксенона формула соединения всегда +2.
Почему степень окисления чаще положительная?
Знак заряда определяется высокой электроотрицательностью партнеров (F, O) по сравнению с ксеноном:
- Положительная СО (+): Ксенон отдает или смещает электронную плотность к фтору или кислороду.
- Нулевая СО (0): Характерна для атомарного газа, не вступающего в связи.
- Отрицательная СО (-): Физически не обоснована для благородных газов, так как их оболочка уже максимально заполнена.
Как определить степень окисления ксенона
По таблице Менделеева
- Семейство: Благородные газы (p-элемент).
- Валентные электроны: 8 (на 5s и 5p подуровнях).
- Атомная масса ксенона: 131 а.е.м.
По валентности (Число связей)
В отличие от инертного состояния, валентность ксенона в соединениях переменна и чаще всего четна: II, IV, VI или VIII.
- В дифториде (XeF2): Атом ксенона образует две связи с фтором. Его валентность — II, а степень окисления равна +2.
- В тетраоксиде (XeO4): Ксенон образует связи с четырьмя атомами кислорода. Валентность — VIII, СО ксенона — +8.
По электронной конфигурации
- Электронная формула ксенона: [Kr] 4d10 5s2 5p6.
- Атому ксенона степени окисления +8 достичь возможно только при полной распаковке p- и s-пар на d-орбитали.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для XeF6 (гексафторид ксенона):
Сумма СО равна 0. Фтор всегда -1. Обозначим Xe как x.
x + 6 · (-1) = 0 ⇒ x = +6
Примеры степеней окисления ксенона
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +8 | Высшая. Сильнейший окислитель. | XeO4, Ba2XeO6 |
| +6 | Высокая. Проявляется в триоксиде и гексафториде. | XeO3, XeF6 |
| +4, +2 | Наиболее изученные. Стабильные при обычных условиях фториды. | XeF4, XeF2, XeOF2 |
| 0 | Инертный газ. Основное состояние. | Xe (в баллонах) |
Шпаргалка для ксенона
- +8 — высшая степень, проявляется в перксенатах и взрывоопасном XeO4.
- Окисление — ксенон в положительных СО является экстремально сильным окислителем.
- Благородство — несмотря на наличие соединений, ксенон в СО 0 остается инертным и нетоксичным газом.
Пример решения задачи:
▶️ Дано:
Соединение: Na4XeO6 (перксенат натрия).
⌕ Найти:
Определите СО ксенона.
✨ Решение:
Натрий (Na) равен +1, Кислород (O) равен -2. Уравнение: 4 · (+1) + x + 6 · (-2) = 0 → 4 + x — 12 = 0 → x = +8.
✅ Ответ:
Xe(+8).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: ксенон образует устойчивые связи в основном с самыми электроотрицательными элементами — фтором и кислородом. Связи с другими элементами крайне нестабильны.
Часто задаваемые вопросы
Нет, ксенон обладает полностью заполненной электронной оболочкой, и принятие лишних электронов энергетически невозможно.
Наиболее устойчивым считается дифторид ксенона (XeF2), который может храниться в специальных контейнерах при комнатной температуре.
Это связано с большим радиусом атома ксенона. Внешние электроны слабо притягиваются к ядру, что позволяет сверхсильным окислителям «оттягивать» их на себя.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.