Теория:
Степень окисления сурьмы (Sb) в большинстве соединений принимает значения +3 и +5, также -3 достаточно редкий случай, с ограниченным узким кругом соединений.
В металлических сплавах и интерметаллидах сурьма может находиться в состоянии 0.
Может проявлять промежуточные степени окисления (например, +1, +2, +4) но при этом они крайне редки и малоустойчивы.
Например для высшей СО +5: в соединении SbF5 (пентафторид сурьмы) степень окисления элемента равна +5.
Это происходит потому, что сурьма находится в 15-й группе и при взаимодействии с таким мощным окислителем, как фтор, она задействует все свои 5 валентных электронов (5s2 5p3), достигая максимально возможного положительного заряда.
Для сравнения, отрицательная СО -3: встречается в таких соединениях, как Mg3Sb2 (антимонид магния) или SbH3 (стибин).
Здесь ситуация обратная: сурьма выступает в роли более электроотрицательного партнера и «принимает» электронную плотность на свои p-орбитали, чтобы завершить внешний электронный слой до устойчивой конфигурации инертного газа ксенона.
Такие состояния, как в стибине, термически нестабильны, так как сурьма имеет сравнительно низкую электроотрицательность для неметалла и легко стремится вернуться к более стабильным положительным зарядам.
Промежуточные же степени окисления, такие как +4, являются «неудобными» для атома.
Обладая конфигурацией [Kr] 4d10 5s2 5p3, сурьме энергетически выгоднее либо отдать три p-электрона (стабильная СО +3), либо все пять электронов внешнего слоя (СО +5).
Именно поэтому соединения сурьмы(IV), например смешанный оксид Sb2O4, часто представляют собой решетку, где одновременно присутствуют узлы со степенями окисления +3 и +5.
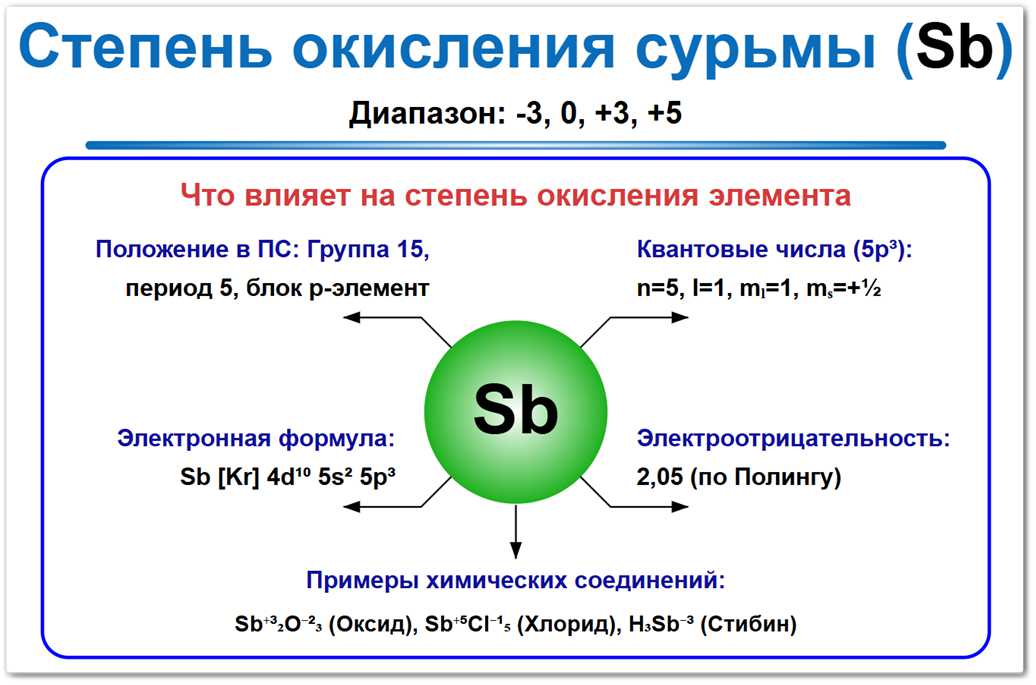
Рис. 1. Возможные степени окисления сурьмы: от -3 до +5. Наиболее устойчивые формы — +3 (сульфиды, хлориды) и высшая форма +5, характерная для фторидов и антимонатов.
Обратите внимание, что химия сурьмы во многом схожа с химией мышьяка (As) и висмута (Bi), её соседей по группе, что проявляется в способности образовывать летучие водородные соединения состава MeH3.
На их формирование влияют электронное строение (5s2 5p3), положение в 15-й группе и значение электроотрицательности 2,05 по шкале Полинга.
Содержание страницы
- 1. Почему у сурьмы стабильная степень окисления?
- 2. Степень окисления сурьмы в соединениях
- 2.1. Высшая степень окисления
- 2.2. Низшая степень окисления
- 2.3. Промежуточные степени окисления
- 3. Почему степень окисления чаще положительная?
- 4. Как определить степень окисления сурьмы
- 4.1. По таблице Менделеева
- 4.2. По валентности (Число связей)
- 4.3. По электронной конфигурации
- 4.4. По химическому соединению (Алгебраический расчет)
- 5. Примеры степеней окисления сурьмы
- 6. Шпаргалка для сурьмы
- 7. Пример решения задачи:
- 8. Проверка знаний
- 9. Часто задаваемые вопросы
Почему у сурьмы стабильная степень окисления?
Причина стабильности состояний сурьмы заключается в заполнении или полном освобождении p-подуровня. Состояние +3 достигается потерей только p-электронов, а +5 — полным вовлечением 5s-пары.
- В простом веществе (Sb⁰): Заряд равен 0. Конфигурация:
5s [↑↓] 5p [↑][↑][↑]. - В ионе (Sb+5): Сурьма отдает все 5 валентных электронов. Конфигурация:
[Kr] 4d10.
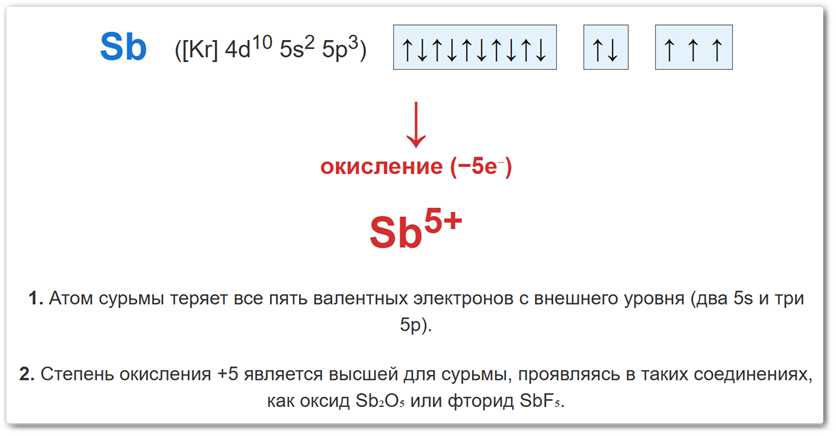
Рис. 2. Процесс окисления сурьмы: от металлического состояния до высшего состояния +5 в составе пентаоксида.
Степень окисления сурьмы в соединениях
В зависимости от реагентов, сурьма в соединениях проявляет степень окисления, которая определяет кислотно-основные свойства вещества:
- Пентахлорид сурьмы (SbCl5): Sb +5, Cl -1.
- Триоксид сурьмы (Sb2O3): Sb +3, O -2.
- Антимонат натрия (NaSbO3): Sb +5.
- Сульфид сурьмы(III) (Sb2S3): Sb +3, S -2.
- Стибин (SbH3): Sb -3, H +1.
Высшая степень окисления
Высшая степень окисления сурьмы равна +5. Это значение полностью соответствует номеру группы (V или 15) в периодической системе и характерно для наиболее сильных окисленных форм элемента.
Низшая степень окисления
Для сурьмы в соединениях с металлами или водородом характерна степень окисления -3, однако степень окисления сурьмы равна 0 в её металлической (самородной) форме или в составе технических сплавов.
Промежуточные степени окисления
Степень окисления сурьмы в веществах часто формально равна +4 (например, в Sb2O4), но такие формы являются результатом сосуществования атомов в состояниях +3 и +5 в одной кристаллической решетке.
Важно: Состояние +3 является наиболее термически устойчивым для сурьмы. Большинство природных минералов, таких как антимонит (Sb2S3), содержат сурьму именно в этой степени окисления, где степень окисления сурьмы формула соединения всегда +3.
Почему степень окисления чаще положительная?
Знак заряда определяется двойственной природой сурьмы как полуметалла:
- Положительная СО (+): Проявляется при связи с неметаллами (кислород, галогены), где сурьма выступает донором электронов.
- Нулевая СО (0): Характерна для простого вещества с металлическим блеском.
- Отрицательная СО (-): Проявляется только в антимонидах и стибине при взаимодействии с активными металлами или водородом.
Как определить степень окисления сурьмы
По таблице Менделеева
- Семейство: p-элемент (полуметалл).
- Валентные электроны: 5 (2 на s-подуровне и 3 на p-подуровне).
- Атомная масса сурьмы: 121,7 а.е.м.
По валентности (Число связей)
Как и у азота с фосфором, валентность сурьмы чаще всего равна III или V.
- В трихлориде (SbCl3): Атом сурьмы образует три связи с хлором. Его валентность — III, а степень окисления равна +3.
- В пентаоксиде (Sb2O5): Сурьма образует пять связей с кислородом. Валентность — V, СО сурьмы — +5.
По электронной конфигурации
- Электронная формула сурьмы: [Kr] 4d10 5s2 5p3.
- Атому сурьмы степени окисления +5 достичь выгодно при взаимодействии с фтором или кислородом, так как это освобождает весь внешний слой.
Для просмотра значений квантовых чисел электронов используй таблицу квантовых чисел.
По химическому соединению (Алгебраический расчет)
Пример для HSb(OH)6 (сурьмяная кислота):
Сумма СО равна 0. Водород +1, Кислород -2. Группа OH в сумме дает -1.
1 + x + 6 · (-1) = 0
1 + x — 6 = 0 ⇒ x = +5
Примеры степеней окисления сурьмы
| СО | Характеристика | Примеры соединений |
|---|---|---|
| +5 | Высшая. Характерна для антимонатов и пентагалогенидов. | SbCl5, Sb2O5, KSbO3 |
| +3 | Самая стабильная. Основная форма в природе. | Sb2S3, SbCl3, Sb2O3 |
| 0 | Металл. Компактное состояние или сплав. | Sb (серый полуметалл) |
| -3 | Отрицательная. Встречается в стибине и антимонидах. | SbH3, Na3Sb, Mg3Sb2 |
Шпаргалка для сурьмы
- +5 — высшая степень, пентафторид SbF5 является одной из самых сильных кислот Льюиса.
- Токсичность — соединения сурьмы в степенях +3 и +5 ядовиты и требуют осторожного обращения.
- Огонь — оксиды сурьмы используются как антипирены (добавки, снижающие горючесть материалов).
Пример решения задачи:
▶️ Дано:
Соединение: SbCl3.
⌕ Найти:
Определите СО сурьмы.
✨ Решение:
Хлор (Cl) имеет СО -1. Уравнение: x + 3 · (-1) = 0 → x — 3 = 0 → x = +3.
✅ Ответ:
Sb(+3).
Проверка знаний
Показать ответы
Правильные ответы: 1, 2, 4, 5.
Разбор ошибок:
3 — неверно: в стибине сурьма более электроотрицательна, чем водород, поэтому её СО равна -3.
Часто задаваемые вопросы
Наиболее распространенными и устойчивыми являются степени окисления +3 и +5.
Формально — да, но структурно это обычно смесь состояний +3 и +5.
Соединения Sb(+5), такие как SbF5, крайне реакционноспособны и агрессивны по отношению к органическим веществам.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.