Синильная кислота, также известная как цианистоводородная кислота или гидроцианид, является неорганическим химическим соединением с формулой HCN.
Эта жидкость бесцветна, очень летуча, горюча, подвижна и чрезвычайно ядовита.
Важно отметить, что у некоторых людей нет способности ощущать ее неприятный запах, поскольку чувствительность к нему различается в разных частях населения.
Синильная кислота может содержаться в некоторых растениях, коксовом газе, а также образовываться при пиролизе органических соединений, содержащих азот.
Например, она может образовываться в табачном дыме или при термическом разложении нейлона и полиуретанов.
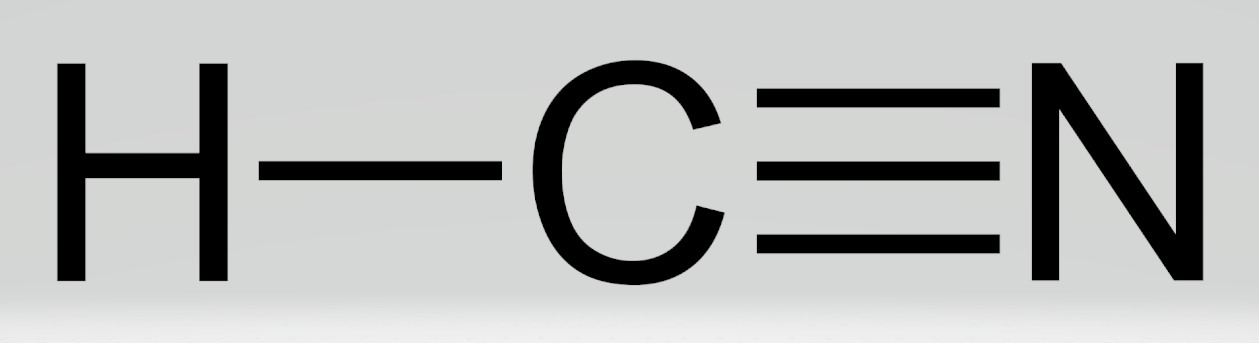
Где: H — атом водорода, C — атом углерода, N — атом азота, — — одинарная связь между водородом и углеродом, ≡ — тройная связь между углеродом и азотом.
Содержание страницы
- 1. Что такое синильная кислота
- 1.1. Структура HCN
- 1.2. Физические свойства
- 1.3. Химическое название HCN
- 1.4. В природе
- 1.5. Получение
- 1.6. Применение
- 1.7. Быстрые ответы?
Что такое синильная кислота
Название кислоты HCN — цианистый водород, высоколетучая, бесцветная и чрезвычайно ядовитая жидкость. Температура кипения 26 ° C и замерзания -14 ° C.
Раствор этого соединения в воде называется синильной кислотой. Он был открыт в 1782 году шведским химиком Карлом Вильгельмом Шееле, который приготовил его из пигмента берлинской лазури.
Соединения цианистого водорода используются в нескольких химических процессах, включая фумигацию, закалку чугуна и стали, нанесение гальванических покрытий.
Следовательно, обогащение руд. Он также используется при получении акрилонитрила, который используется в производстве акриловых волокон, синтетического каучука и пластмасс.
Структурная формула синильной кислоты приведена выше.
Цианистый водород очень токсичен, поскольку он подавляет окислительные процессы в клетках.
Люди могут переносить 50-60 частей соединения на миллион частей воздуха в течение часа без серьезных затрат, но воздействие концентраций 200-500 частей на миллион частей воздуха в течение получаса обычно приводит к летальному исходу.
Цианистый водород является отличным растворителем для ряда солей, но не находит широкого применения в качестве растворителя из-за своей токсичности.
В чистом виде соединение может быть стабильным, но оно легко полимеризуется в присутствии основных веществ, таких как аммиак или цианид.
Соли, используемые при добыче руд, в электролитических процессах и обработке стали.
Органические соединения, такие как альдегиды и кетоны, образуют цианогидрины, которые являются промежуточными продуктами во многих органических синтезах.
Структура HCN
Химическая формула синильной кислоты — HCN. Ее молекулярная формула записывается как CHN, а ее молярная масса составляет 27,03 г / моль.
Цианистый водород может представлять собой простую плоскую молекулу с тройной связью между атомами углерода и азота, рисунок выше.
Интересный факт: имеет характерный запах горького миндаля. Примерно у 20-40% населения мира отсутствует ген, ответственный за рецепторы, воспринимающие этот запах.
Физические свойства
HCN встречается в виде бледно-голубой бесцветной прозрачной жидкости (синильная кислота) или бесцветного газа (цианистый водород).
Синильная кислота имеет плотность 0,687 г/ мл и кипит при температуре чуть выше 25,6 ° C (78,1 ° F).
Молярная масса 27,0253 г/моль. Плотность 0,687 г/см3. Динамическая вязкость 0,201 Па·с. Энергия ионизации 13,6 ± 0,1 эВ и 2,2E−18 Дж.
Он имеет отчетливый запах горького миндаля, который используется для определения присутствия этого очень ядовитого вещества.
Химическое название HCN
Его химическое название — цианистый водород, который является слабой кислотой и частично ионизируется в воде с образованием H+ (или H3O+) и цианид-аниона CN—.
HCN + H2O → H3O+ + CN—
Он вступает в реакцию с основаниями с образованием солей, называемых цианидами.
HCN + KOH → KCN + H2O
В природе
HCN естественным образом содержится в косточках некоторых фруктов, таких как вишня, яблоки и абрикосы, а косточки фруктов содержат небольшое количество цианогидринов из HCN.
Получение
HCN получают в лабораторных условиях путем добавления кислот к цианистым солям щелочных металлов (таким как NaCN, KCN и др.)
HCl + NaCN → HCN + NaCl
Применение
Несмотря на свою токсичность, HCN является необходимым реагентом, используемым в производстве множества полезных промышленных химикатов.
Таких как цианид натрия, цианистый калий, метилметакрилат (мономер, используемый для производства полимеров и пластмасс), хелатирующие агенты EDTA и NTA, а также полимер нейлон.
Цианид натрия или калия используют для получения золота из их руд.
HCN также используется для приготовления пестицидов и боевых отравляющих веществ.
Быстрые ответы?
При вдыхании в небольших концентрациях наблюдается царапанье в горле, горький вкус во рту, головная боль, тошнота, рвота, боли за грудиной. При нарастании интоксикации уменьшается частота пульса, усиливается одышка, развиваются судороги, наступает потеря сознания.
Она встречается в виде химических соединений, к числу которых относятся гликозиды. Амигдалин содержится в семенах горького миндаля, косточках персиков, абрикосов, слив, вишен и др.
Индивидуальная защита: газонепроницаемый костюм химической защиты, включая автономный дыхательный аппарат.
