Диффузия это проникновение частиц одного вещества между частицами другого, происходящее в процессе молекулярного движения, называется диффузией.
Диффузия ускоряется с повышением температуры, так как при этом повышается интенсивность молекулярного движения частиц.

Содержание страницы
- 1. Что такое диффузия и осмос
- 1.1. Осмос
- 1.2. Значение диффузии
- 1.3. Закон диффузии Фика
- 1.4. Первый закон Фика
- 1.5. Второй закон диффузии Фика
- 1.6. Второй закон Фика
- 1.7. Многокомпонентная диффузия
- 1.8. Математическая формулировка закона Фика
- 1.9. Применение закона Фика
- 1.10. Важность закона Фика
- 1.11. Понятие закона диффузии Фика
- 1.12. Диффузия вопросы ответы?
Что такое диффузия и осмос
Наиболее интенсивно диффузия происходит между газами или между газом и жидкостью.
Газы адсорбируются на поверхности жидкости, а затем путем диффузии распространяются по всей ее массе. Этот процесс называется абсорбцией, или растворением газа в жидкости.
По мере растворения газа интенсивность этого процесса снижается и, наконец, наступает состояние насыщения, когда количество молекул газа, поступающего в жидкость, равняется количеству молекул газа, покидающих ее.
Количество газа, которое может раствориться в единице объема жидкости, зависит от природы жидкости и газа, от парциального давления газа над жидкостью и от температуры.
При не слишком высоких давлениях количество газа, растворяющегося в жидкости (при данной температуре и при насыщении), прямо пропорционально парциальному давлению газа над жидкостью (закон Генри).
При повышении температуры растворимость газа в жидкостях обычно уменьшается.
Диффузия быстро протекает в газах, а в жидкостях медленнее и очень медленно в твердых телах. Процесс диффузии ускоряется с повышением температуры, с уменьшением вязкости среды и размеров частиц.
При снижении парциального давления газа над поверхностью жидкости растворенный в ней газ выделяется в форме пузырьков.
Это явление, например, лежит в основе кессонной болезни. На глубине водолаз дышит воздухом под повышенным давлением и кровь его насыщается газами воздуха, особенно азотом (кислород частично связывается с гемоглобином).
В результате резкого снижения давления при возвращении на поверхность воды азот выделяется из крови в виде пузырьков, которые могут вызвать газовую эмболию.
Диффузия может происходить также и через различные пористые перегородки или перепонки (мембраны).
В легких, например, кислород из воздуха поступает в кровь путем диффузии через стенки альвеол, затем, растворяясь в ней, разносится по всему организму.
Осмос
Подобные перепонки называются полупроницаемыми, а само явление избирательного прохождения тех или иных веществ через перепонки называется осмосом.
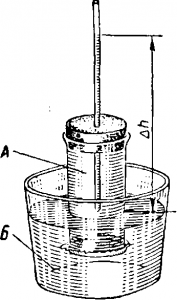
Прибор для демонстрации осмоса
Затянем пергаментом нижний конец трубки А с раствором сахара, а верхний закроем пробкой с манометрической трубкой (рис. 2).
Опустим нижний конец трубки в сосуд Б с дистиллированной водой. Через некоторый промежуток времени уровень в манометрической трубке поднимается.
В результате осмоса воды через полупроницаемую перегородку давление в трубке с раствором увеличилось на величину ∆р, соответствующую давлению столба жидкости высотой h.
Это давление противодействует дальнейшему проникновению воды в раствор сахара и при определенной его величине осмос прекращается.
Величину, равную избыточному давлению со стороны раствора, которая необходима для прекращения диффузии растворителя через полупроницаемую перепонку, называют осмотическим давлением раствора.
Вант-Гофф установил, что:
Для растворов достаточно малой концентрации осмотическое давление любого вещества в растворе равняется давлению, которое это вещество имело бы в газообразном состоянии в таком же объеме и при такой же температуре, как объем и температура данного раствора.
Отсюда следует также, что, подобно давлению газа при постоянном объеме и температуре, осмотическое давление зависит только от числа молекул растворенного вещества, но не зависит ни от его природы, ни от природы растворителя.
Кроме того, осмотическое давление раствора, содержащего различные вещества, равняется сумме осмотических давлений, которые имели бы каждый из этих веществ в отдельности.
Значение диффузии
Диффузия и особенно осмос имеют большое значение для живых организмов, так как эти явления лежат в основе обмена вещества как внутри организма, так и между организмом и внешней средой.
Оболочки клеток являются полупроницаемыми. Благодаря этому растворы питательных веществ проходят снаружи внутрь клетки, а продукты жизнедеятельности клетки выводятся из нее в окружающую среду.
Осмотическое давление и человек
Осмос имеет решающую роль в распределении воды в организмах. Например, осмотическое давление в клетках растений достигает 5—10 атм, благодаря чему они активно всасывают воду.
Осмотическое давление крови человека составляет около 8 атм. В основном оно создается содержащимися в плазме крови растворами неорганических солей.
Белки, составляющие основное количество растворенных в плазме веществ, благодаря высокому молекулярному весу имеют в растворе относительно малое число молекул создают осмотическое давление порядка только 4—5 мм рт. ст.
Закон диффузии Фика
Закон диффузии Фика говорит, что диффузия обрабатывает движение молекул из области более высокой концентрации в область более низкой концентрации.
Диффузионный процесс, подчиняющийся законам Фика, называется нормальной диффузией или диффузией Фика.
Диффузионный процесс, который не подчиняется законам Фика, известен как аномальная диффузия или нефиковская диффузия.
Есть два закона-полупроводники, т. Е. Первый закон Фика используется для получения второго закона Фика, который аналогичен уравнению диффузии.
Согласно закону диффузии Фика, “Молярный поток, обусловленный диффузией, пропорционален градиенту концентрации”.
Скорость изменения концентрации раствора в точке пространства пропорциональна второй производной концентрации с пространством.
Первый закон Фика
Движение растворенного вещества от более высокой концентрации к более низкой концентрации через градиент концентрации.
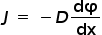
Где,
J: диффузионный поток
D: диффузия
φ : концентрация
x: положение
Второй закон диффузии Фика
Второй закон диффузии Фика представляет собой линейное уравнение с зависимой переменной, являющейся концентрацией рассматриваемых химических веществ.
Распространение каждого химического вида происходит независимо. Эти свойства упрощают численное моделирование систем переноса массы ,описанных во втором законе Фика.
При моделировании диффузии часто рекомендуется начинать с предположения, что все коэффициенты диффузии равны и не зависят от температуры, давления и т. д.
Такое упрощение гарантирует линейность уравнений переноса массы в моделируемой области, а также позволяет упростить корреляции с известными аналитическими пределами.
Это предположение можно ослабить, как только поведение системы со всеми одинаковыми коэффициентами диффузии будет хорошо понято.
Размерное исследование второго закона Фика показывает, что в диффузионных процессах существует фундаментальная зависимость между прошедшим временем и квадратом периода, в течение которого происходит диффузия.
Понимание этой взаимосвязи очень важно для точного численного моделирования диффузии.
Второй закон Фика
Предсказание изменения концентрации вместе со временем из-за диффузии.
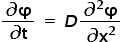
Где,
D: диффузия
t: время
x: положение
φ: концентрация
Многокомпонентная диффузия
В случае конденсированных жидкостей или газовых смесей, где в больших массовых долях присутствует более одного химического вещества, коэффициент диффузии больше не может рассматриваться как постоянный или независимый от состава.
Взаимодействие молекул разных видов друг с другом слишком распространено для физического описания, чтобы игнорировать эти межмолекулярные зависимости.
Таким образом, коэффициент диффузии становится тензором, и уравнение диффузии модифицируется, чтобы связать массовый поток одного химического вещества с градиентами концентрации всех присутствующих химических веществ.
Необходимые уравнения сформулированы как описание распределения Максвелла-Стефана. Они часто используются для описания газовых смесей, таких как синтез-газ в реакторе или смесь кислорода, азота и воды в катоде топливного элемента.
В диффузии Максвелла-Стефана рациональным выбором зависимых переменных являются не концентрации видов, а мольные или массовые доли видов (xi и ωi соответственно).
Диффузионный массовый поток каждого вида, в свою очередь, выражается на основе мольных градиентов или массовых долей с использованием Dik многокомпонентные коэффициенты диффузии.
Они симметричны, так что n-компонентная система требует n(n-1)/2 независимых коэффициентов для параметризации скорости диффузии ее компонентов.
Такие количества часто неизвестны для четырехкомпонентных или более сложных смесей. Упрощения могут быть применены к уравнениям Максвелла-Стефана, чтобы использовать эквивалентную диффузию закона Фика.
Системы, чаще всего включающие концентрированные смеси, требуют конвекции и сохранения импульса (потока жидкости), которые должны быть разрешены диффузией.
В материале, состоящем из двух или более химических веществ, в котором имеются пространственные неоднородности состава.
Существует движущая сила для интердиффузии различных молекулярных частиц, чтобы сделать состав материала однородным.
В смеси всего двух молекул диффузионный поток каждого молекулярного вида пропорционален градиенту его состава.
Эта пропорциональность известна как закон диффузии Фика и в небольшой степени является аналогом массопереноса закона вязкости Ньютона и закона теплопроводности Фурье
Математическая формулировка закона Фика
Математическая формулировка закона Фика должна выполняться со значительной осторожностью, потому, что существует множество способов представления структуры вещества и потому что важно его администрировать.
Применение закона Фика
-
Биологическое применение:
Поток = −P (c2 − c1) (из первого закона Фика)
Где,
P: проницаемость
c2 — c1: разница в концентрации
-
Жидкости — закон Фика относится к двум смешивающимся жидкостям, когда они вступают в контакт, и диффузия происходит в макроскопической точке.
-
Изготовление полупроводниковых уравнений диффузии Закон Фика используется для изготовления интегральных схем.
-
Фармацевтическое применение
-
Применение в пищевой промышленности.
Важность закона Фика
Газы, растворенные в жидкостях, беспорядочно перемещаются по жидкости в термодинамическом процессе, который хорошо описывается как диффузия.
Скорости диффузии газа в непрерывном теле жидкости постоянны, наличие барьера внутри жидкости может существенно повлиять на скорость диффузии газа.
Скорость, с которой газы могут диффундировать через мембраны, является важным аспектом физиологии дыхания, поскольку кислород и углекислый газ должны пересекать альвеолярную мембрану в процессе газообмена.
Важно знать физические законы, которые управляют диффузией растворенного газа через мембраны, поскольку они в значительной степени информируют наше понимание процесса газообмена на альвеолярной мембране.
Закон Фика описывает скорость, с которой растворенный газ диффундирует через мембрану, учитывая определенные свойства мембраны и газа.
Понятие закона диффузии Фика
Адольф Фик впервые сообщил о законах, регулирующих перенос массы с помощью диффузионных средств.
Работа Фика была вдохновлена Томасом Грэмом, который не смог предложить фундаментальные законы, благодаря которым Фик станет знаменитым.
Закон Фика аналогичен отношениям, открытым в ту же эпоху другими выдающимися учеными.
Эксперименты Фика всегда касались измерения концентраций и потоков соли, диффундирующей между двумя резервуарами через трубки с водой.
Хорошо известно, что работа Фика в первую очередь касалась диффузии в жидкостях, потому что в то время диффузия в твердых телах вообще не считалась возможной.
Теперь мы можем сказать, что законы Фика являются основными для понимания диффузии в твердых телах, жидкостях и газах.
Когда диффузионный процесс не следует законам Фика,его называют нефиковским.
Диффузия вопросы ответы?
Приведите примеры диффузии в окружающем мире?
Перемешивание запахов цветов в воздухе, всасывание корнями растений воды и минеральных солей, обмен кислородом воздуха в дыхательных системах животного мира и т.д.
Что такое закон диффузии Фика?
Закон диффузии Фика описывает механизм диффузии (движение молекул от более высокой концентрации к более низкой концентрации) для решения коэффициента диффузии, разработанного Адольфом Фиком в 1855 году.
Есть два закона, которые взаимосвязаны, т. Е. Первый закон Фика используется для получения второго закона Фика, который аналогичен уравнению распределения.
Каковы недостатки закона диффузии Фика?
В уравнениях переноса излучения также важен первый закон Фика. Однако, когда постоянная диффузии мала и излучение ограничено скоростью света, а не сопротивлением вещества, через которое проходит излучение, оно становится ошибочным.
Каковы три переменные в числителе закона диффузии Фика?
Закон Фика гласит, что химическая природа мембраны, площадь поверхности мембраны, градиент парциального давления газа через мембрану и толщина мембраны определяют скорость диффузии газа через проницаемую мембрану.
