Теория:
Франций (Fr) в периодической системе: 7‑й период, 1‑я группа (по устаревшей классификации — IА), атомная масса [223] а.е.м.
Занимает положение в 7‑м периоде, что определяет его статус самого тяжелого и химически активного щелочного металла среди элементов главной подгруппы I группы.
Будучи химическим гомологом (аналогом) цезия, он проявляет свойства типичного металла с крайне низкой энергией ионизации.
Его поведение продиктовано наличием единственного валентного электрона на удаленной 7s-орбитали.
А его нахождение в 1‑й группе (ранее — главная подгруппа I группы) задает его ключевые параметры:
- Постоянную валентность I.
- Единственную возможную степень окисления +1, что характерно для всех щелочных металлов.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Rn] 7s1.
На которой наглядно можно определить его положение как завершающего представителя s-блока, находящегося под цезием и открывающего 7-й период.
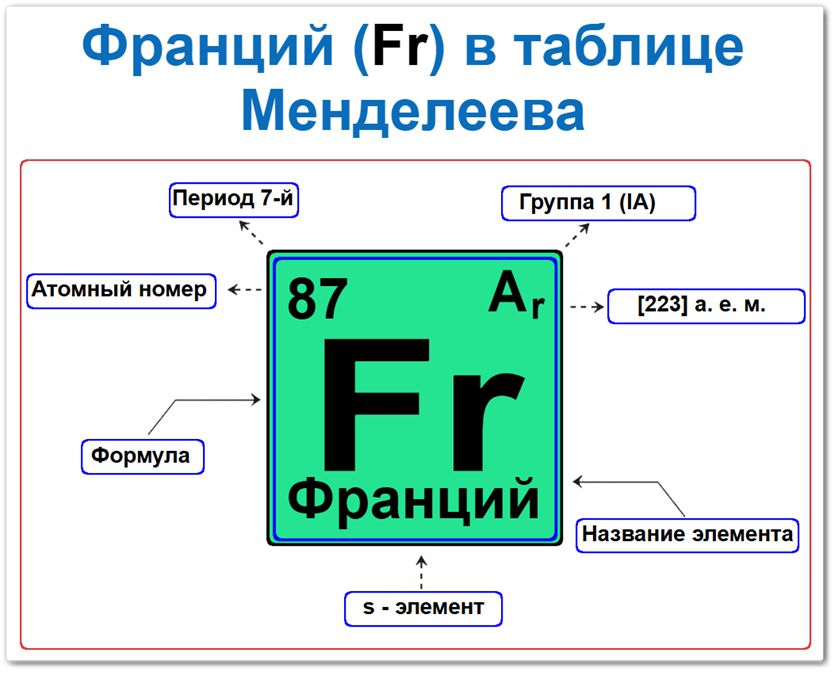
Франций в таблице Менделеева можно определить на основании закона периодичности: положение в группе и периоде, а также порядкового номера / атомный номер (Z = 87).
Содержание страницы
- 1. Как определить положение Франция в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 87)
- 3. Название и символ
- 4. Группа (1 / I A)
- 5. Период (7‑й)
- 6. Относительная атомная масса (Ar)
- 7. s‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Франция по Таблице Менделеева
- 9. Проверка знаний: Как определить франций по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Франция в Таблице Менделеева
Локация франция в таблице описывается характеристиками его нестабильного радиоактивного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (вертикальный ряд щелочных металлов).
- Период (горизонтальный ряд).
- Электронное семейство (франций — s‑элемент).
Порядковый номер / атомный номер (Z = 87)
- Служит уникальным кодом элемента в ряду естественных радиоактивных металлов.
- В ядре — 87 протонов; в нейтральной оболочке — 87 электронов.
- Электронное строение: [Rn] 7s1.
Важно: Наличие 1 электрона на внешнем 7s-подуровне делает его самым электроположительным элементом (согласно теоретическим расчетам, хотя релятивистские эффекты вносят свои коррективы).
Название и символ
- Название: «франций» (назван Маргаритой Перей в честь её родины — Франции).
- Символ: Fr.
- Примечание: Это последний элемент, обнаруженный в природе (в составе урановых руд), а не синтезированный искусственно в ускорителе.
Группа (1 / I A)
Расположен в 1‑й группе; по классической классификации — главная подгруппа I группы (подгруппа лития).
Химический потенциал:
- Валентность франция: постоянная валентность I.
- Степень окисления: всегда +1 (за исключением крайне редких условий).
- Реакционная способность: обладает колоссальной скоростью взаимодействия с водой и кислородом.
Период (7‑й)
Находится в 7‑м периоде — его электроны распределены по семи энергетическим уровням.
Влияние на свойства:
- Максимальный радиус: Имеет один из самых больших атомных радиусов в таблице, что облегчает отдачу валентного электрона.
- Релятивистский вклад: Из-за огромного заряда ядра валентный 7s-электрон движется настолько быстро, что его масса возрастает, что делает франций чуть менее активным, чем предсказывает простая экстраполяция.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Fr) ≈ [223] а.е.м. (для изотопа 223Fr).
- Определение: средняя масса наиболее стабильного природного изотопа.
- Стабильность: Франций чрезвычайно нестабилен. Самый долгоживущий изотоп 223Fr имеет период полураспада всего 22 минуты.
Все значения для всех элементов можно узнать в таблице атомных масс.
s‑Элемент (электронное семейство)
Застраивающимся является внешний s‑подуровень (7s1).
Специфика блока: Это типичный s-металл. Его свойства полностью определяются единственным электроном, который слабо связан с ядром из-за сильного экранирования внутренними слоями.
Определение энергетических уровней Франция по Таблице Менделеева
Положение Франция (Fr) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 7-й период (Количество этажей)
Франций находится в седьмой строке таблицы. Номер периода совпадает с количеством электронных слоев.
- Итог: У Франция 7 энергетических уровней.
2. Список «жильцов» (Распределение электронов)
Атомный номер Франция — 87. Его 87 электронов распределены по уровням следующим образом:
Fr ) 2 ) 8 ) 18 ) 32 ) 18 ) 8 ) 1
Для сравнения: У соседа сверху, Цезия (55), на два электронных слоя меньше, но структура внешних оболочек (…8, 1) идентична.
3. 1-я группа (Химический характер)
Франций стоит в одной колонке с Литием, Натрием и Калием.
- s-элемент: Его металлическая природа выражена максимально ярко.
- Место в блоке: Он является самым тяжелым щелочным металлом, что делает его «королем» восстановителей в химии.
Проверка знаний: Как определить франций по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Франций (Fr) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 87. Точное место Франция в атомном ряду.
- 2) s-элемент 7-го периода. Характеристика его электронной структуры и положения.
- 3) Щелочной металл. Это определяет его химическое поведение и сходство с цезием.
- 4) Ошибка. Франций слишком радиоактивен и редок для строительства.
- 5) Ошибка. Это типичный металл, а не газ.
- 6) Ошибка. Все изотопы франция распадаются очень быстро (максимум 22 минуты).
Часто задаваемые вопросы:
Он расположен в 1-й группе (щелочные металлы) и 7-м периоде. Атомный номер — 87.
Поскольку франций находится в 7-м периоде, у него 7 энергетических уровней. Электронная схема: 2, 8, 18, 32, 18, 8, 1.
Наиболее стабильным является изотоп франций-223, но даже его период полураспада составляет всего около 22 минут.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.