Теория:
Кремний (Si) в периодической системе: 3‑й период, 14‑я группа (по устаревшей классификации — IV A), атомная масса 28,085 а.е.м.
Занимает положение в 3‑м периоде, что определяет его принадлежность к p-элементам и группе металлоидов.
Кремний — второй по распространенности элемент в земной коре (после кислорода). В чистом виде встречается крайне редко, обычно находится в виде кремнезема (SiO2) или силикатов.
Будучи химическим элементом p-блока, он располагается в правой части таблицы Менделеева, находясь под углеродом и над германием, разделяя свойства металлов и неметаллов.
Нахождение Кремния в 14‑й группе и наличие четырех валентных электронов обуславливают его ключевые параметры:
Постоянную валентность IV.
А также широчайшее применение в строительстве (песок, кирпич, цемент), электронике (чипы, транзисторы) и производстве стекла и оптики.
Структура атома подтверждается его электронной формулой (конфигурацией):
1s2 2s2 2p6 3s2 3p2 (или [Ne] 3s2 3p2).
На которой наглядно можно определить его положение как p-блочного элемента, находящегося в процессе заполнения внешнего 3p-подуровня.
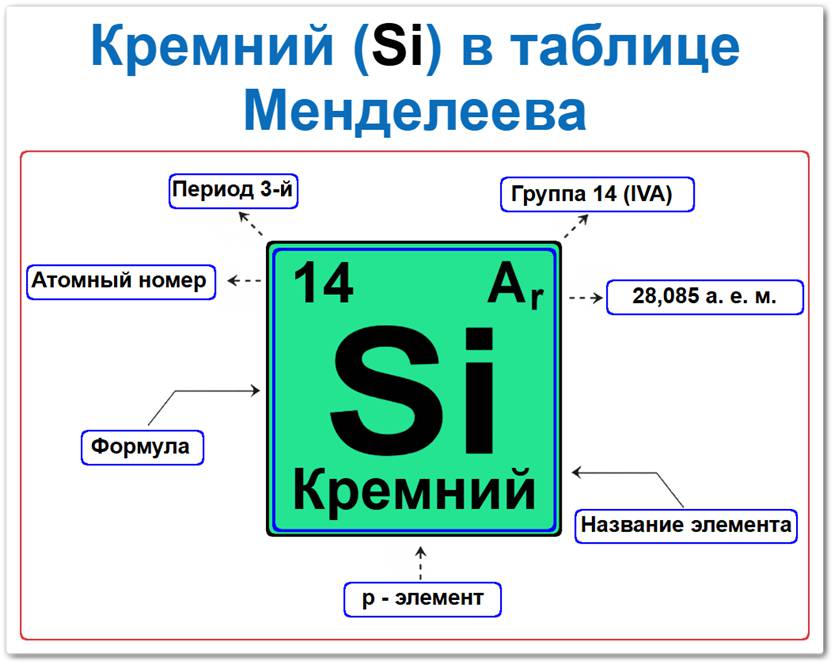
Кремний элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду металлоидов период 3, группа 14, а также по его порядковому номеру (Z = 14).
Содержание страницы
- 1. Как определить положение Кремния в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 14)
- 3. Название и символ
- 4. Группа (14 / IV A)
- 5. Период (3‑й)
- 6. Относительная атомная масса (Ar)
- 7. p‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Кремния по Таблице Менделеева
- 9. Проверка знаний: Как определить кремний по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Кремния в Таблице Менделеева
Локация кремния в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (14-я группа, подгруппа углерода).
- Период (горизонтальный ряд).
- Электронное семейство (кремний — p‑элемент).
Порядковый номер / атомный номер (Z = 14)
- Служит уникальным кодом элемента в системе.
- В ядре — 14 протонов; в нейтральной оболочке — 14 электронов.
- Электронное строение: 2, 8, 4.
Важно: Для плотника кремний — это основа абразивов. Шлифовальная шкурка и заточные камни часто делаются из карбида кремния (SiC). В справочнике 1934 года кремниевые соединения описывались как основа керамической промышленности.
Название и символ
- Название: «кремний» (от др.-греч. krepnos — «утёс, гора», подчеркивает твердость кремня).
- Символ: Si (Silicium).
- Примечание: Впервые выделен в чистом виде Йёнсом Берцелиусом в 1824 году. Это темно-серый кристаллический элемент с металлическим блеском, очень хрупкий.
Группа (14 / IV A)
Расположен в 14‑й группе. В периодической системе кремний находится в одной вертикальной колонке с углеродом (сверху) и германием (снизу) и относиться к (подгруппе углерода).
Химический потенциал:
- Валентность кремния: типичная валентность IV.
- Степень окисления: от -4 до +4. Наиболее устойчивая — +4. Кремний образует прочные связи с кислородом, создавая основу почти всех минералов на Земле.
Период (3‑й)
Находится в 3‑м периоде — его электроны распределены по трем энергетическим уровням.
Влияние на свойства:
- Химическая активность: При обычных температурах кремний довольно инертен, но при нагревании активно реагирует с фтором и кислородом.
- Техническое значение: Кремний — главный полупроводник современности. Без него не работала бы Яндекс.Метрика и ваш сайт.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Si) ≈ 28,085 а.е.м.
- Определение: среднее значение массы природных изотопов, основным из которых является стабильный Кремний-28.
Все значения для всех элементов можно узнать в таблице атомных масс.
p‑Элемент (электронное семейство)
Заполняется внешний 3p‑подуровнь (3p2).
Специфика блока: Будучи металлоидом, кремний сочетает блеск металла и хрупкость неметалла. Его электропроводность растет при нагревании, что противоположно свойствам металлов.
Определение энергетических уровней Кремния по Таблице Менделеева
Положение Кремния (Si) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 3-й период (Количество этажей)
Номер периода определяет число электронных слоев.
- Итог: У Кремния 3 энергетических уровня.
2. Список «жильцов» (Распределение электронов)
Атомный номер Кремния — 14. Его 14 электронов распределены по уровням следующим образом:
Si ) 2 ) 8 ) 4
3. 14-я группа (Химический характер)
Кремний — элемент главной подгруппы IV группы (или 14-й группы).
- p-элемент: Относится к семейству металлоидов (полуметаллов).
- Металлические свойства: Полупроводник, тугоплавкий, химически стоек к большинству кислот.
Проверка знаний: Как определить кремний по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Кремний (Si) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 14. Соответствует заряду ядра (14 протонов).
- 2) 3-й период, 14-я группа. Его адрес в периодической системе.
- 3) p-элемент. Показывает структуру внешней электронной оболочки.
- 4) Ошибка. Щелочные металлы — это 1-я группа.
- 5) Ошибка. Кремний — твердое кристаллическое вещество.
- 6) Ошибка. Номер 32 принадлежит германию.
Часто задаваемые вопросы:
Кремний расположен в 3-м периоде, 14-й группе. Порядковый номер — 14.
У кремния 3 энергетических уровня.
Электронная схема: 2, 8, 4.
Кремний является p-элементом. В его атоме заполняется внешний p-подуровень.
