Теория:
Германий (Ge) в периодической системе: 4‑й период, 14‑я группа (по устаревшей классификации — IV A), атомная масса 72,63 а.е.м.
Занимает положение в 4‑м периоде, что определяет его принадлежность к полуметаллам (металлоидам).
Германий — один из немногих элементов, существование которых было предсказано Д. И. Менделеевым (как «экасилиций») до его фактического открытия.
Являясь химическим аналогом кремния и олова, он входит в состав p-элементов, располагаясь в правой части таблицы Менделеева на границе между металлами и неметаллами.
Нахождение Германия в 14‑й группе и особенности строения его внешней оболочки обуславливают его ключевые параметры:
Наиболее характерные валентности II и IV.
А также стратегическое применение в производстве полупроводников, волоконной оптики и инфракрасной техники.
Структура атома подтверждается его электронной формулой (конфигурацией):
[Ar] 3d10 4s2 4p2.
На которой наглядно можно определить его положение как p-блочного элемента, у которого заполняется 4p-подуровень.
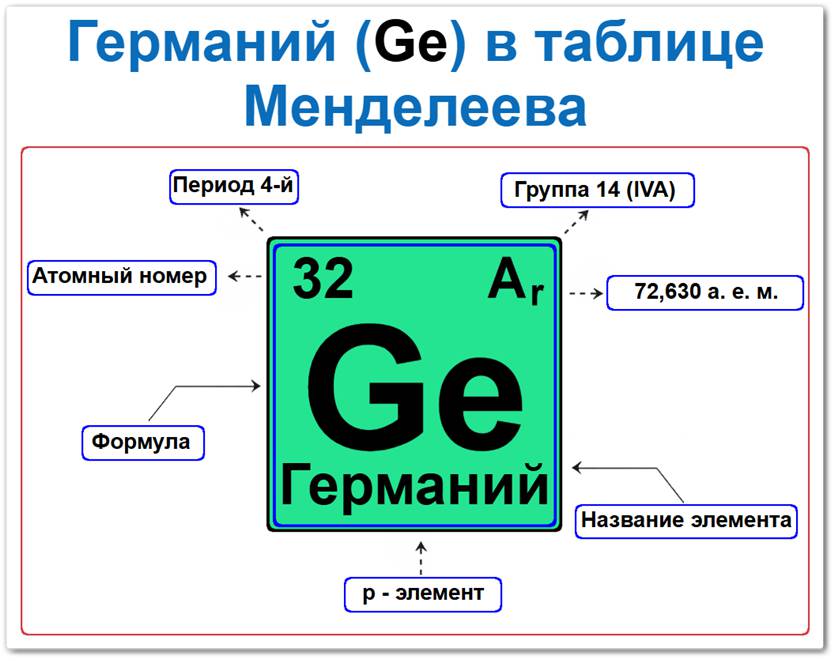
Германий элемент таблицы Менделеева который можно определить на основании закона периодичности: положение в ряду полупроводников период 4, группа 14, а также по его порядковому номеру (Z = 32).
Содержание страницы
- 1. Как определить положение Германия в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 32)
- 3. Название и символ
- 4. Группа (14 / IV A)
- 5. Период (4‑й)
- 6. Относительная атомная масса (Ar)
- 7. p‑Элемент (электронное семейство)
- 8. Определение энергетических уровней Германия по Таблице Менделеева
- 9. Проверка знаний: Как определить германий по таблице Менделеева
- 10. Часто задаваемые вопросы:
Как определить положение Германия в Таблице Менделеева
Локация германия в таблице описывается характеристиками его атомного ядра — его «химическим аттестатом» (паспортом):
- Порядковый номер (атомный номер).
- Наименование (название) элемента.
- Группа (14-я группа, подгруппа углерода).
- Период (горизонтальный ряд).
- Электронное семейство (германий — p‑элемент).
Порядковый номер / атомный номер (Z = 32)
- Служит уникальным кодом элемента в системе.
- В ядре — 32 протона; в нейтральной оболочке — 32 электрона.
- Электронное строение: [Ar] 3d10 4s2 4p2.
Важно: Германий является классическим полупроводником. Его электрическая проводимость сильно зависит от температуры и наличия примесей, что сделало его основой первых транзисторов.
Название и символ
- Название: «германий» (в честь Германии, родины первооткрывателя).
- Символ: Ge.
- Примечание: Открыт Клеменсом Винклером в 1886 году в минерале аргиродите. В чистом виде — хрупкий, серебристо-белый металлоид с металлическим блеском.
Группа (14 / IV A)
Расположен в 14‑й группе. В периодической системе германий находится в одной вертикальной колонке с кремнием (сверху) и оловом (снизу).
Химический потенциал:
- Валентность германия: типичные валентности II и IV.
- Степень окисления: +4 (наиболее устойчивая) и +2. Соединения германия широко используются в современной микроэлектронике.
Период (4‑й)
Находится в 4‑м периоде — его электроны распределены по четырем энергетическим уровням.
Влияние на свойства:
- Химическая активность: Германий устойчив к воздействию воздуха и воды при комнатной температуре, растворяется только в сильных окислителях.
- Техническое значение: Прозрачность германия в инфракрасном диапазоне делает его незаменимым для линз приборов ночного видения.
Все значения элементов в полной сводной таблице параметров химических элементов (Z, Ar, Группа, Период).
Относительная атомная масса (Ar)
- Ar(Ge) ≈ 72,63 а.е.м.
- Определение: среднее значение массы природных изотопов, которых у германия пять (наиболее распространенный — германий-74).
Все значения для всех элементов можно узнать в таблице атомных масс.
p‑Элемент (электронное семейство)
Заполняющимся является 4p‑подуровень (4p2).
Специфика блока: Как p-элемент IV группы, германий проявляет амфотерные свойства с преобладанием неметаллических признаков, что характерно для элементов «диагонали Менделеева».
Определение энергетических уровней Германия по Таблице Менделеева
Положение Германия (Ge) в системе Менделеева — это готовый «паспорт» его внутреннего устройства.
1. 4-й период (Количество этажей)
Номер периода определяет число электронных слоев.
- Итог: У Германия 4 энергетических уровня.
2. Список «жильцов» (Распределение электронов)
Атомный номер Германия — 32. Его 32 электрона распределены по уровням следующим образом:
Ge ) 2 ) 8 ) 18 ) 4
3. 14-я группа (Химический характер)
Германий — элемент главной подгруппы IV группы (или 14-й группы).
- p-элемент: Относится к семейству углерода.
- Полупроводниковые свойства: Занимает промежуточное положение между металлами и диэлектриками.
Проверка знаний: Как определить германий по таблице Менделеева
Выберите три верных тезиса, которые однозначно характеризуют Германий (Ge) в структуре таблицы.
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3
- 1) Номер 32. Соответствует количеству протонов в ядре.
- 2) 4-й период, 14-й группа. Его координаты в системе Менделеева.
- 3) p-элемент. На внешнем уровне 4 электрона ($4s^2 4p^2$).
- 4) Ошибка. Инертные газы — это 18-я группа.
- 5) Ошибка. Германий — твердое кристаллическое вещество.
- 6) Ошибка. В 1-й группе находятся активные металлы, германий же полупроводник.
Часто задаваемые вопросы:
Германий расположен в 4-м периоде, 14-й группе. Его порядковый номер — 32.
У германия 4 энергетических уровня.
Электронная схема: 2, 8, 18, 4.
Германий является p-элементом. Его внешние электроны находятся на s- и p-орбиталях четвертого уровня.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.