Теория:
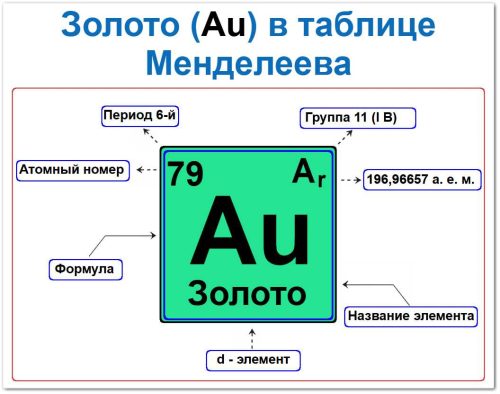
Золото (Au) — классический тяжёлый благородный металл, чьё химическое поведение и уникальные физические свойства определяются его положением в 5d‑блоке и сильными релятивистскими эффектами.
Идентификация золота основана на двух фундаментальных константах:
-
Атомный номер Z = 79 — определяет электронную конфигурацию (теоретически [Xe] 4f14 5d10 6s1).
-
Местоположение: 6‑й период, 11‑я группа (I B).
Это положение диктует свойства элемента:
-
Наличие одного валентного s‑электрона (по необычной конфигурации).
-
Классические степени окисления +1 и +3.
Содержание страницы
- 1. Как определить положение золота в Таблице Менделеева
- 2. Порядковый номер / атомный номер (Z = 79)
- 3. Название и символ
- 4. Группа (11‑я / I B)
- 5. Период (6‑й)
- 6. Относительная атомная масса Золота (Ar)
- 7. d‑Элемент (электронное семейство)
- 8. Проверка знаний: Как определить водород по таблице Менделеева
- 9. Часто задаваемые вопросы:
Как определить положение золота в Таблице Менделеева
Положение золота в таблице задаётся несколькими фундаментальными характеристиками — своего рода «химическим паспортом»:
- Порядковый номер и атомный номер.
- Название элемента.
- Группа (вертикальный столбец).
- Период (горизонтальный ряд).
- Электронный блок, (золото d‑элемент).
Порядковый номер / атомный номер (Z = 79)
-
Однозначно идентифицирует элемент.
-
В ядре — 79 протонов; в нейтральном атоме — 79 электронов.
-
Электронная конфигурация: [Xe] 4f14 5d10 6s1.
Примечание: наличие 4f‑подоболочки увеличивает атомную массу и плотность.
Название и символ
- Название: «Золото».
- Символ: Au (от лат. Aurum).
Группа (11‑я / I B)
Относится к металлам‑монетчикам (Cu, Ag, Au).
Степени окисления:
- +1: наиболее стабильная (например, AuCl).
- +3: наиболее распространённая (например, HAuCl4).
- 0: в чистом виде.
Особенность: провал электрона (d10 s1), что определяет склонность к отдаче s‑электрона.
Период (6‑й)
Имеет шесть энергетических уровней.
Особенности:
- Лантаноидное сжатие: радиус почти как у Ag, но масса выше.
- Высокая плотность (≈ 19,3 г/см3).
- Релятивистские эффекты: сжатие 6s‑орбитали и её низкая энергия.
Именно эти эффекты:
- Делают золото инертным (трудно потерять 6s‑электрон);
- Придают характерный жёлтый цвет (поглощение в сине‑зелёной области спектра).
Все значения для всех элементов можно узнать в таблице атомных масс.
Относительная атомная масса Золота (Ar)
Ar(Au) = 196,96657 ≈ 197 (безразмерная величина)
-
Значение: 196,96657 — это средневзвешенное значение масс природных изотопов золота.
Важно: золото — моноизотопный элемент.
Особенность: в природе оно существует почти на 100% как изотоп 197Au.
d‑Элемент (электронное семейство)
Золото — переходный металл, валентные электроны находятся на 5d‑ и 6s‑подуровнях.
Свойства:
- Высокая электропроводность;
- Благородный металл (не реагирует с кислородом, водой и большинством кислот).
- Проявляет переменную валентность (+1, +3).
- Принадлежность к d‑блоку объясняет высокую температуру плавления, каталитические свойства и образование комплексных соединений.
Проверка знаний: Как определить водород по таблице Менделеева
Отметьте три правильных утверждения, которые однозначно определяют Золото (Au) в Периодической системе.
По каким признакам можно безошибочно установить, что речь идёт именно о Золоте?
Показать верные ответы и пояснения
Правильные ответы: 1, 2, 3 (или 4, в зависимости от контекста)
- 1) В атомном ядре содержится ровно 79 протонов.
Это главный отличительный признак: атомный номер Z = 79 однозначно задаёт химический элемент. - 2) Находится в 6-м периоде и 11-й группе (I B).
Такое сочетание положения в таблице уникально для золота и определяет:- шесть электронных оболочек;
- принадлежность к металлам-монетчикам;
- влияние лантаноидного сжатия.
- 3) Полный набор валентных электронов описывается формулой: 6s1.
— Внимание: Это упрощенный ответ. Строго говоря, валентными являются 6s1 и 5d10. Но 6s1 отражает его необычную d10s1 конфигурацию. - 4) Является d-элементом с высокой электроотрицательностью.
Технически верно: Au является d-элементом и имеет аномально высокую ЭО (2,54 по Полингу), что объясняет его инертность, но этот признак не уникален. - 5) Имеет степень окисления +2.
Неверно: +1 и +3 являются основными, +2 встречается крайне редко и в основном в комплексных формах. - 6) Имеет самую высокую плотность среди всех известных металлов.
Неверно: Золото очень плотное, но самым плотным элементом является Осмий (Os), а за ним следует Иридий (Ir).
Часто задаваемые вопросы:
Атомный номер (Z) — 79. Относительная атомная масса (Ar) — 196,967 (округлённо 197).
Жёлтый цвет — следствие релятивистских эффектов в тяжёлом атоме, которые изменяют энергетический разрыв между 5d- и 6s-орбиталями, заставляя его поглощать синий свет и отражать жёлтый.
Инертность объясняется релятивистским сжатием 6s-орбитали. Это делает единственный валентный электрон очень трудным для отрыва, защищая атом от химических реакций.

Добавить комментарий
Для отправки комментария вам необходимо авторизоваться.